苄撑巴比妥类化合物在作为PCSK9拮抗剂和降低低密度脂蛋白中的应用的制作方法
本发明涉及一种苄撑巴比妥类化合物作为pcsk9拮抗剂的应用,本发明还涉及一种苄撑巴比妥类化合物在降低低密度脂蛋白中的应用,属于医药领域。
背景技术:
pcsk9是一种可溶性的内源性丝氨酸蛋白酶,为哺乳动物前蛋白转化酶家族的成员之一。主要在肝脏合成,在肠道、肾脏及脑也有低水平的表达。pcsk9在肝细胞中以非活化的形式存在,一旦释放到血液中就可以与ldl受体结合,透过细胞内吞作用进入肝细胞后降解。肝细胞表面的ldl受体就会减少,而血液中的ldl过多会导致血脂水平的升高。先天pcsk9变异人群的高酯血症发病率低。当前对于pcsk9拮抗剂的研究,仍然集中于单克隆抗体的方向,然而单克隆抗体作为药物应用于临床,在使用上有诸多不便。
技术实现要素:
本发明的目的在于提供一种苄撑巴比妥类化合物在作为pcsk9拮抗剂中的应用,以及进一步的,一种苄撑巴比妥类化合物在降低低密度脂蛋白中的应用。
本发明采用了如下技术方案:
一种苄撑巴比妥类pcsk9拮抗剂在作为pcsk9拮抗剂中的应用。
作为优选,本发明的应用中的苄撑巴比妥类pcsk9拮抗剂,为结构式v所示的化合物,
作为优选,结构式v中,r1,r2分别是h,-or’,-oc(o)r”,-oso2r”,-oc(o)nr’r”,-o-亚烷基-or’,-o-亚烷基-nr’r”,-so2r’,-s(o)r,-sr,-nr’r”,-nhc(o)r’,-nhc(o)or’,-nhc(o)nr’r”,-nr’c(o)r”,-nr’c(o)or”,-nr’c(o)nr”r”’中的任意一种,或者有取代或未经取代的烷基,环烷基,烯基,炔基,芳基,杂芳基中的任意一种,
x是取代或未经取代的烷基,环烷基,烯基,炔基,芳基,杂芳基中的任意一种,
y是取代或未经取代的烷基,环烷基,烯基,炔基,芳基,杂芳基中的任意一种。
作为优选,结构式v中,r1,r2分别是h,烷基。
作为优选,结构式v中,r1,r2是h。
作为优选,结构式v中,x是取代或未取代的芳基和杂芳基。
作为优选,结构式v中,y是取代或未取代的芳基和杂芳基。
作为优选,结构式v中,苄撑巴比妥类pcsk9拮抗剂形成组合物。
更优选的,苄撑巴比妥类pcsk9拮抗剂为下列三种化合物中的任意一种:
更优选的,苄撑巴比妥类pcsk9拮抗剂的用量为:100μm至50μm。
本发明还提供一种苄撑巴比妥类化合物在降低低密度脂蛋白中的应用,其特征在于,包括上述任意一项所述的苄撑巴比妥类化合物。
发明的有益效果
本发明的苄撑巴比妥类化合物在作为pcsk9拮抗剂中的应用和在降低低密度脂蛋白中的应用,能够有效降低低密度脂蛋白的浓度。并且,本发明提供了一种小分子的苄撑巴比妥类化合物作为pcsk9拮抗剂,制造方便且易于进入临床应用。
附图说明
图1是超速过滤亲和力筛选过程示意图;
图2是超速离心亲和力筛选过程示意图;
图3是超速离心亲和力筛选结果;
图4是ldl摄取实验的viva2956的结果;
图5是ldl摄取实验的阳性对照结果。
具体实施方式
以下结合附图来说明本发明的具体实施方式。
本实施方式提供一种化合物在降低血液中低密度脂蛋白中的应用。本应用中包括向受试者施用降低低密度脂蛋白有效量的本文化合物,混合物和组合物。
1.本发明的化合物具有图中v的结构:
其中,r1,r2独立的地是h,-or’,-oc(o)r”,-oso2r”,-oc(o)nr’r”,-o-亚烷基-or’,-o-亚烷基-nr’r”,-so2r’,-s(o)r,-sr,-nr’r”,-nhc(o)r’,-nhc(o)or’,-nhc(o)nr’r”,-nr’c(o)r”,-nr’c(o)or”,-nr’c(o)nr”r”’,或者有取代或未经取代的烷基,环烷基,烯基,炔基,芳基,杂芳基。
其中,x是取代或未经取代的烷基,环烷基,烯基,炔基,芳基,杂芳基。
其中,y是取代或未经取代的烷基,环烷基,烯基,炔基,芳基,杂芳基。
作为一种优选方案,r1,r2是h。
作为一种优选方案,x是杂芳基。
作为一种优选方案,y是取代的苯基。
本实施方式中在经过筛选之后,降低ldl的化合物v,较佳的为如下三种化合物:
三种化合物在本发明中分别被命名为viva2488,viva5589以及viva2956。
在这三种化合物中,降低ldl最佳的为viva2956。
含有本发明化合物的药物组合物,该药物组合物包含治疗有效量的游离形式或可药用盐形式的符合通式(i)的化合物作为活性成分;一种或多种药用载体物质和/或稀释剂。
以下介绍筛选的方法:
2.筛选与pcsk9具有较强结合力的分子:
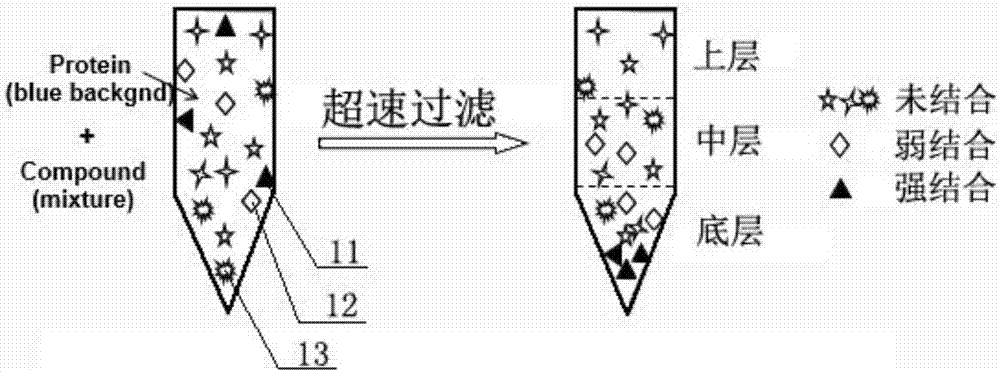
筛选方法a,超速过滤亲和力筛选,过程如图1所示,具体如下:
用筛选缓冲盐溶液25mmhepes,ph=7.9,300mmnacl准确配置浓度为50μmpcsk9蛋白和100μmldlr溶液,分别与2μm化合物viva2956进行混合,使总体积为550μl,在25℃下孵育30min后,取50μl作为样品r0,余下的500μl转移至蛋白超滤浓缩离心管中,pcsk9用30kd尺寸的超滤浓缩离心管,ldlr用10kd尺寸的超滤浓缩离心管。在转速13000rmp条件下离心至过滤膜上层剩余50μl蛋白溶液,加入450μl筛选缓冲盐溶液,混合均匀后继续离心至50μl,重复一次,最后得到50μl蛋白溶液作为样品r3。在r0和r3样品中加入150μl乙腈,混合均匀后,经转速13000rmp离心时间10min后除去沉淀的蛋白,得到上清溶液,取上清溶液进行超高效液相色谱与质谱联用(μplc/ms)分析,得到r0和r3样品中化合物viva2956的色谱峰高值r0和r3,计算pcsk9的r3/r0和ldlr。化合物viva2956的r3/r0=128%,ldlr的r3/r0=261%。
图1中蛋白14为pcsk9。化合物15为pcsk9拮抗剂。有拮抗作用的化合物15用实心三角形来表示,其它形状如星形和圆形表示待筛选的化合物分子。
筛选方法b,超速离心亲和力筛选,过程如图2所示,具体如下:
用筛选缓冲盐溶液25mmhepes,ph=7.9,300mmnacl准确配置浓度为30μm的pcsk9蛋白,与浓度为2μm的待筛选化合物进行混合,混合后总体积为150μl,在25℃下孵育30min,放入超速离心机,经转速90000rmp离心时间70min后取出,快速将样品分成上、中、下三层样品,分别为样品ct、cm、cb,每层样品体积为50μl,在每层样品中分别加入150μl乙腈,混合均匀,在转速13000rmp离心时间10min后除去沉淀的蛋白,得到上清溶液,取上清溶液进行lc/ms分析,得到ct和cb样品中化合物的色谱峰高值ct和cb,计算cb/ct的值,化合物viva2956的cb/ct=1.54。
图2中,第一化合物11,表示与pcsk9强结合的化合物,第二化合物12表示与pcsk9弱结合的化合物,第三化合物13表示与pcsk9不结合的化合物。
超速离心亲和力筛选结果图3所示,cb/ct的值越大,亲合结合越强。
下面的方法用来测定本发明化合物对pcsk9-ldlr之间结合的抑制活性。对于每个化合物测定了多个浓度下的抑制率,进而推算出其ic50值,即在此浓度下结合的ldlr为不加入化合物时的一半。
3.pcsk9-ldlr抑制活性的测定
3.1、材料
a、二甲基亚砜(dmso)(sigmad5879)
b、吐温20(tween20)
c、透明96孔板(costar42592)
d、检测缓冲液(25mmhepes,300mmnacl,ph7.9,0.2%bsa)
e、pbs缓冲液
f、链亲和素(streptavidin)
g、生物素化的pcsk9蛋白
h、带his标签的ldlr蛋白
i、一抗:anti-hisantibody(tiangenab102-02)
j、二抗:ab-hrp(santacruzbiotechnologysc-2005)
k、四甲基联苯胺(tmb)(bbilifesciencest0759)
l、待测化合物:stk952488、stk385589和zinc09042956
3.2、测试方法
在酶联免疫吸附试验(enzyme-linkedimmunosorbentassay(elisa))中,以链亲和素(streptavidin)包被实验板并特异性吸附上生物素化的pcsk9蛋白。随后分别加入化合物viva2488,viva5589或viva2956,常温孵育30分钟。之后再加入带his标签的ldlr蛋白,常温孵育1小时。反复洗板(pbs中加入0.2%tween20)后经由一抗、二抗的特异性偶联及tmb反应,最终经由450nm处消光来测定结合在板上的ldlr蛋白量。在实验中,随着三个化合物浓度的升高,pcsk9和ldlr的结合被逐渐阻断。最终测得的ic50值分别为1.8e-4m(viva488),2.9e-4m(viva5589)和4.9e-5m(viva2956)。
4.ldl摄取实验
本实验中所用材料的来源:
hepg2细胞来源上海中科院细胞库
ldluptakeassaykit购于biovision,cat.no.k585-100
pcsk9抗体购于r&d公司,cat.no.af3888
4.1将hepg2细胞按照40,000个细胞/孔的密度种于96孔透明细胞培养板中,37度co2细胞培养箱中培养过夜。
4.2第二天,弃去hepg2培养基更换为含有10%脱脂血清的培养基,继续培养18小时。
4.3第三天,
(1)配置终浓度为100μm,50μm,20μm和10μm的化合物,使其最终dmso含量为0.5%。终浓度为50μg/ml和25μg/ml的pcsk9抗体最为阳性对照。
(2)将化合物或抗体与25μg/ml的pcsk9蛋白于4度冰箱中预孵育1小时;
(3)取出细胞,弃去培养基,用100μl的分析缓冲液assaybuffer洗涤细胞3次;
(4)将用含10%脱脂血清培养基配制的f-ldl(70μg/ml)、不同浓度的化合物或抗体和pcsk9蛋白的混合物加入细胞中,37度co2培养箱中孵育6小时。这里的f-ldl,是指进行过荧光标记后的ldl。
(5)用100μlassaybuffer洗涤4次。
(6)tecan酶标仪测荧光值,ex/em=540/575nm;
(7)将终浓度为1μg/mldapi,0.1%tritionx100加入到细胞中,孵育15分钟;
(8)用酶标仪读取荧光,ex/em=364/454nm;
(9)分析数据。
实验结果
如图4所示,化合物viva2956在100μm和50μm有大约30%左右的抑制作用,在20μm和10μm浓度下无抑制作用。
如图5所示,pcsk9抗体在50μg/ml的浓度下接近100%抑制,在25μg/ml浓度作用下有50%左右的抑制作用。
由于本发明的苄撑巴比妥类pcsk9拮抗剂属于小分子物质,因此能够通过化学合成的方法制备,与大分子的拮抗剂相比,便于进行大规模生产,降低成本。
- 还没有人留言评论。精彩留言会获得点赞!