抗人PD‑1的单克隆抗体及其制备方法和应用与流程
本发明涉及生物医药和诊疗领域,具体涉及一种抗人PD-1的单克隆抗体及其制备方法和应用。
背景技术:
程序性细胞死亡因子(programmed cell death 1,PD-1)是一种共刺激分子,属于CD28/CTLA4家族。PD-1通过与程序性细胞死亡因子配体1或者2(programmed cell death ligand 1 or 2,PD-L1或PD-L2)结合后,招募并激活蛋白络氨酸磷酸酶等激活信号通路,对T细胞免疫起到负相调节的功能。PD-1还可以通过抑制辅助性T细胞间接影响体液免疫或者直接通过与B细胞上的PD-L结合影响抗体分泌。PD-1/PD-L1信号异常可以引起体内免疫微循环失去稳态,导致自身免疫性疾病或者肿瘤发生。
商品化抗PD-1单克隆抗体功能也比较单一,或只能做免疫印迹实验,或只能做免疫组化、流式等实验,浪费人力物力和时间,不利于开展科研实验和临床试验。比如Abacamanti-PD1 antibody(ab36151)用于ELISA与WB,而常见地,Abacam anti-PD1 antibody【J43】(ab95791)用于Flow Cyt。
抗原的表位分为线性表位和空间表位,免疫印迹(western blot)检测的是抗原的线性表位,而免疫组化检测的有可能是线性表位也有可能是空间表位,这两个实验往往需要购买和使用多种单克隆抗体。
本发明旨在提供一种既可以靶向结合人的PD-1蛋白也同时能够作为ELISA、Westernblot、免疫组化等应用的PD-1单克隆抗体,大大节约科研的成本和时间。
技术实现要素:
第一方面,本发明提供了一种抗人PD-1的单克隆抗体,所述抗人PD-1的单克隆抗体具有的特异性抗原结合结构域,既可以靶向结合人的PD-1蛋白也可以同时能够用于ELISA、Westernblot、免疫组化等实验。
本发明的示例性抗人PD-1的单克隆抗体列于文中的表1和表2。本发明提供的抗人PD-1的单克隆抗体包括重链可变区(HCVR)和轻链可变区(LCVR))。表1列出了本发明提供的抗人PD-1的单克隆抗体的HCVR、LCVR的氨基酸序列,及其在序列表中的序列号。表2列出了编码本发明所述的HCVR、LCVR氨基酸序列对应的核苷酸序列,及其在序列表中的序列号。
本发明提供的抗人PD-1的单克隆抗体的氨基酸序列包括:至少一条HCVR氨基酸序列、至少一条LCVR氨基酸序列;具体HCVR和LCVR优选为任一选自表1的氨基酸序列。
编码本发明提供的抗人PD-1的单克隆抗体的核苷酸序列包括:至少一条HCVR核苷酸序列、至少一条LCVR核苷酸序列;具体HCVR和LCVR优选为任一选自表2的核苷酸序列。
表1 序列表中的氨基酸序列
在本发明一实施例中,抗人PD-1的单克隆抗体2D1-1是经过筛选出的最佳效果的抗人PD-1的单克隆抗体。
在本发明一些实施例中,表1各序列具体为:
SEQUENCE NO.1(2D1.HCVR)的氨基酸序列为(三处下划线处的序列先后依次为CDR1、CDR2、CDR3):QVQLQQSGDDLVKPGASVKLSCKASGYTFTSYWINWIKQRPGQGLEWIGRIAPGSGSTYYNEMFKGKATLTVDTSSSTAYIQLSSLSSEDS AVYFCARLGQYYAMDYWGQGTTLTVSS;
SEQUENCE NO.2(2D1.LCVR)的氨基酸序列为(三处下划线处的序列先后依次为CDR1、CDR2、CDR3):DIVMTQTPLSLPVSLGDQASISCRSSQSLVHSNGNTYLHWYLQKPGQSPKLLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDLGVY FCSQSTHVPYTFGGGTKLELKR。
表2 序列表中的核苷酸序列
在本发明一些实施例中,表2各序列具体为:
SEQUENCE NO.3(2D1.HCVR)的核苷酸序列为(三处下划线处的序列先后依次为CDR1、CDR2、CDR3):CAGGTTCAGCTTCAGCAGTCTGGAGATGATCTGGTAAAGCCTGGGGCCTCAGTGAAGCTGTCCTGCAAGGCTTCTGGCTACACCTTCACCAGCTACTGGATTAACTGGATAAAACAGAGGCCTGGACAGGGCCTTGAGTGGATAGGACGTATTGCTCCTGGAAGTGGTAGTACATACTACAA TGAAATGTTCAAGGGCAAGGCAACACTGACCGTAGACACATCCTCCAGCACAGCCTACATTCAGCTCAGCAGCCTGTCATCTGAGGACTCTGCTGTCTATTTCTGTGCAAGACTGGGACAATACTATGCTATGGATTATTGGGGTCAAGGCACCACTCTCACAGTCTCCTCA;
SEQUENCE NO.4(2D1.LCVR)的核苷酸序列为(三处下划线处的序列先后依次为CDR1、CDR2、CDR3):GACATTGTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAGCCTTGTACACAGTAATGGAAACACCTATTTACATTGGTACCTGCAGAAGCCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTC TGGGGTCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGAGGCTGAGGATCTGGGAGTTTAT TTCTGCTCTCAAAGTACACATGTTCCGTACACGTTCGGAGGGGGGACCAAGCTGGAGCTGAAACGG;
具体地,SEQUENCE NO.3-4分别对应编码SEQUENCE NO.1-2的氨基酸序列。
鉴于序列同源性,本领域技术人员可以理解的是,如下实施方案应纳入本发明保护范围:
在本发明一些实施例中,所述的HCVR为与表1中所示任一HCVR氨基酸序列具有至少90%、至少95%、至少98%或至少99%同源性的氨基酸序列。
在本发明一些实施例中,所述的LCVR为与表1中所示任一LCVR氨基酸序列具有至少90%、至少95%、至少98%或至少99%同源性的氨基酸序列。
在本发明一些实施例中,所述的编码HCVR的序列为与表2中所示任一HCVR核苷酸序列具有至少90%、至少95%、至少98%或至少99%同源性的核苷酸序列。
在本发明一些实施例中,所述的编码LCVR的序列为与表2中所示任一LCVR核苷酸序列具有至少90%、至少95%、至少98%或至少99%同源性的核苷酸序列。
可以理解的,由于“核苷酸序列”具有碱基简并、突变等情况,行业内普通技术人员可调整某些碱基的种类,所述的碱基变化虽然导致了密码子的变化,但不会引起密码子翻译的氨基酸的变化,很常见的,亮氨酸的密码子就具有多种密码子,比如:UUA、UUG、CUU。
在本发明一个实施例中,HCVR(VH)和LCVR(VL)之间还连接有连接肽,连接肽的氨基酸序列为(GGGGS)n(n=1-4)、(GGS)4或(Gly)n(n=6-8),但不限于此。该连接肽主要采用了以甘氨酸和丝氨酸为主构成的多肽序列,其中,甘氨酸是分子量最小、侧链最短的氨基酸,可增加侧链的柔韧性;丝氨酸是亲水性最强的氨基酸,可增加肽链的亲水性。
在本发明一些实施例中,所述抗人PD-1的单克隆抗体的N段具有免疫球蛋白κ链信号肽的氨基酸序列。
本发明提供的所述抗人PD-1的单克隆抗体的N端加上了免疫球蛋白轻链κ链的分泌信号肽,从而保证抗体的表达并分泌到宿主细胞外。
第二方面,本发明还提供了一种如第一方面所述的抗人PD-1的单克隆抗体的制备方法,该方法包括:将第一方面所述的抗人PD-1的单克隆抗体的核苷酸序列用于构建表达所述的抗人PD-1的单克隆抗体的重组表达载体;导入宿主细胞;在表达条件下,培养宿主细胞,表达,分离纯化,获得所述抗人PD-1的单克隆抗体。
第三方面,本发明还提供了如第一方面所述的抗人PD-1的单克隆抗体按下述一种或多种方法进行应用:
(1)将所述抗人PD-1的单克隆抗体单独进行应用;
(2)将所述抗人PD-1的单克隆抗体与化疗、放疗、手术、生物治疗、免疫治疗中的一种或几种联合应用。
在本发明一些实施例中,应用(1)中,采用体内投递的方式将所述抗人PD-1的单克隆抗体直接投递到患者体内进行治疗。
在本发明一些实施例中,应用(1)中,先通过体外转染技术将所述抗人PD-1的单克隆抗体与免疫效应细胞混合,然后将所述混有抗人PD-1的单克隆抗体的免疫效应细胞输回患者体内实施治疗。
在本发明一些实施例中,应用(1)或(2)中,向患者施用如上抗人PD-1的单克隆抗体或含抗人PD-1的单克隆抗体的药物组合物,可向患者施用多于一次。
在本发明一些实施例中,应用(1)或(2)中,所述的投递的方式为靶向投递,包括但不限于采用可靶向投递的liposome脂质体(或其多聚体)等行业常用载体进行投递。
通过向包括人的哺乳动物施用本发明第一方面提供的抗体或第四方面提供的药物组合物,可预防或治疗肿瘤或其他PD-1的相关疾病,比如PD-1表达异常或紊乱相关的疾病。
第四方面,本发明提供了一种药物组合物,包括至少一种如第一方面所述的抗人PD-1的单克隆抗体,及可药用的载剂、赋形剂或稀释剂。
本发明提供的药物组合物可根据常规方法制成药物制剂。制剂过程中,优选将抗体与载体混合或用载体稀释,或装入容器形式的载体中。当载体作为稀释剂时,其可以为固体、半固体或液体,用作用于抗体的囊泡、赋形剂或培养基。因此,制剂可以是片剂、丸剂、粉剂、袋装剂、胶囊、酏剂、混悬剂、乳剂、溶液剂、糖浆剂、气溶胶、软和硬明胶胶囊、注射用无菌溶液、无菌粉剂等形式。合适的载体、赋形剂或稀释剂的实例包括乳糖、葡萄糖、蔗糖、山梨醇、甘露醇、硅酸钙、纤维素、甲基纤维素、微晶纤维素、聚乙烯吡咯烷酮、水、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石粉、硬脂酸镁和矿物油。制剂还可以包括填充剂、抗凝血剂、润滑剂、润湿剂、调味剂、乳化剂、防腐剂等。
第五方面,本发明提供了一种诊断试剂,包括至少一种如第一方面所述的抗人PD-1的单克隆抗体,及诊断剂,所述的诊断剂包括但不限于荧光团、发色团、染料、放射性同位素、化学发光分子、顺磁性离子或自旋捕获试剂。
第六方面,本发明提供了一种如第一方面所述的抗人PD-1的单克隆抗体在ELISA、Western blot、免疫组化检测PD-1抗原中的应用。
第七方面,本发明提供了一种核酸分子,编码如第一方面所述的抗人PD-1的单克隆抗体的氨基酸序列;在某些实施方式中,所述的核酸分子编码的氨基酸序列,为与如第一方面所述抗人PD-1的单克隆抗体的氨基酸序列具有至少90%、至少95%、至少98%或至少99%同源性的氨基酸序列。
第八方面,本发明提供了一种表达如第一方面所述的抗人PD-1的单克隆抗体的重组载体;在某些实施方式中,所述的重组载体具有本发明第七方面提供的任一核酸分子序列。
在本发明一些实施例中,所述的载体为质粒载体。具体地,所述重组载体是在空质粒的多克隆位点中插入本发明第七方面提供的任一核酸分子序列获得,具体插入方法可采用常规的基因克隆,也可采用无缝克隆(Seamless cloning)。
在本发明一些实施例中,所述的重组载体还包含表达目的多肽(本发明中为抗人PD-1的单克隆抗体)所需的所有必要元件的基因表达系统,通常其包括以下元件:启动子、编码多肽的基因序列,终止子;此外还可选择性包括信号肽编码序列等;这些元件是操作性相连的。
如本文所用,所述的“可操作地连接”是指两个或多个核酸区域或核酸序列的功能性的空间排列。例如:启动子区被置于相对于目的基因核酸序列的特定位置,使得核酸序列的转录受到该启动子区域的引导,从而,启动子区域被“可操作地连接”到该核酸序列上。优选地,所述信号肽为免疫球蛋白κ链信号肽。优选地,所述标签为His标签、GST标签、c-myc标签和Flag标签中的至少一种。以上的信号肽和标签种类为本发明人的优选方式,本领域技术人员可以根据具体需要选择合适的信号肽和标签。
第九方面,本发明提供了一种具有如第八方面所述载体的宿主细胞(优选为真核细胞或包括人在内的哺乳动物细胞);还提供了将如第八方面所述载体导入宿主细胞中的方法;还提供了通过在允许产生抗体的条件下培养具有所述载体的宿主细胞,并分离力所产生的抗体的方法。
第十方面,本发明提供了一种检测试剂盒,包括固体检测支持物,所述的固体检测支持物包含至少一种如第一方面所述的抗人PD-1的单克隆抗体。在一些实施方式中,所述固体支持物是可连接大分子如抗体、蛋白质、多肽、肽、多核苷酸的固体表面,如磁性珠、胶乳珠、微量滴定板孔、玻璃平板、尼龙、琼脂糖、聚丙烯酰胺、二氧化硅颗粒、硝酸纤维素膜等。
第十一方面,本发明提供了一种在待测样品中检测异常细胞的方法,其包括使所述样品与至少一种如第一方面所述的抗人PD-1的单克隆抗体相接触。在一些实施方式中,所述的样品来自经切除的肿瘤床。
如本发明所述,“异常细胞”是具有对于该细胞类型为非典型特征(包括非典型生长、非典型位置处的典型生长或针对非典型靶标的典型作用)的任何细胞。这样的细胞包括癌细胞、良性增生细胞或发育异常细胞或炎性细胞。
在本发明一些实施例中,采用如第十一方面所述的方法对移植前捐赠的组织或器官进行筛选,以提供基本不含PD-1的组织或器官。
在本发明一些实施例中,采用如第十一方面所述的方法对血液供给品进行筛选,以提供基本不含PD-1的血液供给品。
第十二方面,如第一方面所述的抗人PD-1的单克隆抗体或如第八方面所述的重组载体在制备诊断、预防、治疗PD-1相关疾病的试剂或药物中的应用。
如本发明所述的,所述的“PD-1疾病”包括但不限于PD-1表达异常或紊乱相关疾病,比如,PD-1抗原阳性的肿瘤或癌症。
商品化抗PD-1单克隆抗体功能也比较单一,或只能做免疫印迹实验,或只能做免疫组化、流式等实验,浪费人力物力和时间,不利于开展科研实验和临床试验。
本发明提供的抗人和鼠的PD-1单克隆抗体既可以靶向结合人的PD-1蛋白也能够作为ELISA、Western blot、免疫组化等科研试剂,应用性极强。
附图说明
图1为本发明实施例1提供的单克隆抗体的制备方法流程图;
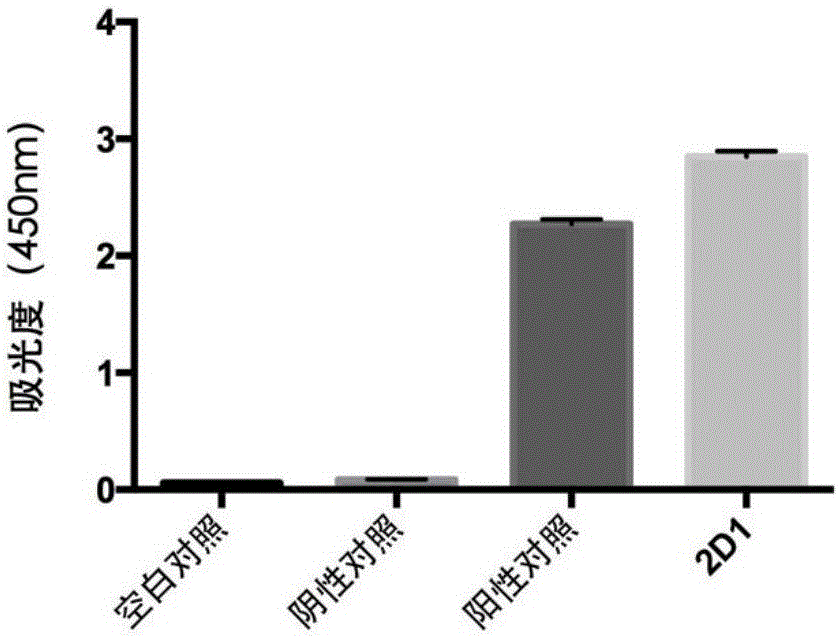
图2为本发明实施例1提供的间接ELISA测定抗血清效价结果;
图3为本发明实施例2提供的Western Blot检测PD-1抗体与PD-1的结合的结果;
图4为本发明实施例3提供的PD-1单抗与细胞表面的PD-1分子结合的流式检测结果;
图5本发明实施例4提供的PD-1蛋白与对应抗体的相互作用分析流程示意;
图6本发明实施例4提供的PD-1蛋白与对应抗体的相互作用分析实验条件优化后的实验结果。
具体实施方式
以下所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
本发明实施例中无特别说明外,所用试剂及耗材均为市售商品。
实施例1 单克隆抗体的制备
本发明实施例1提供的单克隆抗体的制备方法流程图如图1所示。
结合图1,本发明实施例1提供了一种单克隆抗体的制备方法,包括以下步骤:
(1)动物免疫
1)每只老鼠标记后,断尾取血约20ul,-20度保存作为免疫前对照。
2)以本发明PD-1抗原(2ug/ul)为免疫抗原免疫Balb/c小鼠,100μg/kg体重,共注射六只。首免时将免疫原与等量的弗氏完全佐剂混合制成乳化剂,颈背部皮下多点注射,每个注射点注射30-50ul左右混有佐剂的抗原,每只小鼠注射6-8个点为宜;
间隔1周进行二免和三免,方法剂量同一免;
取相同剂量免疫原加等量弗氏不完全佐剂混合乳化,继续四免、方法剂量同一免,四免一周后尾部采血检测血清效价及抑制,待检测符合要求时腹腔冲击免疫一次,3天后取脾细胞。
(2)细胞融合和克隆化
取免疫Balb/c小鼠脾细胞,按5:1比例与SP2/0骨髓瘤细胞融合,采用间接竞争ELISA测定细胞上清液,筛选阳性孔。利用有限稀释法对阳性孔进行克隆化,直到得到稳定分泌单克隆抗体的杂交瘤细胞株。
(3)细胞冻存和复苏
取处于对数生长期的杂交瘤细胞用冻存液制成5×l06个/ml的细胞悬液,分装于冻存管,在液氮中长期保存。复苏时取出冻存管,立即放入37℃水浴中速融,离心去除冻存液后,移入培养瓶内培养。
(4)单克隆抗体的制备与纯化
采用体内诱生法,将8周龄的Balb/c小鼠腹腔注入弗氏不完全佐剂0.5ml/只,7天后腹腔注射杂交瘤细胞5×l06个/只,7天后采集腹水。用亲和层析柱进行腹水纯化,获得PD-1抗原的2D1株单克隆抗体,紫外分光光度计测定蛋白浓度,-20℃保存备用。
间接ELISA测定抗血清效价。以包被抗原的最佳浓度包板,阳性血清及阴性血清(作为阴性对照)从1:4000起倍比稀释,同时以PBS作空白对照:
试剂:包被缓冲液(pH9.6,0.05M碳酸盐缓冲液),0.015M,pH7.4的PBS-T洗涤缓冲液,封闭液,终止液。
⑴包被:将抗原用包被缓冲液作系列稀释25ng/well,每个板孔加入100μL,37℃孵育3h,甩净孔内液体,PBS-T洗涤三次;
⑵封闭:每孔加入200μL 5%的脱脂奶粉,37℃孵育1h,甩净孔内液体,PBS-T洗涤三次;
⑶孵育一抗:每孔加入100μL细胞培养上清,37℃孵育1h,甩净孔内液体,PBS-T洗涤三次;
⑷孵育二抗:每孔加入100μL稀释度为1:8000的羊抗鼠IgG-HRP二抗,37℃孵育30min,甩净孔内液体,PBS-T洗涤五次;
⑸显色:每孔加入100μL TMB底物,避光反应10min;
⑹终止:每孔加入50μL 2mol/L硫酸;
⑺酶标仪测定OD450。
结果如图2所示。由图2可知,本发明实施例制备的2D1株单克隆抗体表现出较高的特异性和灵敏性。
实施例2 Western Blot检测PD-1抗体与PD-1的结合
本发明实施例2提供了一种Western Blot检测PD-1的2D1株单克隆抗体与PD-1的结合的方法,包括:
试剂:HRP标记山羊抗小鼠lgG(H+L),PD-1免疫血清,实施例1制备的2D1单克隆抗体。
1)12%分离胶,3%浓缩胶配制。
2)样本预处理:40ul样本+10ul上样缓冲液混合均匀,100℃热处理5min上样;上样顺序:蛋白预染marker,PD-1;电泳的条件:首先跑浓缩胶,80V,30min,然后分离胶,120V,50min,直至染料离底部1cm处停止电泳。
3)转膜,转膜条件:电泳条件为100V,4℃,90min。
4)封闭,适量5%脱脂奶粉加入膜中,室温摇床孵育1h。
5)一抗孵育:抗PD-1鼠单克隆抗体,稀释度1:8000,37℃孵育1h。PBST洗5次,每次5min。
6)二抗孵育:HRP标记山羊抗小鼠lgG(H+L),稀释度1:8000,室温摇床孵育30min。PBST洗5次,每次5min。
7)曝光:在暗室中向膜上加入曝光底物,于暗盒中曝光,然后将胶片放入显影液中显影5min,再在定影液中漂洗几次晾干即可。结果如图3所示,由图3可知,本发明实施例制备的P-2D1单克隆抗体可与PD-1高效结合,其中,PC为PD-1小鼠免疫血清,2D1为实施例1制备的2D1单克隆抗体。
实施例3 流式检测2D1单克隆抗体与细胞表面的PD-1分子的结合
本发明实施例3提供了一种流式检测实施例1筛选的PD-1单抗与转染了PD-1基因的293T细胞表面的PD-1分子的结合的方法,包括:
试剂:同型对照IgG,PE-抗鼠IgG二抗
实验步骤:
1.收集293T细胞细胞,确定细胞总数。
2.用冰冷PBS(3%FBS)重悬细胞成约1-5x106个细胞每毫升。
3.每管加入100uL的细胞悬液。
4.加入0.1-10ug/ml的一抗(2D1杂交瘤细胞株上清,含有本发明实所述的2D1单抗),4度避光孵育30min;设置对照组,等比例加入阴性血清。
5.400g离心5min并用冰冷PBS(3%FBS)重悬细胞。
6.用PBS(3%FBS)稀释二抗至最佳浓度,并重悬细胞,4度避光孵育30min。
7.洗涤细胞三次,每次400g离心5min并用冰冷PBS(3%FBS)重悬细胞。
8.将细胞悬液立即放于4度避光保存,流式分析。结果如图4所示,曲线-1、2分别为PD-1 2D1单抗、对照组的结果,由图4可知,本发明实施例提供的PD-1 2D1单抗与293T细胞细胞表面的PD-1分子的靶向结合效率较高。
实施例4 验证PD-1蛋白与对应抗体的相互作用
本发明实施例5采用Bio-rad公司ProteOn XPR36相互作用平行分析系统对实施例1所筛选的PD-1单抗与对应抗体的相互作用进行检测,并获得亲和力,包括:
芯片修饰:传感芯片表面用50mM NaOH和8mM CHAPS分别在横向和纵向两个方向冲洗两遍,然后纵向连续注入3针PBS,流速设为100μl/min。
通道用0.05M sulfo-NHS和0.02M EDAC活化,条件为30μl/min,6分钟。将5μl Undecylamine(十一胺)和495l DMSO(二甲基亚砜)混合后用pH 5.0的醋酸钠溶液稀释20倍。混合液用移液器吹打混匀,直至澄清。Undecylamine(0.05%v/v)以30μl/min,注入到通道,持续6分钟。最后将通道用1M盐酸乙醇胺去活化,条件是30μl/min,6分钟。随后芯片表面用50mM NaOH纵向流过芯片以稳定基线。
A蛋白(100μg)按照已有文献的描述的制备成终浓度22μM的PBS溶液。芯片表面用PBS以100μl/min横向注入30秒冲洗。冲洗3-4次后A蛋白以100μl/min横向注入,结合1分钟,解离10分钟。测定动力学数据时,A蛋白以一系列浓度(300、150、75、37.5、18.75nM)注入通道,仅留一个通道注入缓冲液。
将抗体偶联到L6通道,以interspot作为阴性参照位点(图5种的箭头所指处)。以浓度梯度(300、150、75、37.5、18.75nM)和缓冲液作为参照,横向流过抗体。示意图如图5所示:
检测结果:
1:条件优化结果
每个相互作用都需要优化实验条件,以获得最优的实验条件。针对本次实验,按照试剂盒操作,优化以下条件:
pH值选择、偶联浓度选择。根据优化结果(反应过程中抗原抗体的响应值)发现:pH4.5最符合本次实验,偶联抗体浓度为20ug。
2:抗体偶联结果(包括活化、固定和封闭三个过程,按照试剂盒操作,评估反应过程中抗原抗体的响应值)显示,抗体偶联量最优为:1600RU。
3:蛋白与抗体相互作用检测结果:
经过抗原浓度优化与实验条件优化后测得:
实验条件优化:将流速调整为:75ul/min,相互作用时间调整为220sec,抗原起始浓度为150nM,解离时间仍为600sec,再生条件:0.85%磷酸。
实验条件优化后实验结果如图6所示:
通过软件扣除阴性对照interspot信号值,再扣除空白参照缓冲液的信号值,拟合后实验结果为:抗原与抗体的亲和力KD=1.34E-10。
图6中,横坐标为反应时间,纵坐标为反应过程中抗原抗体的响应值。ka:2.20E+05 1/Ms kd:2.94E-051/s KD:1.34E-10M,各曲线由上至下依次对应L6A1、L6A2、L6A3、L6A4、L6A5、L6A6,其中抗体偶联到L6通道,L6A1-L6A6分别对应L6通道第1到6行。
实验所得PD-1抗体具有高亲和力,同时能用于ELISA、Western Blot、免疫组化等科研使用。
实施例5 可变区核苷酸检测
本发明实施例5对实施例1所筛选的PD-1单抗的可变区核苷酸进行检测,包括:
1.总RNA的提取
1)培养2D1细胞至铺满瓶底的80%~90%时,收集5*106个细胞到1.5ml离心管,2000xg,离心5min,弃上清。
2)按每管加入1ml Trizol,反复吹打细胞,室温放置5min。
3)每管加入200ul氯仿,剧烈震荡15s,室温放置3min。
4)10000xg,4度离心15min,此时样品分为三层,无色水相,中间层和有机相。转移无色水相于新的1.5ml离心管,加入500ul异丙醇,室温放置10min。
5)10000xg,4度离心10min,弃上清,加入1ml 75%的乙醇,并剧烈涡旋。
6)7500xg,4度离心5min,弃上清,室温晾干沉淀5min左右。
7)用DEPC水溶解RNA,55℃~60℃水浴中孵育10min。
2.单链cDNA的合成
将RNA反转录成cDNA,反应分两步进行
1)在PCR管中,RNA 10ul,RNA水21ul,用枪头反复吹打均匀,70度保温5min,之后立即冰上放置,防止RNA复性。
2)以上体系中加入以下试剂,反应体系如下:
表1 RT-PCR反应体系
3.PCR扩增VH、VL
1)根据鼠抗体轻链重链可变区第一骨架区和J段序列,分别设计扩增重链可变区引物(FH:gAggTgMWgcTKVWgSAgTcTggA,RH:gAcDgTgASHRDRgTBccTKSRccccA)和轻链可变区引物(FL:gAHRTYgTKMTSAcMcARWcTMcA,RL:KATYTccARYYTKgTSccHBcDccgAA),取cDNA扩增VH和VL基因。
表2 VH-PCR反应体系
表3 VL-PCR反应体系
PCR扩增程序:94℃预变性5min,(94℃变性50s,52℃复性35s,72°延伸50s,30cycles),72℃延伸5min。4℃保留。
2)1.2%琼脂糖凝胶电泳鉴定、送测序公司测
琼脂糖凝胶电泳鉴定,电泳纯化产物送测序公司测序。获得2D1单克隆抗体重链可变区核苷酸序列及2D1单克隆抗体轻链可变区核苷酸序列。
具体地,2D1单克隆抗体重链(2D1.HCVR)可变区核苷酸序列如下SEQUENCE NO.3所示(三处下划线处的序列先后依次为CDR1、CDR2、CDR3):
CAGGTTCAGCTTCAGCAGTCTGGAGATGATCTGGTAAAGCCTGGGGCCTCAGTGAAGCTGTCCTGCAAGGCTTCTGGCTACACCTTCACCAGCTACTGGATTAACTGGATAAAACAGAGGCCTGGACAGGGCCTTGAGTGGATAGGACGTATTGCTCCTGGAAGTGGTAGTACATACTACAATGAAATGTTCAAGGGCAAGGCAACACTGACCGTAGACACATCCTCCAGCACAGCCTACATTCAGCTCAGCAGCCTGTCATCTGAGGACTCTGCTGTCTATTTCTGTGCAAGACTGGGACAATACTATGCTATGGATTATTGGGGTCAAGGCACCACTCTCACAGTCTCCTCA;
具体地,2D1单克隆抗体轻链(2D1.LCVR)可变区核苷酸序列如下SEQUENCE NO.4所示(三处下划线处的序列先后依次为CDR1、CDR2、CDR3):
GACATTGTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAGCCTTGTACACAGTAATGGAAACACCTATTTACATTGGTACCTGCAGAAGCCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGGTCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGAGGCTGAGGATCTGGGAGTTTATTTCTGCTCTCAAAGTACACATGTTCCGTACACGTTCGGAGGGGGGACCAAGCTGGAGCTGAAACGG。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
SEQUENCE LISTING
<110> 中国科学院深圳先进技术研究院
<120> 抗人PD-1的单克隆抗体及其制备方法和应用
<130> 2016
<160> 4
<170> PatentIn version 3.3
<210> 1
<211> 118
<212> PRT
<213> 人工序列
<400> 1
Gln Val Gln Leu Gln Gln Ser Gly Asp Asp Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Asn Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Ala Pro Gly Ser Gly Ser Thr Tyr Tyr Asn Glu Met Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Ile Gln Leu Ser Ser Leu Ser Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Leu Gly Gln Tyr Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 2
<211> 113
<212> PRT
<213> 人工序列
<400> 2
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys
100 105 110
Arg
<210> 3
<211> 354
<212> DNA
<213> 人工序列
<400> 3
caggttcagc ttcagcagtc tggagatgat ctggtaaagc ctggggcctc agtgaagctg 60
tcctgcaagg cttctggcta caccttcacc agctactgga ttaactggat aaaacagagg 120
cctggacagg gccttgagtg gataggacgt attgctcctg gaagtggtag tacatactac 180
aatgaaatgt tcaagggcaa ggcaacactg accgtagaca catcctccag cacagcctac 240
attcagctca gcagcctgtc atctgaggac tctgctgtct atttctgtgc aagactggga 300
caatactatg ctatggatta ttggggtcaa ggcaccactc tcacagtctc ctca 354
<210> 4
<211> 339
<212> DNA
<213> 人工序列
<400> 4
gacattgtga tgacccaaac tccactctcc ctgcctgtca gtcttggaga tcaagcctcc 60
atctcttgca gatctagtca gagccttgta cacagtaatg gaaacaccta tttacattgg 120
tacctgcaga agccaggcca gtctccaaag ctcctgatct acaaagtttc caaccgattt 180
tctggggtcc cagacaggtt cagtggcagt ggatcaggga cagatttcac actcaagatc 240
agcagagtgg aggctgagga tctgggagtt tatttctgct ctcaaagtac acatgttccg 300
tacacgttcg gaggggggac caagctggag ctgaaacgg 339
- 还没有人留言评论。精彩留言会获得点赞!