新型多胺化合物及其制造方法,以及使用其的环氧树脂用固化剂、环氧树脂组合物和环氧树脂固化物与流程
本发明提供作为新型化合物的多胺化合物及其制造方法,还涉及含有新型多胺化合物的环氧树脂用固化剂、环氧树脂组合物和环氧树脂固化物。
背景技术:
多胺化合物作为环氧树脂用固化剂用途而广泛使用。
作为多胺化合物,已知有:二乙三胺、三乙四胺、聚氧丙烯二胺(注册商标:jeffamine)、异佛尔酮二胺、间苯二甲胺、1,3-双(氨甲基)环己烷等。它们在工业上被制造,市售了含有多胺化合物的环氧树脂用固化剂。
多胺化合物一般存在如下缺点:吸收大气中的二氧化碳气体、水分,容易形成氨基甲酸盐,在用作环氧树脂用固化剂时,在固化物的涂膜上产生白化现象、粘性。另外,多胺化合物具有挥发性,因此具有操作环境恶化的缺点。
所以,多胺化合物直接用作环氧树脂用固化剂的情况少,一般改性使用。作为代表性的改性方法,可列举出:通过与具有羧基的化合物的反应的改性、通过与环氧化合物的反应的改性、通过醛化合物与酚化合物的曼尼希反应的改性、通过与丙烯酸化合物的迈克尔加成反应的改性等。
例如通过醛化合物与酚化合物的曼尼希反应的改性中,在曼尼希反应产物中残存未反应的酚。由于酚化合物对环境不优选,因此有近年不使用酚的倾向加剧。
这些改性胺的性能本质上受到改性前的胺的特性左右,因此期望高性能的胺成分。
关于各种多胺的改性方法、其性能,已出版总说,且存在详细的记载(参照下述非专利文献1:“总说环氧树脂”环氧树脂技术协会:p123~p140(3.2.1多胺的种类和性质、3.2.2改性多胺的种类和性能)))。
现有技术文献
非专利文献
非专利文献1:总说环氧树脂(エポキシ樹脂技術協会:p123~p140(3.2.1ポリアミンの種類と性質、3.2.2変性ポリアミンの種類と性能)
技术实现要素:
发明要解决的问题
本发明提供前所未知的、作为环氧树脂用固化剂有用的新型的多胺化合物及其制造方法、以及使用其的环氧树脂用固化剂、环氧树脂组合物和环氧树脂固化物。
用于解决问题的方案
本发明人为了解决上述课题进行了深入研究,结果发现通过以下所示项目可以解决。
[1]一种多胺化合物,其如下述式(1)所示,
(式(1)中的r1、r2各自独立地为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基,n为1~2的整数。)
[2]根据[1]所述的多胺化合物,其中,前述式(1)的化合物为下述式(2)所示的化合物。
[3]根据[1]所述的多胺化合物,其中,前述式(1)的化合物为下述式(3)所示的化合物。
[4]根据[1]所述的多胺化合物,其中,前述式(1)的化合物为下述式(4)所示的化合物。
[5]根据[1]所述的多胺化合物,其中,前述式(1)的化合物为下述式(5)所示的化合物。
[6]根据[1]所述的多胺化合物,其中,前述式(1)的化合物为下述式(6)所示的化合物。
[7]一种多胺化合物的制造方法,其将下述式(7)所示的氨甲基环己烷化合物、和下述式(8)所示的苯二甲醛化合物进行脱水缩合后,进行氢化而生成下述式(1)所示的多胺化合物。
(式(7)中的r1为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基。n为1~2的整数。)
(式(8)中的r2为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基。)
(式(1)中的r1、r2各自独立地为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基,n为1~2的整数。)
[8]一种多胺化合物的制造方法,其将下述式(7)所示的氨甲基环己烷化合物、和下述式(9)所示的氨甲基苯化合物进行脱氨缩合,生成下述式(1)所示的多胺化合物。
(式(7)中的r1为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基。n为1~2的整数。)
(式(9)中的r2为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基。n为1~2的整数。)
(式(1)中的r1、r2各自独立地为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基,n为1~2的整数。)
[9]一种环氧树脂用固化剂,其包含[1]~[6]中任一项所述的多胺化合物。
[10]一种环氧树脂组合物,其包含[9]所述的环氧树脂用固化剂、和环氧树脂。
[11]一种环氧树脂固化物,其使[10]所述的环氧树脂组合物固化而成。
发明的效果
根据本发明,可以提供作为环氧树脂用固化剂有用的新型的多胺化合物及其制造方法、以及使用其的环氧树脂用固化剂、环氧树脂组合物和环氧树脂固化物。
附图说明
图1为式3的化合物的气相色谱
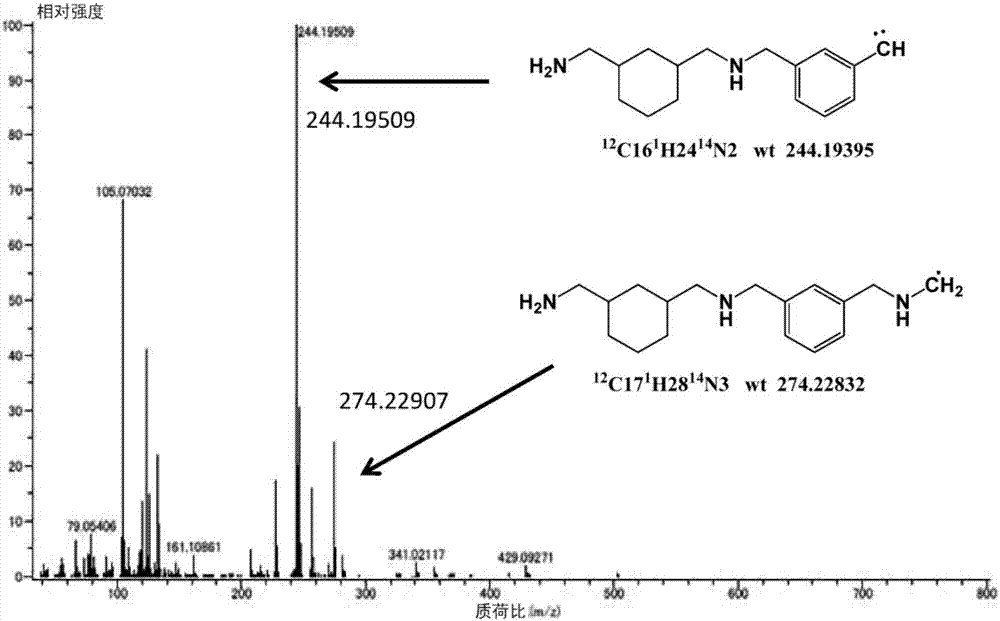
图2为式3的化合物的ei-ms分析结果
图3为式3的化合物的ir分析结果
图4为式3的化合物的1h-nmr分析结果
图5为式4的化合物的气相色谱
图6为式4的化合物的ei-ms分析结果
图7为式4的化合物的ir分析结果
图8为式4的化合物的1h-nmr分析结果
图9为式5的化合物的气相色谱
图10为式5的化合物的ei-ms分析结果
图11为式5的化合物的ir分析结果
图12为式5的化合物的1h-nmr分析结果
图13为式6的化合物的气相色谱
图14为式6的化合物的ei-ms分析结果
图15为式6的化合物的ir分析结果
图16为式6的化合物的1h-nmr分析结果
图17为式7的化合物的气相色谱
图18为式7的化合物的ei-ms分析结果
图19为式7的化合物的ir分析结果
图20为式7的化合物的1h-nmr分析结果
图21为1,3-双(氨甲基)环己烷的ir分析结果
图22为1,3-双(氨甲基)环己烷的1h-nmr分析结果
图23为1,4-双(氨甲基)环己烷的ir分析结果
图24为1,4-双(氨甲基)环己烷的1h-nmr分析结果
图25为间苯二甲胺的ir分析结果
图26为间苯二甲胺的1h-nmr分析结果
图27为对苯二甲胺的ir分析结果
图28为对苯二甲胺的1h-nmr分析结果
具体实施方式
《多胺化合物》
本发明的多胺化合物如式(1)所示。本发明的多胺化合物作为环氧树脂用固化剂有用,例如尤其可以无需改性地用作环氧树脂用固化剂。另外,使用本发明的多胺化合物的环氧树脂组合物可以得到良好的环氧树脂固化物的涂膜。
式(1)中的r1、r2各自独立地为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基、n为1~2的整数。键合在两个环己烷环的各(ch2nh2)的n可以相同也可以不同。
作为碳数1~10的烷基,例如可列举出:甲基、乙基;直链或支链的丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基;或,环状的环己基、环戊基、苯基、苄基等。
作为碳数1~10的烷氧基,例如可列举出:甲氧基、乙氧基;直链或支链的丙氧基、丁氧基;或,环状的苯氧基等。
作为卤素原子可列举出氟、氯、溴、碘等。
作为前述式(1)所示的化合物,进一步优选为下述式(2)所示的化合物。
作为前述式(2)所示的化合物,进一步优选为下述式(3)、下述式(4)、下述式(5)、下述式(6)所示的化合物。
(通过脱水缩合和氢化的制造方法)
前述式(1)所示的化合物可以将下述式(7)所示的氨甲基环己烷化合物、和下述式(8)所示的苯二甲醛化合物进行脱水缩合后,进行氢化而得到。
式(7)中的r1为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基。n为1~2的整数。式(7)中的r1与上述式(1)的r1同样,省略其说明。
前述式(8)中的r2为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基。式(8)中的r2与上述式(1)的r2同样,省略其说明。
作为前述式(7)所示的氨甲基环己烷化合物,优选为双(氨甲基)环己烷。尤其,进一步优选为1,3-双(氨甲基)环己烷、1,4-双(氨甲基)环己烷。
上述1,3-双(氨甲基)环己烷、1,4-双(氨甲基)环己烷可以用公知的方法合成。例如可以通过将间苯二甲胺、对苯二甲胺进行核氢化而容易地得到。另外,使用作为试剂销售的物质。
作为前述式(8)所示的苯二甲醛化合物,进一步优选为间苯二甲醛、对苯二甲醛。
关于式(7)所示的氨甲基环己烷化合物与式(8)所示的苯二甲醛化合物的反应,已知胺与醛是指,进行脱水缩合一般容易形成称作席夫碱的亚胺体。上述脱水缩合反应即使无催化剂也能容易地进行反应,也可以使用催化剂。作为催化剂,一般使用氧化铝这样的固体催化剂。
上述脱水缩合反应可以无溶剂地实施,还可以在溶剂存在下实施。使用溶剂时,只要是对胺和醛为非活性的溶剂就可以使用。作为前述溶剂,例如可以使用:二乙醚、四氢呋喃这样的醚溶剂、苯、甲苯、二甲苯这样的芳香族溶剂。
上述脱水缩合可以通过使反应生成的水去除到体系外来进行。作为去除水的方法,可以实施在苯等共沸溶剂的共存下进行共沸脱水的方法、减压下去除水的方法等。
通过上述脱水缩合得到的亚胺体可以分离,尤其也可以不分离地实施接下来的工序的氢化。
作为通过上述脱水缩合得到的亚胺体的氢化反应的催化剂,一般只要是具有氢还原活性的物质就可以使用。作为这样的催化剂,例如可以使用铂、钯、钌、铑这样的贵金属催化剂;镍、钴、铁催化剂这样的贱金属催化剂。这些催化剂可以单独使用金属、或者可以以负载在活性炭、氧化铝、二氧化硅、二氧化钛、氧化锆这样的载体的状态使用。这些之中,进一步优选使用负载有钯的催化剂。
亚胺体的氢化反应只要是氢气氛围,可以在常压条件、高压条件任意条件下实施。反应压力优选为0.5mpa~2mpa,进一步优选为0.5mpa~0.98mpa。反应压力越高反应速度越大。
亚胺体的氢化反应可以无溶剂地实施,也可以使用溶剂。使用溶剂时,只要是在氢化反应为非活性、或与胺化合物不反应的溶剂就可以任意使用。作为前述溶剂,例如可以使用:水、甲醇、乙醇、异丙醇这样的醇溶剂、二乙醚、四氢呋喃这样的醚溶剂、二甲基甲酰胺这样的酰胺溶剂、氨甲基环己烷化合物这样的胺溶剂。其中,进一步优选为水、醇溶剂、胺溶剂。
(通过脱氨缩合的制造方法)
前述式(1)所示的化合物也可以将式(7)所示的氨甲基环己烷化合物、和式(9)所示的氨甲基苯化合物进行脱氨缩合而得到。
前述式(7)中的r1为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基。n为1~2的整数。式(7)中的r1与上述式(1)的r1同样,省略其说明。
前述式(9)中的r2为选自氢、碳数1~10的烷基、碳数1~10的烷氧基、羟基、酰胺基、和卤素原子的取代基。n为1~2的整数。式(9)中的r2与上述式(1)的r2同样,省略其说明。
作为前述式(7)所示的氨甲基环己烷化合物,优选为双(氨甲基)环己烷。尤其进一步优选为1,3-双(氨甲基)环己烷、1,4-双(氨甲基)环己烷。
前述式(9)所示的化合物优选n=1,进一步优选为间苯二甲胺、对苯二甲胺。
作为上述脱氨反应的催化剂,一般可以使用具有氢还原活性的物质、强碱性化合物。作为具有氢还原活性的物质,例如可以使用铂、钯、钌、铑这样的贵金属催化剂、镍、钴、铁催化剂这样的贱金属催化剂。这些催化剂可以单独使用金属,或也可以以负载在活性炭、氧化铝、二氧化硅、二氧化钛、氧化锆这样的载体的状态使用。这些之中,优选使用负载有钯的催化剂。另外,作为强碱性化合物,例如可以使用氢化钠、氨基化钠、氨基化锂等,进一步优选为氨基化钠。
作为上述脱氨反应中的溶剂,只要是在该反应中为非活性的溶剂就可以任意使用。例如可以使用:二乙醚、四氢呋喃这样的醚溶剂、二甲基甲酰胺这样的酰胺溶剂、苯、甲苯、二甲苯这样的芳香族溶剂。另外,也可以不使用溶剂而使上述化合物直接反应。上述脱氨反应进一步优选不使用溶剂的方法。上述脱氨反应的温度优选在50~250℃的范围实施,进一步优选在100~200℃下实施。
《环氧树脂用固化剂》
前述式(1)所示的多胺化合物可以用作环氧树脂用固化剂(以下有时仅称“固化剂”。)。
将式(1)所示的多胺化合物用作固化剂时,可以并用有助于环氧树脂的固化的其它胺化合物。此时,相对于式(1)所示的多胺化合物和其它胺化合物的总量,式(1)所示的多胺化合物的量优选为20重量%以上。为了更进一步活用环氧树脂用固化剂的特征,相对于式(1)所示的多胺化合物和其它胺化合物的总量,式(1)所示的多胺化合物的量进一步优选为30重量%以上,进一步优选为50重量%以上。
使用式(1)所示的多胺化合物的本发明的环氧树脂用固化剂,在上述其它胺化合物的基础上,在无损本发明的効果的范围内,也可以包含对溶剂等的固化没有帮助的成分。
另外,将本发明的环氧树脂用固化剂用作后述环氧树脂组合物时,可以并用其它固化剂。
《环氧树脂组合物》
本发明的环氧树脂组合物包含环氧树脂和使用上述式(1)所示的多胺化合物的环氧树脂用固化剂。本发明的环氧树脂组合物使用的环氧树脂只要是本发明的环氧树脂用固化剂包含的、具有与来自氨基的活性氢反应的缩水甘油基的环氧树脂,就没有特别的限定,例如适宜使用以双酚a型环氧树脂、双酚f型环氧树脂、或它们的混合物作为主成分的物质。进一步,本发明的环氧树脂组合物中,可以根据用途使用填充剂、增塑剂等改性成分、反应性或非反应性的稀释剂、触变剂等流动调整成分、颜料、流平剂、赋粘剂等成分、凹陷抑制剂、流挂剂、流动剂、消泡剂、紫外线吸收剂、光稳定剂等添加剂。本发明的环氧树脂组合物中,环氧树脂与环氧树脂用固化剂的混合比,由环氧树脂的环氧当量计算的官能团数[ep]与由环氧树脂用固化剂的活性氢当量计算的官能团数[h]之比[ep/h]优选处于0.90~1.10的范围,进一步优选处于0.95~1.05的范围。配合比越接近等量残存官能团越少,可以得到优异性能的环氧树脂。
《环氧树脂固化物》
本发明的环氧树脂组合物可以使用公知的方法使其固化制成环氧树脂固化物。固化条件根据用途适宜选择,没有特别限定,例如本发明的环氧树脂组合物可以在15~30℃的常温条件下使用,也可以加热至30℃以上使其加热固化。
本发明的多胺化合物与以往使用的多胺化合物相比较,具有快速固化性。另外,使本发明的环氧树脂组合物固化得到干燥性、耐水性良好、并且外观也优秀的物质。
实施例
以下,示出实施例和比较例对本发明进行具体说明。但是,本发明不受这些实施例的制约。作为原料的间苯二甲醛、对苯二甲醛、间苯二甲胺、对苯二甲胺、1,3-双(氨甲基)环己烷(顺/反=74/26)为可以获得的试剂,1,4-双(氨甲基)环己烷(顺/反=60/40)使用现有技术(例如日本特开昭50-126638号公报),由对苯二甲胺进行合成。另外,用作催化剂的5%pd/c使用n.e.chemcatcorporation制造的催化剂。
(气相色谱)
将样品溶解于甲醇,使用安装有agilentinc.制造的柱(制品名:hp-1ms)的agilentinc.制造的气相色谱(制品名:gc-6850)进行分析。
(ms分析)
使用日本电子株式会社制造的飞行时间质谱仪(型号:jms-t100gcv),实施ei-ms分析。内标使用2,4,6-三(三氟甲基)-1,3,5-三嗪进行精密质量(日文:ミリマス)测定。
(ir分析)
使用thermofisherscientificinc.制造的ir分析装置(型号:nicolet6700),进行ir光谱的分析。作为参考试样,测定间苯二甲胺、对苯二甲胺、1,3-双(氨甲基)环己烷、1,4-双(氨甲基)环己烷,与这些结果(参照图21(1,3-双(氨甲基)环己烷)、图23(1,4-双(氨甲基)环己烷)、图25(间苯二甲胺)、图27(对苯二甲胺))相比较来进行各化合物的鉴定。
(1h-nmr分析)
使用日本电子株式会社制造的nmr装置(型号:jnm-eca500)实施1h-nmr分析。将样品溶解于重甲醇,标准使用四甲基硅烷(tms),以tms的化学位移为0ppm实施各光谱的解析。作为参考试样,测定间苯二甲胺、对苯二甲胺、1,3-双(氨甲基)环己烷、1,4-双(氨甲基)环己烷,与这些结果(参照图22(1,3-双(氨甲基)环己烷)、图24(1,4-双(氨甲基)环己烷)、图26(间苯二甲胺)、图28(对苯二甲胺))相比较来进行各化合物的鉴定。
(粘度测定)
使用东机产业公司制造的粘度计(型号:tve-25l),测定25℃下的粘度。
(涂膜干燥试验)
对于环氧树脂组合物,用以下方法进行涂膜干燥评价。
在玻璃板(25mm×300mm×2mm)上用76μm的涂膜器涂布环氧树脂,在23℃、50%rh的条件下使用rc型涂料干燥时间测定器(tp技研公司制造)测定涂膜的指触干燥(涂膜上形成针的痕迹的时间)、半干燥(针的痕迹不蹭到下层的玻璃板的时间)、完全干燥时间(针的痕迹完全消失的时间)。
(涂膜性的评价试验)
环氧树脂组合物用以下方法进行涂膜性的评价。
环氧树脂组合物在冷轧钢板(jisg3141、spcc-sb,70mm×150mm×0.8mm)上使用200μm的刮刀涂布,使其在23℃、50%rh的条件下固化。
-外观-
对于经过7天后的涂膜,对透明性、平滑性、光泽用目视按照以下基准判定为4阶段。
ex/优秀、g/良好、f/略微不良、p/不良
-涂膜干燥-
第1天、第4天、第7天的涂膜干燥性用指触按照以下基准判定为4阶段。
ex/无发粘、g/稍有发粘、f/略微发粘、p/发粘
(活性氢当量)
将分离的化合物假定为纯度100%,由以下式(a)算出胺化合物的活性氢当量。
式(a)…(由鉴定出的化学式算出的分子量)÷(活性氢数〔伯胺的官能团数×2+仲胺的官能团数〕)
[实施例1]
将1,3-双(氨甲基)环己烷60g溶解于苯50ml,加热至70℃。将间苯二甲醛6.7g溶解于苯100ml,花费30分钟滴加至1,3-双(氨甲基)环己烷的苯溶液。滴加后,加热至100℃,使用迪安-斯达克分水器装置花费1小时将水共沸脱水。冷却后,反应液转移至300ml的不锈钢制高压釜,添加5%pd/c(含水率54.1%)0.3g。高压釜用氢气升压至0.9mpa,在80℃下进行1小时反应。反应结束后,冷却并用加压过滤机去除催化剂,用蒸发器去除作为溶剂的苯。其后,通过蒸馏去除过量的1,3-双(氨甲基)环己烷,获得下述式(3)所示的脂环式多胺化合物17.2g。
对于得到的化合物,将气相色谱的结果示于图1,ms分析的结果示于图2,ir分析的结果示于图3,1h-nmr分析的结果示于图4。由气相色谱的结果,确认气相色谱纯度为96%,由ms分析、ir分析、1h-nmr分析的结果,确认得到的化合物为前述式(3)所示的脂环式多胺化合物。另外,得到的化合物的25℃的粘度为1856mpa·s、活性氢当量为64。
将上述得到的脂环式多胺化合物3.5g与双酚a型液态环氧树脂(三菱化学制造、jer828(注册商标)、环氧当量:186g/eq、以下简称“dgeba”)10g混合,制备环氧树脂组合物a(参照表1)。对于得到的环氧树脂组合物a,进行“涂膜干燥试验”、“环氧树脂涂膜性的评价试验”。结果示于表2。
[实施例2]
将“1,3-双(氨甲基)环己烷”设定为“1,4-双(氨甲基)环己烷”,除此以外,进行与实施例1同样的操作,获得下述式(4)所示的脂环式多胺化合物16.7g。
对于得到的化合物,将气相色谱的结果示于图5,ms分析的结果示于图6,ir分析的结果示于图7,1h-nmr分析的结果示于图8。由气相色谱的结果,确认气相色谱纯度为96%,由ms分析、ir分析、1h-nmr分析的结果,确认得到的化合物为前述式(4)所示的脂环式多胺化合物。另外,得到的化合物的25℃的粘度为2119mpa·s、活性氢当量为64。
将上述得到的脂环式多胺化合物3.5g与dgeba10g混合,制备环氧树脂组合物b(参照表1)。对于得到的环氧树脂组合物b,进行“涂膜干燥试验”、“环氧树脂涂膜性的评价试验”。结果示于表2。
[实施例3]
将1,3-双(氨甲基)环己烷60g溶解于苯50ml,加热至70℃。将对苯二甲醛6.7g溶解于苯200ml,花费30分钟滴加至1,3-双(氨甲基)环己烷的苯溶液。滴加后,加热至100℃,使用迪安-斯达克分水器装置花费1小时将水共沸脱水。共沸脱水后,通过蒸馏去除苯100ml。冷却后,反应液转移至300ml的不锈钢制高压釜,添加5%pd/c(含水率54.1%)0.3g。高压釜用氢气升压至0.9mpa,在80℃下进行1小时反应。反应结束后,冷却并用加压过滤机去除催化剂,用蒸发器去除作为溶剂的苯。其后,通过蒸馏去除过量的1,3-双(氨甲基)环己烷,取得下述式(5)所示的脂环式多胺化合物17.1g。
对于得到的化合物,将气相色谱的结果示于图9,ms分析的结果示于图10,ir分析的结果示于图11,1h-nmr分析的结果示于图12。由气相色谱的结果,确认气相色谱纯度为96%,由ms分析、ir分析、1h-nmr分析的结果,确认得到的化合物为前述式(5)所示的脂环式多胺化合物。另外,得到的化合物的25℃的粘度为2784mpa·s、活性氢当量为64。
将上述得到的脂环式多胺化合物3.5g与dgeba10g混合,制备环氧树脂组合物c(参照表1)。对于得到的环氧树脂组合物c,进行“涂膜干燥试验”、“环氧树脂涂膜性的评价试验”。结果示于表2。
[实施例4]
将“1,3-双(氨甲基)环己烷”设定为“1,4-双(氨甲基)环己烷”,除此以外,进行与实施例3同样的操作,获得下述式(6)所示的脂环式多胺化合物17.3g。
将得到的化合物的气相色谱的结果示于图13,ms分析的结果示于图14,ir分析的结果示于图15,1h-nmr分析的结果示于图16。由气相色谱的结果,确认气相色谱纯度为94%,由ms分析、ir分析、1h-nmr分析的结果,确认得到的化合物为前述式(6)所示的脂环式多胺化合物。另外,得到的化合物的25℃的粘度为2343mpa·s、活性氢当量为64。
将上述得到的脂环式多胺化合物3.5g与dgeba10g混合,制备环氧树脂组合物d(参照表1)。对得到的环氧树脂组合物d进行“涂膜干燥试验”、“环氧树脂涂膜性的评价试验”。结果示于表2。
[实施例5]
将1,3-双(氨甲基)环己烷30g和1,4-双(氨甲基)环己烷30g溶解于苯50ml,加热至70℃。将间苯二甲醛3.35g和对苯二甲醛3.35g溶解于苯100ml,花费30分钟滴加至1,3-双(氨甲基)环己烷和1,4-双(氨甲基)环己烷的苯溶液。滴加后,加热至100℃,使用迪安-斯达克分水器装置花费1小时将水共沸脱水。冷却后,反应液转移至300ml的不锈钢制高压釜,添加5%pd/c(含水率54.1%)0.3g。高压釜用氢气升压至0.9mpa,在80℃下进行1小时反应。反应结束后,冷却并用加压过滤机去除催化剂,用蒸发器去除作为溶剂的苯。其后,通过蒸馏去除过量的1,3-双(氨甲基)环己烷和1,4-双(氨甲基)环己烷,获得下述式(7)所示的脂环式多胺化合物的异构体混合物17.2g。
对于得到的化合物,将气相色谱的结果示于图17,ms分析的结果示于图18,ir分析的结果示于图19,1h-nmr分析的结果示于图20。由气相色谱的结果,确认气相色谱纯度为96%,由ms分析、ir分析、1h-nmr分析的结果,确认得到的化合物为前述式(7)所示的脂环式多胺化合物的异构体混合物。另外,得到的化合物的25℃的粘度为2244mpa·s、活性氢当量为64。
将如上得到的脂环式多胺化合物3.5g与dgeba10g混合,制备环氧树脂组合物e(参照表1)。对于得到的环氧树脂组合物e,进行“涂膜干燥试验”、“环氧树脂涂膜性的评价试验”。结果示于表2。
[比较例1]
将1,3-双(氨甲基)环己烷1.9g与dgeba10g混合,制备环氧树脂组合物f。使用的1,3-双(氨甲基)环己烷的25℃的粘度为9mpa·s、活性氢当量为35.6(参照表1)。对于得到的环氧树脂组合物f,进行“涂膜干燥试验”、“环氧树脂涂膜性的评价试验(但仅进行第4天、第7天)”。结果示于表2。
[表1]
环氧树脂组合物的调制条件
[表2]
由表2可知,将本发明的多胺化合物用作固化剂的实施例的环氧树脂组合物在涂膜干燥试验中显示出良好的结果。与其相对,比较例1的环氧树脂组合物,直至完全干燥的时间为24小时以上。
另外,由涂膜性评价试验的结果可知,使用本发明的多胺化合物用作固化剂的实施例的环氧树脂组合物,可以得到外观优异、良好的固化物。与其相对,使用比较例1的环氧树脂组合物时,外观差,另外,涂膜干燥性也差。
可知如上将本发明的多胺化合物用作固化剂的实施例的环氧树脂组合物即使无需改性作为环氧树脂用固化剂是有用的。
2015年3月11日申请的日本国专利申请2015-048409号的公开,其整体通过参照并援引入本说明书。
另外,说明书中记载的所有文献、专利申请、和技术标准,各个文献、专利申请和技术标准通过参照并援引入与数个记载的情况相同程度地参照并援引入本说明书中。
产业上的可利用性
本发明的新型多胺化合物作为环氧树脂用固化剂是极有用的化合物。得到的环氧树脂组合物可以在粘接剂、涂料等广泛的领域中使用。
- 还没有人留言评论。精彩留言会获得点赞!