用于检测耐碳青霉烯类抗生素的七种耐药基因的LAMP引物组合及其应用的制作方法
本发明属于生物技术领域,具体涉及用于检测耐碳青霉烯类抗生素的七种耐药基因的LAMP引物组合及其应用。
背景技术:
我国是抗生素滥用情况最为严重的国家之一,然而随着抗生素使用量的加大,细菌耐药情况也越发严重。抗生素种类繁多,作用机制多样,其中β-内酰胺类抗生素中的碳青霉烯类可以通过与革兰氏阳性细菌或阴性细菌中大分子量青霉素结合蛋白(PBP)的高度亲和力,通过抑制细菌细胞壁合成而发挥杀菌作用。耐药细菌体内的耐药基因(如耐药基因OXA-23、耐药基因OXA-24、耐药基因OXA-58、耐药基因OXA-66、耐药基因KPC-2、耐药基因IMP-4或耐药基因VIM-2)则可通过产生灭活碳青霉烯类抗生素的β-内酰胺酶,OprD缺乏或存在外排泵,PBP靶位改变导致亲和力下降等机制完成使碳青霉烯类抗生素失活的作用。
细菌产生耐药性的原因很多,主要分为产生灭活酶、抗菌药物作用靶位改变、改变细菌外膜通透性、影响主动泵出系统、影响细菌被膜的形成及交叉耐药性等六方面。
目前关于对细菌耐药性的检测主要有以下几种方法:细菌耐药表型的检测(包括耐药筛选试验、折点敏感试验及药敏试验的仪器化和自动化等)、β-内酰胺酶检测、特殊耐药菌检测和耐药基因检测等。其中最为直观的检测方法是以体外培养的药物检测,但仍存在培养时间长等缺陷。随着耐药机理的研究逐步深入,分子生物学方法检测细菌耐药逐渐被临床接受。常见检测细菌耐药基因的方法主要有:聚合酶链式反应、PCR-限制性片段长度多态性分析、PCR-单链构象多态性分析、生物芯片技术、自动DNA测序等。传统的基因鉴定方法为PCR法和DNA测序法,其中传统的PCR法检测周期较长,通常需要3-4个小时;Sanger DNA测序法对引物特异性要求较高,且价格较昂贵,后期数据分析较复杂,不适合临床推广使用。
环介导等温扩增法(loop-mediated isothermal amplification,LAMP)是利用一种具有链置换活性和瀑布式核酸扩增功能的Bst DNA聚合酶,在等温条件下进行核酸的变性和自动循环的链置换核酸扩增反应。LAMP针对靶序列的6个区域设计4条特异引物,利用具备链置换功能的DNA聚合酶在恒定温度下不断复制扩增DNA。为了提高反应效率,可在反应体系中添加两条环引物,使之分别与茎环结构结合,启动链置换合成,循环复制。
LAMP具有简便、快速、灵敏、特异的优势,尤其适合在基层开展LAMP试剂盒的应用推广。LAMP技术中,引物是决定检测结果灵敏度和特异性的关键因素。
技术实现要素:
本发明的目的为提供一种用于检测耐碳青霉烯类抗生素的七种耐药基因的LAMP引物组合及其应用。
本发明首先提供了一种引物组合,为如下(a1)或(a2)或(a3):
(a1)由引物组Ⅰ、引物组Ⅱ、引物组Ⅲ、引物组Ⅳ、引物组Ⅴ、引物组Ⅵ和引物组Ⅶ组成;
(a2)由所述引物组Ⅰ、所述引物组Ⅱ、所述引物组Ⅲ、所述引物组Ⅳ、所述引物组Ⅴ、所述引物组Ⅵ和所述引物组Ⅶ中的任意两个、任意三个、任意四个、任意五个或任意六个组成;
(a3)所述引物组Ⅰ、所述引物组Ⅱ、所述引物组Ⅲ、所述引物组Ⅳ、所述引物组Ⅴ、所述引物组Ⅵ或所述引物组Ⅶ。
所述引物组Ⅰ可由引物Ⅰ-F3、引物Ⅰ-B3、引物Ⅰ-FIP、引物Ⅰ-BIP、引物Ⅰ-LF和引物Ⅰ-LB组成;
所述引物Ⅰ-F3可为如下(b1)或(b2);
(b1)序列表的序列1所示的单链DNA分子;
(b2)将序列1经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列1具有相同功能的DNA分子;
所述引物Ⅰ-B3可为如下(b3)或(b4);
(b3)序列表的序列2所示的单链DNA分子;
(b4)将序列2经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列2具有相同功能的DNA分子;
所述引物Ⅰ-FIP可为如下(b5)或(b6);
(b5)序列表的序列3所示的单链DNA分子;
(b6)将序列3经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列3具有相同功能的DNA分子;
所述引物Ⅰ-BIP可为如下(b7)或(b8);
(b7)序列表的序列4所示的单链DNA分子;
(b8)将序列4经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列4具有相同功能的DNA分子;
所述引物Ⅰ-LF可为如下(b9)或(b10);
(b9)序列表的序列5所示的单链DNA分子;
(b10)将序列5经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列5具有相同功能的DNA分子;
所述引物Ⅰ-LB可为如下(b11)或(b12);
(b11)序列表的序列6所示的单链DNA分子;
(b12)将序列6经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列6具有相同功能的DNA分子。
所述引物组Ⅱ可由引物Ⅱ-F3、引物Ⅱ-B3、引物Ⅱ-FIP、引物Ⅱ-BIP、引物Ⅱ-LF和引物Ⅱ-LB组成;
所述引物Ⅱ-F3可为如下(c1)或(c2);
(c1)序列表的序列7所示的单链DNA分子;
(c2)将序列7经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列7具有相同功能的DNA分子;
所述引物Ⅱ-B3可为如下(c3)或(c4);
(c3)序列表的序列8所示的单链DNA分子;
(c4)将序列8经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列8具有相同功能的DNA分子;
所述引物Ⅱ-FIP可为如下(c5)或(c6);
(c5)序列表的序列9所示的单链DNA分子;
(c6)将序列9经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列9具有相同功能的DNA分子;
所述引物Ⅱ-BIP可为如下(c7)或(c8);
(c7)序列表的序列10所示的单链DNA分子;
(c8)将序列10经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列10具有相同功能的DNA分子;
所述引物Ⅱ-LF可为如下(c9)或(c10);
(c9)序列表的序列11所示的单链DNA分子;
(c10)将序列11经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列11具有相同功能的DNA分子;
所述引物Ⅱ-LB可为如下(c11)或(c12);
(c11)序列表的序列12所示的单链DNA分子;
(c12)将序列12经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列12具有相同功能的DNA分子。
所述引物组Ⅲ可由引物Ⅲ-F3、引物Ⅲ-B3、引物Ⅲ-FIP、引物Ⅲ-BIP、引物Ⅲ-LF和引物Ⅲ-LB组成;
所述引物Ⅲ-F3可为如下(d1)或(d2);
(d1)序列表的序列13所示的单链DNA分子;
(d2)将序列13经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列13具有相同功能的DNA分子;
所述引物Ⅲ-B3可为如下(d3)或(d4);
(d3)序列表的序列14所示的单链DNA分子;
(d4)将序列14经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列14具有相同功能的DNA分子;
所述引物Ⅲ-FIP可为如下(d5)或(d6);
(d5)序列表的序列15所示的单链DNA分子;
(d6)将序列15经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列15具有相同功能的DNA分子;
所述引物Ⅲ-BIP可为如下(d7)或(d8);
(d7)序列表的序列16所示的单链DNA分子;
(d8)将序列16经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列16具有相同功能的DNA分子;
所述引物Ⅲ-LF可为如下(d9)或(d10);
(d9)序列表的序列17所示的单链DNA分子;
(d10)将序列17经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列17具有相同功能的DNA分子;
所述引物Ⅲ-LB可为如下(d11)或(d12);
(d11)序列表的序列18所示的单链DNA分子;
(d12)将序列18经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列18具有相同功能的DNA分子。
所述引物组Ⅳ可由引物Ⅳ-F3、引物Ⅳ-B3、引物Ⅳ-FIP、引物Ⅳ-BIP、引物Ⅳ-LF和引物Ⅳ-LB组成;
所述引物Ⅳ-F3可为如下(e1)或(e2);
(e1)序列表的序列19所示的单链DNA分子;
(e2)将序列19经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列19具有相同功能的DNA分子;
所述引物Ⅳ-B3可为如下(e3)或(e4);
(e3)序列表的序列20所示的单链DNA分子;
(e4)将序列20经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列20具有相同功能的DNA分子;
所述引物Ⅳ-FIP可为如下(e5)或(e6);
(e5)序列表的序列21所示的单链DNA分子;
(e6)将序列21经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列21具有相同功能的DNA分子;
所述引物Ⅳ-BIP可为如下(e7)或(e8);
(e7)序列表的序列22所示的单链DNA分子;
(e8)将序列22经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列22具有相同功能的DNA分子;
所述引物Ⅳ-LF可为如下(e9)或(e10);
(e9)序列表的序列23所示的单链DNA分子;
(e10)将序列23经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列23具有相同功能的DNA分子;
所述引物Ⅳ-LB可为如下(e11)或(e12);
(e11)序列表的序列24所示的单链DNA分子;
(e12)将序列24经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列24具有相同功能的DNA分子。
所述引物组Ⅴ可由引物Ⅴ-F3、引物Ⅴ-B3、引物Ⅴ-FIP、引物Ⅴ-BIP、引物Ⅴ-LF和引物Ⅴ-LB组成;
所述引物Ⅴ-F3可为如下(f1)或(f2);
(f1)序列表的序列25所示的单链DNA分子;
(f2)将序列25经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列25具有相同功能的DNA分子;
所述引物Ⅴ-B3可为如下(f3)或(f4);
(f3)序列表的序列26所示的单链DNA分子;
(f4)将序列26经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列26具有相同功能的DNA分子;
所述引物Ⅴ-FIP可为如下(f5)或(f6);
(f5)序列表的序列27所示的单链DNA分子;
(f6)将序列27经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列27具有相同功能的DNA分子;
所述引物Ⅴ-BIP可为如下(f7)或(f8);
(f7)序列表的序列28所示的单链DNA分子;
(f8)将序列28经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列28具有相同功能的DNA分子;
所述引物Ⅴ-LF可为如下(f9)或(f10);
(f9)序列表的序列29所示的单链DNA分子;
(f10)将序列29经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列29具有相同功能的DNA分子;
所述引物Ⅴ-LB可为如下(f11)或(f12);
(f11)序列表的序列30所示的单链DNA分子;
(f12)将序列30经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列30具有相同功能的DNA分子。
所述引物组Ⅵ可由引物Ⅵ-F3、引物Ⅵ-B3、引物Ⅵ-FIP、引物Ⅵ-BIP、引物Ⅵ-LF和引物Ⅵ-LB组成;
所述引物Ⅵ-F3可为如下(g1)或(g2);
(g1)序列表的序列31所示的单链DNA分子;
(g2)将序列31经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列31具有相同功能的DNA分子;
所述引物Ⅵ-B3可为如下(g3)或(g4);
(g3)序列表的序列32所示的单链DNA分子;
(g4)将序列32经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列32具有相同功能的DNA分子;
所述引物Ⅵ-FIP可为如下(g5)或(g6);
(g5)序列表的序列33所示的单链DNA分子;
(g6)将序列33经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列33具有相同功能的DNA分子;
所述引物Ⅵ-BIP可为如下(g7)或(g8);
(g7)序列表的序列34所示的单链DNA分子;
(g8)将序列34经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列34具有相同功能的DNA分子;
所述引物Ⅵ-LF可为如下(g9)或(g10);
(g9)序列表的序列35所示的单链DNA分子;
(g10)将序列35经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列35具有相同功能的DNA分子;
所述引物Ⅵ-LB可为如下(g11)或(g12);
(g11)序列表的序列36所示的单链DNA分子;
(g12)将序列36经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列36具有相同功能的DNA分子。
所述引物组Ⅶ可由引物Ⅶ-F3、引物Ⅶ-B3、引物Ⅶ-FIP、引物Ⅶ-BIP、引物Ⅶ-LF和引物Ⅶ-LB组成;
所述引物Ⅶ-F3可为如下(h1)或(h2);
(h1)序列表的序列37所示的单链DNA分子;
(h2)将序列37经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列37具有相同功能的DNA分子;
所述引物Ⅶ-B3可为如下(h3)或(h4);
(h3)序列表的序列38所示的单链DNA分子;
(h4)将序列38经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列38具有相同功能的DNA分子;
所述引物Ⅶ-FIP可为如下(h5)或(h6);
(h5)序列表的序列39所示的单链DNA分子;
(h6)将序列39经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列39具有相同功能的DNA分子;
所述引物Ⅶ-BIP可为如下(h7)或(h8);
(h7)序列表的序列40所示的单链DNA分子;
(h8)将序列40经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列40具有相同功能的DNA分子;
所述引物Ⅶ-LF可为如下(h9)或(h10);
(h9)序列表的序列41所示的单链DNA分子;
(h10)将序列41经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列41具有相同功能的DNA分子;
所述引物Ⅶ-LB可为如下(h11)或(h12);
(h11)序列表的序列42所示的单链DNA分子;
(h12)将序列42经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列42具有相同功能的DNA分子。
所述引物组Ⅰ中,引物Ⅰ-F3、引物Ⅰ-B3、引物Ⅰ-FIP、引物Ⅰ-BIP、引物Ⅰ-LF和引物Ⅰ-LB的摩尔比具体可为0.5:0.5:2:2:1:1。
所述引物组Ⅱ中,引物Ⅱ-F3、引物Ⅱ-B3、引物Ⅱ-FIP、引物Ⅱ-BIP、引物Ⅱ-LF和引物Ⅱ-LB的摩尔比具体可为0.5:0.5:2:2:1:1。
所述引物组Ⅲ中,引物Ⅲ-F3、引物Ⅲ-B3、引物Ⅲ-FIP、引物Ⅲ-BIP、引物Ⅲ-LF和引物Ⅲ-LB的摩尔比具体可为0.5:0.5:2:2:1:1。
所述引物组Ⅳ中,引物Ⅳ-F3、引物Ⅳ-B3、引物Ⅳ-FIP、引物Ⅳ-BIP、引物Ⅳ-LF和引物Ⅳ-LB的摩尔比具体可为0.5:0.5:2:2:1:1。
所述引物组Ⅴ中,引物Ⅴ-F3、引物Ⅴ-B3、引物Ⅴ-FIP、引物Ⅴ-BIP、引物Ⅴ-LF和引物Ⅴ-LB的摩尔比具体可为0.5:0.5:2:2:1:1。
所述引物组Ⅵ中,引物Ⅵ-F3、引物Ⅵ-B3、引物Ⅵ-FIP、引物Ⅵ-BIP、引物Ⅵ-LF和引物Ⅵ-LB的摩尔比具体可为0.5:0.5:2:2:1:1。
所述引物组Ⅶ中,引物Ⅶ-F3、引物Ⅶ-B3、引物Ⅶ-FIP、引物Ⅶ-BIP、引物Ⅶ-LF和引物Ⅶ-LB的摩尔比具体可为0.5:0.5:2:2:1:1。
本发明还保护所述引物组合在制备试剂盒中的应用;所述试剂盒的用途可为如下(y1)或(y2)或(y3):
(y1)鉴定耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2;
(y2)用于检测待测样本中是否含有耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2;
(y3)用于检测待测菌是否含有耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2。
本发明还保护含有所述引物组合的试剂盒;所述试剂盒的用途可为如下(y1)或(y2)或(y3):
(y1)鉴定耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2;
(y2)用于检测待测样本中是否含有耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2;
(y3)用于检测待测菌是否含有耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2。
本发明还保护所述试剂盒的制备方法,包括将各条引物单独包装的步骤。
本发明还保护一种检测待测菌是否含有耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2的方法,包括如下步骤:
(1)提取待测菌的基因组DNA;
(2)以步骤(1)提取的基因组DNA为模板,分别采用所述引物组合中的每个引物组进行环介导等温扩增,然后进行如下判断:
如果采用所述引物组Ⅰ可以实现以所述基因组DNA为模板的特异性扩增,待测菌中含有或疑似含有耐药基因OXA-23;如果采用所述引物组Ⅰ不可以实现以所述基因组DNA为模板的特异性扩增,待测菌中不含有或疑似不含有耐药基因OXA-23;
如果采用所述引物组Ⅱ可以实现以所述基因组DNA为模板的特异性扩增,待测菌中含有或疑似含有耐药基因OXA-24;如果采用所述引物组Ⅱ不可以实现以所述基因组DNA为模板的特异性扩增,待测菌中不含有或疑似不含有耐药基因OXA-24;
如果采用所述引物组Ⅲ可以实现以所述基因组DNA为模板的特异性扩增,待测菌中含有或疑似含有耐药基因OXA-58;如果采用所述引物组Ⅲ不可以实现以所述基因组DNA为模板的特异性扩增,待测菌中不含有或疑似不含有耐药基因OXA-58;
如果采用所述引物组Ⅳ可以实现以所述基因组DNA为模板的特异性扩增,待测菌中含有或疑似含有耐药基因OXA-66;如果采用所述引物组Ⅳ不可以实现以所述基因组DNA为模板的特异性扩增,待测菌中不含有或疑似不含有耐药基因OXA-66;
如果采用所述引物组Ⅴ可以实现以所述基因组DNA为模板的特异性扩增,待测菌中含有或疑似含有耐药基因KPC-2;如果采用所述引物组Ⅴ不可以实现以所述基因组DNA为模板的特异性扩增,待测菌中不含有或疑似不含有耐药基因KPC-2;
如果采用所述引物组Ⅵ可以实现以所述基因组DNA为模板的特异性扩增,待测菌中含有或疑似含有耐药基因IMP-4;如果采用所述引物组Ⅵ不可以实现以所述基因组DNA为模板的特异性扩增,待测菌中不含有或疑似不含有耐药基因IMP-4;
如果采用所述引物组Ⅶ可以实现以所述基因组DNA为模板的特异性扩增,待测菌中含有或疑似含有耐药基因VIM-2;如果采用所述引物组Ⅶ不可以实现以所述基因组DNA为模板的特异性扩增,待测菌中不含有或疑似不含有耐药基因VIM-2。
本发明还保护一种检测待测样本中是否含有耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2的方法,包括如下步骤:
(1)提取待测样本的总DNA;
(2)以步骤(1)提取的总DNA为模板,分别采用所述引物组合中的每个引物组进行环介导等温扩增,然后进行如下判断:
如果采用所述引物组Ⅰ可以实现以所述总DNA为模板的特异性扩增,待测样本中含有或疑似含有耐药基因OXA-23;如果采用所述引物组Ⅰ不可以实现以所述总DNA为模板的特异性扩增,待测样本中不含有或疑似不含有耐药基因OXA-23;
如果采用所述引物组Ⅱ可以实现以所述总DNA为模板的特异性扩增,待测样本中含有或疑似含有耐药基因OXA-24;如果采用所述引物组Ⅱ不可以实现以所述总DNA为模板的特异性扩增,待测样本中不含有或疑似不含有耐药基因OXA-24;
如果采用所述引物组Ⅲ可以实现以所述总DNA为模板的特异性扩增,待测样本中含有或疑似含有耐药基因OXA-58;如果采用所述引物组Ⅲ不可以实现以所述总DNA为模板的特异性扩增,待测样本中不含有或疑似不含有耐药基因OXA-58;
如果采用所述引物组Ⅳ可以实现以所述总DNA为模板的特异性扩增,待测样本中含有或疑似含有耐药基因OXA-66;如果采用所述引物组Ⅳ不可以实现以所述总DNA为模板的特异性扩增,待测样本中不含有或疑似不含有耐药基因OXA-66;
如果采用所述引物组Ⅴ可以实现以所述总DNA为模板的特异性扩增,待测样本中含有或疑似含有耐药基因KPC-2;如果采用所述引物组Ⅴ不可以实现以所述总DNA为模板的特异性扩增,待测样本中不含有或疑似不含有耐药基因KPC-2;
如果采用所述引物组Ⅵ可以实现以所述总DNA为模板的特异性扩增,待测样本中含有或疑似含有耐药基因IMP-4;如果采用所述引物组Ⅵ不可以实现以所述总DNA为模板的特异性扩增,待测样本中不含有或疑似不含有耐药基因IMP-4;
如果采用所述引物组Ⅶ可以实现以所述总DNA为模板的特异性扩增,待测样本中含有或疑似含有耐药基因VIM-2;如果采用所述引物组Ⅶ不可以实现以所述总DNA为模板的特异性扩增,待测样本中不含有或疑似不含有耐药基因VIM-2。
以上任一所述方法中,采用所述引物组Ⅰ时,所述环介导等温扩增的反应体系中引物Ⅰ-F3、引物Ⅰ-B3、引物Ⅰ-FIP、引物Ⅰ-BIP、引物Ⅰ-LF和引物Ⅰ-LB的摩尔浓度依次为0.5μM、0.5μM、2μM、2μM、1μM、1μM。
以上任一所述方法中,采用所述引物组Ⅱ时,所述环介导等温扩增的反应体系中引物Ⅱ-F3、引物Ⅱ-B3、引物Ⅱ-FIP、引物Ⅱ-BIP、引物Ⅱ-LF和引物Ⅱ-LB的摩尔浓度依次为0.5μM、0.5μM、2μM、2μM、1μM、1μM。
以上任一所述方法中,采用所述引物组Ⅲ时,所述环介导等温扩增的反应体系中引物Ⅲ-F3、引物Ⅲ-B3、引物Ⅲ-FIP、引物Ⅲ-BIP、引物Ⅲ-LF和引物Ⅲ-LB的摩尔浓度依次为0.5μM、0.5μM、2μM、2μM、1μM、1μM。
以上任一所述方法中,采用所述引物组Ⅳ时,所述环介导等温扩增的反应体系中引物Ⅳ-F3、引物Ⅳ-B3、引物Ⅳ-FIP、引物Ⅳ-BIP、引物Ⅳ-LF和引物Ⅳ-LB的摩尔浓度依次为0.5μM、0.5μM、2μM、2μM、1μM、1μM。
以上任一所述方法中,采用所述引物组Ⅴ时,所述环介导等温扩增的反应体系中引物Ⅴ-F3、引物Ⅴ-B3、引物Ⅴ-FIP、引物Ⅴ-BIP、引物Ⅴ-LF和引物Ⅴ-LB的摩尔浓度依次为0.5μM、0.5μM、2μM、2μM、1μM、1μM。
以上任一所述方法中,采用所述引物组Ⅵ时,所述环介导等温扩增的反应体系中引物Ⅵ-F3、引物Ⅵ-B3、引物Ⅵ-FIP、引物Ⅵ-BIP、引物Ⅵ-LF和引物Ⅵ-LB的摩尔浓度依次为0.5μM、0.5μM、2μM、2μM、1μM、1μM。
以上任一所述方法中,采用所述引物组Ⅶ时,所述环介导等温扩增的反应体系中引物Ⅶ-F3、引物Ⅶ-B3、引物Ⅶ-FIP、引物Ⅶ-BIP、引物Ⅶ-LF和引物Ⅶ-LB的摩尔浓度依次为0.5μM、0.5μM、2μM、2μM、1μM、1μM。
以上任一所述方法中,环介导等温扩增反应条件为:65℃恒温50min。
本发明还保护所述引物组合在检测待测菌是否含有耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2中的应用。
本发明还保护所述引物组合在检测待测样本中是否含有耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2中的应用。
本发明还保护所述引物组合在鉴定耐药基因OXA-23和/或耐药基因OXA-24和/或耐药基因OXA-58和/或耐药基因OXA-66和/或耐药基因KPC-2和/或耐药基因IMP-4和/或耐药基因VIM-2中的应用。
以上任一所述待测样本可为人(Homo sapiens)的脓液。
以上任一所述耐药基因OXA-23具体可为Genebank号为KP203815.1的核苷酸序列所示的DNA分子。以上任一所述耐药基因OXA-24具体可为Genebank号为KR922888.1的核苷酸序列所示的DNA分子。以上任一所述耐药基因OXA-58具体可为Genebank号为KF740447.1的核苷酸序列所示的DNA分子。以上任一所述耐药基因OXA-66具体可为Genebank号为DQ923479.1的核苷酸序列所示的DNA分子。以上任一所述耐药基因KPC-2具体可为Genebank号为KT001101.1的核苷酸序列所示的DNA分子。以上任一所述耐药基因IMP-4具体可为Genebank号为AY795963.1的核苷酸序列所示的DNA分子。以上任一所述耐药基因VIM-2具体可为NCBI Gene ID号为14678525的核苷酸序列所示的DNA分子。
环介导等温扩增技术(loop-mediated isothermal amplification,LAMP)是近年来发展出的一种敏感、特异、简便、快捷的核酸扩增技术,其原理是在一种具有链置换活性的DNA聚合酶的作用下,识别6-8个区域的4-6条引物,在等温条件下快速、特异地扩增目的基因,可推广应用于快速、准确的检测常见的碳青霉烯类耐药基因。LAMP方法具有灵敏性高、特异性好、反应时间短、判定结果方便、不需要昂贵仪器等优势。
本发明提供的引物组合鉴定用于检测耐碳青霉烯类抗生素的七种耐药基因,具有高特异性和高灵敏度,可以实现简便、快速、准确检测。本发明具有重大的推广价值。
附图说明
图1为实施例2中采用引物组Ⅰ的检测结果。
图2为实施例2中采用引物组Ⅱ的检测结果。
图3为实施例2中采用引物组Ⅲ的检测结果。
图4为实施例2中采用引物组Ⅳ的检测结果。
图5为实施例2中采用引物组Ⅴ的检测结果。
图6为实施例2中采用引物组Ⅵ的检测结果。
图7为实施例2中采用引物组Ⅶ的检测结果。
图8为实施例4中样本一的检测结果。
图9为实施例4中样本二的检测结果。
图10为实施例4中样本三的检测结果。
具体实施方式
下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。
反应液为博奥生物集团有限公司的产品,产品目录号为CP.440020。pUC57质粒为生工生物工程(上海)股份有限公司的产品。-T Easy质粒为Promega公司的产品。
DNA拷贝数的计算方法如下:
1 A260吸光度值=ds DNA 50μg/ml;
核酸浓度=(OD260)×(稀释倍数)×(50)=x ng/μl;
平均分子量(MW)代表克/摩尔,单位道尔顿(dolton),即1dolton=1g/mol;
摩尔=6.02×1023;
平均分子量(MW):dsDNA=(碱基数)×(660道尔顿/碱基);
拷贝数计算公式:
(6.02×1023copies/摩尔)×(x ng/μl×10-9)/(DNA长度×660)=copies/μl。
实施例1、试剂盒的制备
试剂盒由七个LAMP引物组组成,每个引物组用于检测一种耐碳青霉烯类抗生素的耐药基因。
用于检测耐药基因OXA-23的引物组如下:
外引物F3:5’-GAATATGTGCCAGCCTCTA-3’(序列表中序列1);
外引物B3:5’-TCTTTTTGCATGAGATCAAGAC-3’(序列表中序列2);
内引物FIP:5’-CCTTTTCTCGCCCTTCCATTTAAATTTGAATGCCCTGATCGGA-3’(序列表中序列3);
内引物BIP:5’-TACCGCTTGGGAAAAAGACATGGTCGCGCAAGTTCCTGA-3’(序列表中序列4);
环引物LF:5’-CCGTTTTCTGGTTCTCCAA-3’(序列表中序列5);
环引物LB:5’-ACACTAGGAGAAGCCATGA-3’(序列表中序列6)。
用于检测耐药基因OXA-24的引物组如下:
外引物F3:5’-CTGTGTTCCAATATTTGTATTTCC-3’(序列表中序列7);
外引物B3:5’-GCAACAACAAATGAGATTTTCA-3’(序列表中序列8);
内引物FIP:5’-ATCAAGAGCTTGCAAGACGGACATTAACCCGCTTTACTTCTTTCTG-3’(序列表中序列9);
内引物BIP:5’-CTGGAACTGCTGACAATGCCATTGAATGGGATGGTAAAAAAAGAACTT-3’(序列表中序列10);
环引物LF:5’-TGGCCTAGAGCTAATG-3’(序列表中序列11);
环引物LB:5’-CCTCACCTAAAGTCATATC-3’(序列表中序列12)。
用于检测耐药基因OXA-58的引物组如下:
外引物F3:5’-CCAATTAGTGCATTGGCAATT-3’(序列表中序列13);
外引物B3:5’-TTGGGGCTTGTGCTGAG-3’(序列表中序列14);
内引物FIP:5’-TGTGTTTGTCACATATGATGGTCAAAGATGCAGGAATATAAGCTGTT-3’(序列表中序列15);
内引物BIP:5’-CGCTTGAACATTCTGATCGATGATTATGAGTCGAGCAAAAACAAGTACA-3’(序列表中序列16);
环引物LF:5’-GCATTTAGACCGAGCA-3’(序列表中序列17);
环引物LB:5’-GAGTTATTCACTTGTGGAA-3’(序列表中序列18)。
用于检测耐药基因OXA-66的引物组如下:
外引物F3:5’-CTAATAAAACGCTTCCATTTAGC-3’(序列表中序列19);
外引物B3:5’-GAACAGAGCTAGGTATTCCTT-3’(序列表中序列20);
内引物FIP:5’-ACATCCCATCCCCAACCACTTTTTGTCCAAGATGAAGTGCAATCC-3’(序列表中序列21);
内引物BIP:5’-CCACAAGTAGGCTGGTTAACTGTCTAAGTTAAGGGAGAACGCTACA-3’(序列表中序列22);
环引物LF:5’-CCATTCTTTTCTTCTATGAATAGCA-3’(序列表中序列23);
环引物LB:5’-TTGTTCAGCCTCAAGGGAAT-3’(序列表中序列24)。
用于检测耐药基因KPC-2的引物组如下:
外引物F3:5’-CTGACGGCCTTCATGCG-3’(序列表中序列25);
外引物B3:5’-GCCAATCAACAAACTGCT-3’(序列表中序列26);
内引物FIP:5’-ATGGCGGAGTTCAGCTCCATCTATCGGCGATACCACGT-3’(序列表中序列27);
内引物BIP:5’-AGGCGATGCGCGCGATACCCAGTGTCAGTTTTTGTAAGC-3’(序列表中序列28);
环引物LF:5’-CCAGCGGTCCAGACG-3’(序列表中序列29);
环引物LB:5’-GCGCCGTGACGGAAA-3’(序列表中序列30)。
用于检测耐药基因IMP-4的引物组如下:
外引物F3:5’-TCTAATTGACACTCCATTTACG-3’(序列表中序列31);
外引物B3:5’-AGTTAACCCCGCCAAAT-3’(序列表中序列32);
内引物FIP:5’-ATGAAAATGAGAGGAAATACTGCCTATACTGAAAAGTTAGTCACTTGGT-3’(序列表中序列33);
内引物BIP:5’-TGGCTTAATTCTCAATCCATCCCTTAGCTTGAACCTTACCGTCT-3’(序列表中序列34);
环引物LF:5’-ATAGCCACGTTCCACAA-3’(序列表中序列35);
环引物LB:5’-CGTATGCGTCTGAATTAAC-3’(序列表中序列36)。
用于检测耐药基因VIM-2的引物组如下:
外引物F3:5’-GGCACTTCTCGCGGAGA-3’(序列表中序列37);
外引物B3:5’-GCTCGATGAGAGTCCTTCT-3’(序列表中序列38);
内引物FIP:5’-CGACGCGGTCGTCATGAAAGCAAATTGGACTTCCTGTAACG-3’(序列表中序列39);
内引物BIP:5’-GGCTGGGGTGGCAACGTACAGTGCGTGGGAATCTCG-3’(序列表中序列40);
环引物LF:5’-GCGTGGAGACTGCAC-3’(序列表中序列41);
环引物LB:5’-GCATCACCGTCGACAC-3’(序列表中序列42)。
用于检测耐药基因OXA-23的引物组命名为引物组Ⅰ。用于检测耐药基因OXA-24的引物组命名为引物组Ⅱ。用于检测耐药基因OXA-58的引物组命名为引物组Ⅲ。用于检测耐药基因OXA-66的引物组命名为引物组Ⅳ。用于检测耐药基因KPC-2的引物组命名为引物组Ⅴ。用于检测耐药基因IMP-4的引物组命名为引物组Ⅵ。用于检测耐药基因VIM-2的引物组命名为引物组Ⅶ。
实施例2、特异性实验
待测样本1:含耐药基因OXA-23的质粒。含耐药基因OXA-23的质粒的制备方法为:将-T Easy质粒的EcoRI和SpeI间的DNA片段替换为Genebank号为KP203815.1的核苷酸序列所示的DNA分子,得到的重组质粒即为含耐药基因OXA-23的质粒。
待测样本2:含耐药基因OXA-24的质粒。含耐药基因OXA-24的质粒的制备方法为:将-T Easy质粒的EcoRI和SpeI间的DNA片段替换为Genebank号为KR922888.1的核苷酸序列所示的DNA分子,得到的重组质粒即为含耐药基因OXA-24的质粒。
待测样本3:含耐药基因OXA-58的质粒。含耐药基因OXA-58的质粒的制备方法为:将-T Easy质粒的EcoRI和SpeI间的DNA片段替换为Genebank号为KF740447.1的核苷酸序列所示的DNA分子,得到的重组质粒即为含耐药基因OXA-58的质粒。
待测样本4:含耐药基因OXA-66的质粒。含耐药基因OXA-66的质粒的制备方法为:将pUC57质粒的MCS区间的DNA片段替换为Genebank号为DQ923479.1所示的DNA分子,得到的重组质粒即为含耐药基因OXA-66的质粒。
待测样本5:含耐药基因KPC-2的质粒。含耐药基因KPC-2的质粒的制备方法为:将-T Easy质粒的EcoRI和SpeI间的DNA片段替换为Genebank号为KT001101.1的核苷酸序列所示的DNA分子,得到的重组质粒即为含耐药基因KPC-2的质粒。
待测样本6:含耐药基因IMP-4的质粒。含耐药基因IMP-4的质粒的制备方法为:将-T Easy质粒的EcoRI和SpeI间的DNA片段替换为Genebank号为AY795963.1的核苷酸序列所示的DNA分子,得到的重组质粒即为含耐药基因IMP-4的质粒。
待测样本7:含耐药基因VIM-2的质粒。含耐药基因VIM-2的质粒的制备方法为:将-T Easy质粒的EcoRI和SpeI间的DNA片段替换为NCBI Gene ID号为14678525的核苷酸序列所示的DNA分子,得到的重组质粒即为含耐药基因VIM-2的质粒。
各个待测样本分别进行如下步骤:
1、提取待测样本的质粒DNA。
2、以步骤1提取的质粒DNA为模板,分别采用实施例1制备的各个引物组进行环介导等温扩增。
反应体系(10μL):7.0μL反应液、1μL引物混合物、1μL质粒DNA(5pg-50pg),补水至10μL。引物混合物即引物组中的各条引物组成的混合物。反应体系中,外引物F3和外引物B3的终浓度均为0.5μM,内引物FIP和内引物BIP的终浓度均为2μM,环引物LF和环引物LB的终浓度均为1μM。
反应条件:65℃恒温50min。反应过程中,采用荧光PCR仪检测荧光信号。
按照上述方法,将质粒DNA替换为无菌水,其它步骤均不变,作为空白对照。
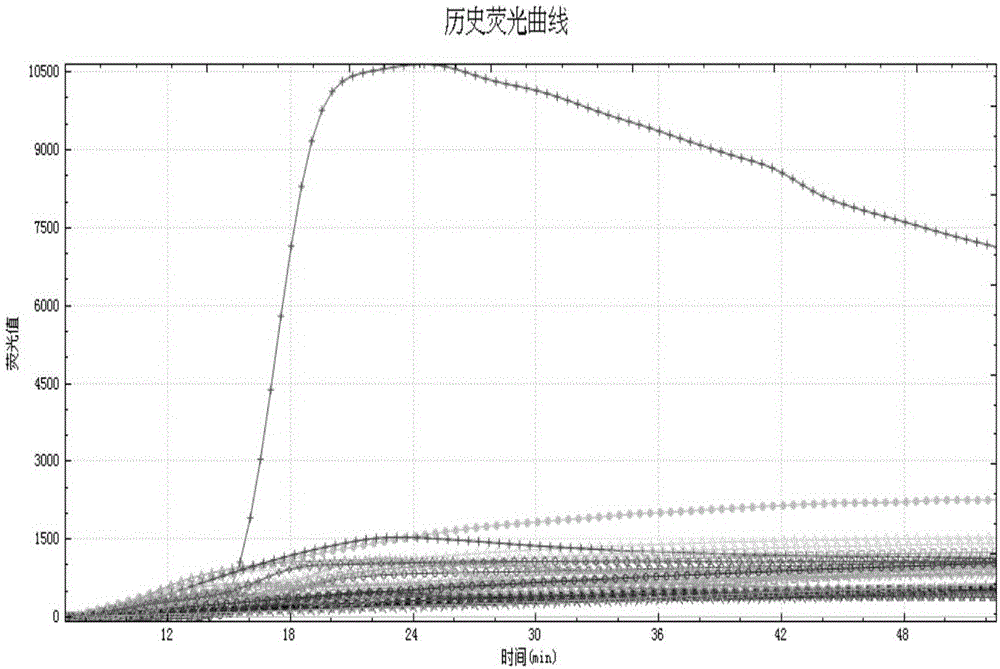
采用引物组Ⅰ的结果见图1(“S型”扩增曲线为待测样本1,非“S型”扩增曲线为其它待测样本或空白对照)。待测样本为含耐药基因OXA-23的质粒的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。待测样本为待测样本2、待测样本3、待测样本4、待测样本5、待测样本6或待测样本7的时候均不显示阳性扩增曲线。
采用引物组Ⅱ的结果见图2(“S型”扩增曲线为待测样本2,非“S型”扩增曲线为其它待测样本或空白对照)。待测样本为含耐药基因OXA-24的质粒的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。待测样本为待测样本1、待测样本3、待测样本4、待测样本5、待测样本6或待测样本7的时候均不显示阳性扩增曲线。
采用引物组Ⅲ的结果见图3(“S型”扩增曲线为待测样本3,非“S型”扩增曲线为其它待测样本或空白对照)。待测样本为含耐药基因OXA-58的质粒的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。待测样本为待测样本1、待测样本2、待测样本4、待测样本5、待测样本6或待测样本7的时候均不显示阳性扩增曲线。
采用引物组Ⅳ的结果见图4(“S型”扩增曲线为待测样本4,非“S型”扩增曲线为其它待测样本或空白对照)。待测样本为含耐药基因OXA-66的质粒的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。待测样本为待测样本1、待测样本2、待测样本3、待测样本5、待测样本6或待测样本7的时候均不显示阳性扩增曲线。
采用引物组Ⅴ的结果见图5(“S型”扩增曲线为待测样本5,非“S型”扩增曲线为其它待测样本或空白对照)。待测样本为含耐药基因KPC-2的质粒的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。待测样本为待测样本1、待测样本2、待测样本3、待测样本4、待测样本6或待测样本7的时候均不显示阳性扩增曲线。
采用引物组Ⅵ的结果见图6(“S型”扩增曲线为待测样本6,非“S型”扩增曲线为其它待测样本或空白对照)。待测样本为含耐药基因IMP-4的质粒的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。待测样本为待测样本1、待测样本2、待测样本3、待测样本4、待测样本5或待测样本7的时候均不显示阳性扩增曲线。
采用引物组Ⅶ的结果见图7(“S型”扩增曲线为待测样本7,非“S型”扩增曲线为其它待测样本或空白对照)。待测样本为含耐药基因VIM-2的质粒的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。待测样本为待测样本1、待测样本2、待测样本3、待测样本4、待测样本5或待测样本6的时候均不显示阳性扩增曲线。
以上结果表明,本发明提供的七个引物组分别对其靶标基因具有很高的特异性。
实施例3、灵敏度实验
待测样本1:实施例2中制备的含耐药基因OXA-23的质粒。
待测样本2:实施例2中制备的含耐药基因OXA-24的质粒。
待测样本3:实施例2中制备的含耐药基因OXA-58的质粒。
待测样本4:实施例2中制备的含耐药基因OXA-66的质粒。
待测样本5:实施例2中制备的含耐药基因KPC-2的质粒。
待测样本6:实施例2中制备的含耐药基因IMP-4的质粒。
待测样本7:实施例2中制备的含耐药基因VIM-2的质粒。
1、提取待测样本的质粒DNA,用无菌水进行梯度稀释,得到各个稀释液。
2、以步骤1得到的稀释液为模板,分别采用实施例1制备的引物组进行环介导等温扩增。
待测样本为待测样本1时,采用引物组Ⅰ进行环介导等温扩增。待测样本为待测样本2时,采用引物组Ⅱ进行环介导等温扩增。待测样本为待测样本3时,采用引物组Ⅲ进行环介导等温扩增。待测样本为待测样本4时,采用引物组Ⅳ进行环介导等温扩增。待测样本为待测样本5时,采用引物组Ⅴ进行环介导等温扩增。待测样本为待测样本6时,采用引物组Ⅵ进行环介导等温扩增。待测样本为待测样本7时,采用引物组Ⅶ进行环介导等温扩增。
反应体系(10μL):7.0μL反应液、1μL引物混合物、1μL稀释液(1μL稀释液中含有的基因组拷贝数分别为103、5×102、102或101),补水至10μL。引物混合物即引物组中的各条引物组成的混合物。反应体系中,外引物F3和外引物B3的终浓度均为0.5μM,内引物FIP和内引物BIP的终浓度均为2μM,环引物LF和环引物LB的终浓度均为1μM。
反应条件:65℃恒温50min。反应过程中,采用荧光PCR仪检测荧光信号。
如果在50min内出现阳性扩增曲线(即扩增曲线为“S型”扩增曲线),表明反应体系中的相应基因组含量可以被检测出来。如果在50min内没有出现阳性扩增曲线,表明反应体系中的相应基因组含量不能被检测出来。
引物组Ⅰ检测靶标基因的灵敏度为5×102个拷贝数/反应体系,引物组Ⅱ检测靶标基因的灵敏度为5×102个拷贝数/反应体系,引物组Ⅲ检测靶标基因的灵敏度为5×102个拷贝数/反应体系,引物组Ⅳ检测靶标基因的灵敏度为5×102个拷贝数/反应体系,引物组Ⅴ检测靶标基因的灵敏度为5×102个拷贝数/反应体系,引物组Ⅵ检测靶标基因的灵敏度为5×102个拷贝数/反应体系,引物组Ⅶ检测靶标基因的灵敏度为5×102个拷贝数/反应体系。
实施例4、应用
待测样本为如下样本一、样本二或样本三:
样本一:已通过药敏鉴定及PCR测序鉴定确认含有耐药基因OXA-23的脓液;
样本二:已通过药敏鉴定及PCR测序鉴定确认含有耐药基因KPC-2的脓液;
样本三:已通过药敏鉴定及PCR测序鉴定确认含有耐药基因IMP-4的脓液。
1、提取待测样本的总DNA。
2、以步骤1提取的待测样本的总DNA为模板,分别采用实施例1制备的各个引物组进行环介导等温扩增。
反应体系与反应条件均同实施例2。反应过程中,采用荧光PCR仪检测荧光信号。
按照上述方法,将待测样本的总DNA替换为无菌水,其它步骤均不变,作为空白对照。
样本一的结果见图8(“S型”扩增曲线为引物组Ⅰ,非“S型”扩增曲线为其它引物组或空白对照)。采用引物组Ⅰ的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。采用引物组Ⅰ以外的其它六个引物组或空白对照的时候均不显示阳性扩增曲线,与实际情况完全一致。
样本二的结果见图9(“S型”扩增曲线为引物组Ⅴ,非“S型”扩增曲线为其它引物组或空白对照)。采用引物组Ⅴ的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。采用引物组Ⅴ以外的其它六个引物组或空白对照的时候均不显示阳性扩增曲线,与实际情况完全一致。
样本三的结果见图10(“S型”扩增曲线为引物组Ⅵ,非“S型”扩增曲线为其它引物组或空白对照)。采用引物组Ⅵ的时候显示阳性扩增曲线(即扩增曲线为“S型”扩增曲线)。采用引物组Ⅵ以外的其它六个引物组或空白对照的时候均不显示阳性扩增曲线,与实际情况完全一致。
以上结果表明,利用本发明提供的试剂盒可以对耐碳青霉烯类抗生素的七种耐药基因进行检测,结果准确可靠。
<110> 博奥生物集团有限公司
<120> 用于检测耐碳青霉烯类抗生素的七种耐药基因的LAMP引物组合及其应用
<160> 42
<170> PatentIn version 3.5
<210> 1
<211> 19
<212> DNA
<213> 人工序列
<220>
<223>
<400> 1
gaatatgtgc cagcctcta 19
<210> 2
<211> 22
<212> DNA
<213> 人工序列
<220>
<223>
<400> 2
tctttttgca tgagatcaag ac 22
<210> 3
<211> 43
<212> DNA
<213> 人工序列
<220>
<223>
<400> 3
ccttttctcg cccttccatt taaatttgaa tgccctgatc gga 43
<210> 4
<211> 39
<212> DNA
<213> 人工序列
<220>
<223>
<400> 4
taccgcttgg gaaaaagaca tggtcgcgca agttcctga 39
<210> 5
<211> 19
<212> DNA
<213> 人工序列
<220>
<223>
<400> 5
ccgttttctg gttctccaa 19
<210> 6
<211> 19
<212> DNA
<213> 人工序列
<220>
<223>
<400> 6
acactaggag aagccatga 19
<210> 7
<211> 24
<212> DNA
<213> 人工序列
<220>
<223>
<400> 7
ctgtgttcca atatttgtat ttcc 24
<210> 8
<211> 22
<212> DNA
<213> 人工序列
<220>
<223>
<400> 8
gcaacaacaa atgagatttt ca 22
<210> 9
<211> 46
<212> DNA
<213> 人工序列
<220>
<223>
<400> 9
atcaagagct tgcaagacgg acattaaccc gctttacttc tttctg 46
<210> 10
<211> 48
<212> DNA
<213> 人工序列
<220>
<223>
<400> 10
ctggaactgc tgacaatgcc attgaatggg atggtaaaaa aagaactt 48
<210> 11
<211> 16
<212> DNA
<213> 人工序列
<220>
<223>
<400> 11
tggcctagag ctaatg 16
<210> 12
<211> 19
<212> DNA
<213> 人工序列
<220>
<223>
<400> 12
cctcacctaa agtcatatc 19
<210> 13
<211> 21
<212> DNA
<213> 人工序列
<220>
<223>
<400> 13
ccaattagtg cattggcaat t 21
<210> 14
<211> 17
<212> DNA
<213> 人工序列
<220>
<223>
<400> 14
ttggggcttg tgctgag 17
<210> 15
<211> 47
<212> DNA
<213> 人工序列
<220>
<223>
<400> 15
tgtgtttgtc acatatgatg gtcaaagatg caggaatata agctgtt 47
<210> 16
<211> 49
<212> DNA
<213> 人工序列
<220>
<223>
<400> 16
cgcttgaaca ttctgatcga tgattatgag tcgagcaaaa acaagtaca 49
<210> 17
<211> 16
<212> DNA
<213> 人工序列
<220>
<223>
<400> 17
gcatttagac cgagca 16
<210> 18
<211> 19
<212> DNA
<213> 人工序列
<220>
<223>
<400> 18
gagttattca cttgtggaa 19
<210> 19
<211> 23
<212> DNA
<213> 人工序列
<220>
<223>
<400> 19
ctaataaaac gcttccattt agc 23
<210> 20
<211> 21
<212> DNA
<213> 人工序列
<220>
<223>
<400> 20
gaacagagct aggtattcct t 21
<210> 21
<211> 45
<212> DNA
<213> 人工序列
<220>
<223>
<400> 21
acatcccatc cccaaccact ttttgtccaa gatgaagtgc aatcc 45
<210> 22
<211> 46
<212> DNA
<213> 人工序列
<220>
<223>
<400> 22
ccacaagtag gctggttaac tgtctaagtt aagggagaac gctaca 46
<210> 23
<211> 25
<212> DNA
<213> 人工序列
<220>
<223>
<400> 23
ccattctttt cttctatgaa tagca 25
<210> 24
<211> 20
<212> DNA
<213> 人工序列
<220>
<223>
<400> 24
ttgttcagcc tcaagggaat 20
<210> 25
<211> 17
<212> DNA
<213> 人工序列
<220>
<223>
<400> 25
ctgacggcct tcatgcg 17
<210> 26
<211> 18
<212> DNA
<213> 人工序列
<220>
<223>
<400> 26
gccaatcaac aaactgct 18
<210> 27
<211> 38
<212> DNA
<213> 人工序列
<220>
<223>
<400> 27
atggcggagt tcagctccat ctatcggcga taccacgt 38
<210> 28
<211> 39
<212> DNA
<213> 人工序列
<220>
<223>
<400> 28
aggcgatgcg cgcgataccc agtgtcagtt tttgtaagc 39
<210> 29
<211> 15
<212> DNA
<213> 人工序列
<220>
<223>
<400> 29
ccagcggtcc agacg 15
<210> 30
<211> 15
<212> DNA
<213> 人工序列
<220>
<223>
<400> 30
gcgccgtgac ggaaa 15
<210> 31
<211> 22
<212> DNA
<213> 人工序列
<220>
<223>
<400> 31
tctaattgac actccattta cg 22
<210> 32
<211> 17
<212> DNA
<213> 人工序列
<220>
<223>
<400> 32
agttaacccc gccaaat 17
<210> 33
<211> 49
<212> DNA
<213> 人工序列
<220>
<223>
<400> 33
atgaaaatga gaggaaatac tgcctatact gaaaagttag tcacttggt 49
<210> 34
<211> 44
<212> DNA
<213> 人工序列
<220>
<223>
<400> 34
tggcttaatt ctcaatccat cccttagctt gaaccttacc gtct 44
<210> 35
<211> 17
<212> DNA
<213> 人工序列
<220>
<223>
<400> 35
atagccacgt tccacaa 17
<210> 36
<211> 19
<212> DNA
<213> 人工序列
<220>
<223>
<400> 36
cgtatgcgtc tgaattaac 19
<210> 37
<211> 17
<212> DNA
<213> 人工序列
<220>
<223>
<400> 37
ggcacttctc gcggaga 17
<210> 38
<211> 19
<212> DNA
<213> 人工序列
<220>
<223>
<400> 38
gctcgatgag agtccttct 19
<210> 39
<211> 41
<212> DNA
<213> 人工序列
<220>
<223>
<400> 39
cgacgcggtc gtcatgaaag caaattggac ttcctgtaac g 41
<210> 40
<211> 36
<212> DNA
<213> 人工序列
<220>
<223>
<400> 40
ggctggggtg gcaacgtaca gtgcgtggga atctcg 36
<210> 41
<211> 15
<212> DNA
<213> 人工序列
<220>
<223>
<400> 41
gcgtggagac tgcac 15
<210> 42
<211> 16
<212> DNA
<213> 人工序列
<220>
<223>
<400> 42
gcatcaccgt cgacac 16
- 还没有人留言评论。精彩留言会获得点赞!