检测PKLR基因突变的方法、试剂盒、寡核苷酸及其应用与流程
红细胞丙酮酸激酶是糖酵解途径的三个关键限速酶之一。其作用为催化磷酸烯酮式丙酮酸转化为丙酮酸,同时产生ATP为红细胞提供能量。丙酮酸激酶(pyruvate kinase,PK)有四种同工酶:L、R、M1、M2,其中R型存在于成熟的红细胞中,由PKLR基因编码。红细胞中的丙酮酸激酶遗传性缺乏可引起红细胞能量代谢异常,非球性细胞性溶血性贫血,其分子水平上则存在PKLR基因的突变。
PKLR基因位于1号染色体长臂2区1带,包含11个外显子,共编码574个氨基酸。PKLR基因突变是丙酮酸激酶缺乏症的重要原因。自1961年初次报道后,迄今为止国内外共发现200余例PKLR突变。PKLR的突变种类几乎遍布整个基因,其中最常见的突变为错义突变,包括美国和欧洲的热点突变1529G>A,南欧的热点突变1456C>T和亚洲的1468C>T。
到目前为止PKLR基因的突变是如何引起酶缺乏的机制尚未完全清楚,其可能原因有:部分突变位于丙酮酸激酶活性中心,改变了底物磷酸烯醇式丙酮酸的结合力;部分突变可能引起突变点附近的疏水性下降,影响K+与其结合,导致Km升高;少数位于C区的突变会使结构改变,减弱亚单位间连接,影响三聚体形成,从而降低丙酮酸激酶的活性。
丙酮酸激酶缺乏症的患者严重时在新生儿期即出现严重贫血、需要终生输血。目前临床以检测丙酮酸激酶活性的方法来诊断丙酮酸激酶缺乏症,但这受到多种因素的影响,所以无论对是患者还是对产前诊断来说,对PKLR基因进行全外显子测序都具有非常重要的意义。
技术实现要素:
本发明的目的在于提供检测PKLR基因突变的寡核苷酸,采用PCR技术,可用于快速检测丙酮酸激酶缺乏症患者体内的PKLR基因外显子突变情况。所述寡核苷酸包括至少一对扩增PKLR基因外显子的引物,所述至少一对扩增引物选自PKLR-1F/PKLR-1R、PKLR-2F/PKLR-2R、PKLR-3-4-5F/PKLR-3-4-5R、PKLR-6-7F/PKLR-6-7R、PKLR-8-9F/PKLR-8-9R、PKLR-10F/PKLR-10R,或PKLR-11F/PKLR-11R,其碱基序列为:
PKLR-1F:TGTAAAACGACGGCCAGTAGAGGAAATGCCAGGAGATGA;
PKLR-1R:AACAGCTATGACCATGTTCACCCTCATTTTCCTCCTAT;
PKLR-2F:TGTAAAACGACGGCCAGTAGAGGGTATGCTGAGAGACGAA;
PKLR-2R:AACAGCTATGACCATGAAGAAGCACCTCAAGAAATACCA;
PKLR-3-4-5F:TGTAAAACGACGGCCAGTGGGTTGCATCAGGGAATAAA;
PKLR-3-4-5R:AACAGCTATGACCATGGCCAAGGAGAAGGGAATGTG;
PKLR-6-7F:TGTAAAACGACGGCCAGTGACTATGGGTGGGTCGTTTCT;
PKLR-6-7R:AACAGCTATGACCATGCACCCACAGGTGTCCCTAAAA;
PKLR-8-9F:TGTAAAACGACGGCCAGTGTGTGGGTGTCAGAGAAGTAGC;
PKLR-8-9R:AACAGCTATGACCATGTGGCATTCTGTCTCTCCTGG;
PKLR-10F:TGTAAAACGACGGCCAGTGTGACACCTGGAACTGGAACA;
PKLR-10R:AACAGCTATGACCATGGACCACAGGAGAGAGGCAAG;
PKLR-11F:TGTAAAACGACGGCCAGTGCCAGGCTGGTCTCAAACT;
PKLR-11R:AACAGCTATGACCATGATGAGAATGGGAGACTGTGGA。
进一步地,所述寡核苷酸还包括一对测序引物M13F和M13R,其碱基序列为:
M13F:TGTAAAACGACGGCCAGT;
M13R:AACAGCTATGACCATG。
进一步地,PKLR-1F:PKLR-1R、PKLR-2F:PKLR-2R、PKLR-3-4-5F:PKLR-3-4-5R、PKLR-6-7F:PKLR-6-7R、PKLR-8-9F:PKLR-8-9R、PKLR-10F:PKLR-10R,或PKLR-11F:PKLR-11R的比值均为1。
进一步地,M13F:M13R的比值为1。
进一步地,所述寡核苷酸在辅助检测丙酮酸激酶缺乏症中的应用。
本发明的目的还在于提供一种检测PKLR基因突变的方法,包括以下步骤:
(1)抽提样本中的基因组DNA;
(2)利用至少一对扩增引物对(1)中的DNA进行扩增,获得扩增产物;
(3)利用一对测序引物M13F和M13R对(2)中的扩增产物进行测序,获得所述扩增产物的碱基序列;
(4)将(3)中的碱基序列与PKLR基因野生型参考序列进行比较,确定突变位点是否存在,其中,所述至少一对扩增引物选自PKLR-1F/PKLR-1R、PKLR-2F/PKLR-2R、PKLR-3-4-5F/PKLR-3-4-5R、PKLR-6-7F/PKLR-6-7R、PKLR-8-9F/PKLR-8-9R、PKLR-10F/PKLR-10R,或PKLR-11F/PKLR-11R,其碱基序列为:
PKLR-1F:TGTAAAACGACGGCCAGTAGAGGAAATGCCAGGAGATGA;
PKLR-1R:AACAGCTATGACCATGTTCACCCTCATTTTCCTCCTAT;
PKLR-2F:TGTAAAACGACGGCCAGTAGAGGGTATGCTGAGAGACGAA;
PKLR-2R:AACAGCTATGACCATGAAGAAGCACCTCAAGAAATACCA;
PKLR-3-4-5F:TGTAAAACGACGGCCAGTGGGTTGCATCAGGGAATAAA;
PKLR-3-4-5R:AACAGCTATGACCATGGCCAAGGAGAAGGGAATGTG;
PKLR-6-7F:TGTAAAACGACGGCCAGTGACTATGGGTGGGTCGTTTCT;
PKLR-6-7R:AACAGCTATGACCATGCACCCACAGGTGTCCCTAAAA;
PKLR-8-9F:TGTAAAACGACGGCCAGTGTGTGGGTGTCAGAGAAGTAGC;
PKLR-8-9R:AACAGCTATGACCATGTGGCATTCTGTCTCTCCTGG;
PKLR-10F:TGTAAAACGACGGCCAGTGTGACACCTGGAACTGGAACA;
PKLR-10R:AACAGCTATGACCATGGACCACAGGAGAGAGGCAAG;
PKLR-11F:TGTAAAACGACGGCCAGTGCCAGGCTGGTCTCAAACT;
PKLR-11R:AACAGCTATGACCATGATGAGAATGGGAGACTGTGGA;
M13F:TGTAAAACGACGGCCAGT;
M13R:AACAGCTATGACCATG。
进一步地,PKLR-1F:PKLR-1R、PKLR-2F:PKLR-2R、PKLR-3-4-5F:PKLR-3-4-5R、PKLR-6-7F:PKLR-6-7R、PKLR-8-9F:PKLR-8-9R、PKLR-10F:PKLR-10R,或PKLR-11F:PKLR-11R的比值均为1。
进一步地,M13F:M13R的比值为1。
进一步地,所述方法在辅助检测丙酮酸激酶缺乏症中的应用。
本发明的目的还在于提供一种检测PKLR基因突变的试剂盒,所述试剂盒包括检测体系PCR扩增反应液、测序体系反应液,其中,检测体系PCR扩增反应液包括至少一对扩增引物,所述测序体系反应液包括一对测序引物M13F和M13R,所述至少一对扩增引物选自PKLR-1F/PKLR-1R、PKLR-2F/PKLR-2R、PKLR-3-4-5F/PKLR-3-4-5R、PKLR-6-7F/PKLR-6-7R、PKLR-8-9F/PKLR-8-9R、PKLR-10F/PKLR-10R,或PKLR-11F/PKLR-11R,其碱基序列为:
PKLR-1F:TGTAAAACGACGGCCAGTAGAGGAAATGCCAGGAGATGA;
PKLR-1R:AACAGCTATGACCATGTTCACCCTCATTTTCCTCCTAT;
PKLR-2F:TGTAAAACGACGGCCAGTAGAGGGTATGCTGAGAGACGAA;
PKLR-2R:AACAGCTATGACCATGAAGAAGCACCTCAAGAAATACCA;
PKLR-3-4-5F:TGTAAAACGACGGCCAGTGGGTTGCATCAGGGAATAAA;
PKLR-3-4-5R:AACAGCTATGACCATGGCCAAGGAGAAGGGAATGTG;
PKLR-6-7F:TGTAAAACGACGGCCAGTGACTATGGGTGGGTCGTTTCT;
PKLR-6-7R:AACAGCTATGACCATGCACCCACAGGTGTCCCTAAAA;
PKLR-8-9F:TGTAAAACGACGGCCAGTGTGTGGGTGTCAGAGAAGTAGC;
PKLR-8-9R:AACAGCTATGACCATGTGGCATTCTGTCTCTCCTGG;
PKLR-10F:TGTAAAACGACGGCCAGTGTGACACCTGGAACTGGAACA;
PKLR-10R:AACAGCTATGACCATGGACCACAGGAGAGAGGCAAG;
PKLR-11F:TGTAAAACGACGGCCAGTGCCAGGCTGGTCTCAAACT;
PKLR-11R:AACAGCTATGACCATGATGAGAATGGGAGACTGTGGA;
M13F:TGTAAAACGACGGCCAGT;
M13R:AACAGCTATGACCATG。
进一步地,PKLR-1F:PKLR-1R、PKLR-2F:PKLR-2R、PKLR-3-4-5F:PKLR-3-4-5R、PKLR-6-7F:PKLR-6-7R、PKLR-8-9F:PKLR-8-9R、PKLR-10F:PKLR-10R,或PKLR-11F:PKLR-11R的比值均为1。
进一步地,M13F:M13R的比值为1。
进一步地,所述检测体系PCR扩增反应液还包括2×PCR Buffer、dNTPs和KOD FX DNA Polymerase。
进一步地,所述测序体系反应液还包括测序纯化液、牛小肠碱性磷酸酶、EDTA、无水乙醇、75%乙醇、HIDI和Bigdye Terminator V3.1。
进一步地,所述测序纯化液包括核酸外切酶I、牛小肠碱性磷酸酶。
进一步地,所述试剂盒还包括阳性对照品、阴性对照品和空白对照品。
进一步地,所述试剂盒在辅助检测丙酮酸激酶缺乏症中的应用。
进一步地,引物序列PKLR-1F和PKLR-1R是扩增PKLR基因第1号外显子序列的引物,引物序列PKLR-2F和PKLR-2R是扩增PKLR基因第2号外显子序列的引物,引物序列PKLR-3-4-5F和PKLR-3-4-5R是扩增PKLR基因第3、4和5号外显子序列的引物,引物序列PKLR-6-7F和PKLR-6-7R是扩增PKLR基因第6、7号外显子序列的引物,引物序列PKLR-8-9F和PKLR-8-9R是扩增PKLR基因第8、9号外显子序列的引物,引物序列PKLR-10F和PKLR-10R是扩增PKLR基因第10号外显子序列的引物,引物序列PKLR-11F和PKLR-11R是扩增PKLR基因第11号外显子序列的引物。
有益效果:(1)本发明设计了扩增PKLR基因全部11个外显子序列的引物,通过加接头,使所有7对引物的PCR产物均可以用一对测序引物进行测序,而现有的测序技术要对每种扩增产物设计特异性的测序引物,这就需要设计7条测序引物(单向测序)或14条测序引物(双向测序),因此,本发明所述引物既能将所述PKLR全外显子序列都扩增出来,也保证无论这些外显子的何处位置发生突变,都不会出现漏检的情况;(2)在设计引物时,通过让PKLR基因的第3、4和5号外显子共用一对引物,让PKLR基因的第6和7号外显子共用一对引物,让PKLR基因的第8和9号外显子共用一对引物,显著降低扩增引物的数量,这也会降低扩增产物的数量,从而降低测序引物的数量,因而极大地降低检测成本;(3)本发明采用PCR技术,通过调整引物浓度、退火温度等反应条件,可使扩增效率达到最佳;(4)常用的荧光定量PCR法要针对PKLR基因全部11个外显子可能发生突变的众多突变位点设计多个探针,因此,在11个外显子中,假设每个外显子存在3个突变位点,则要设计33个探针,检测成本显著增加,而本发明通过给设计的扩增引物添加接头,仅需使用一对测序引物就可检测这33个突变位点以及还未被发现的其他突变类型,从而使得检测成本显著降低。
附图说明
图1为PKLR基因在染色体上的定位图。
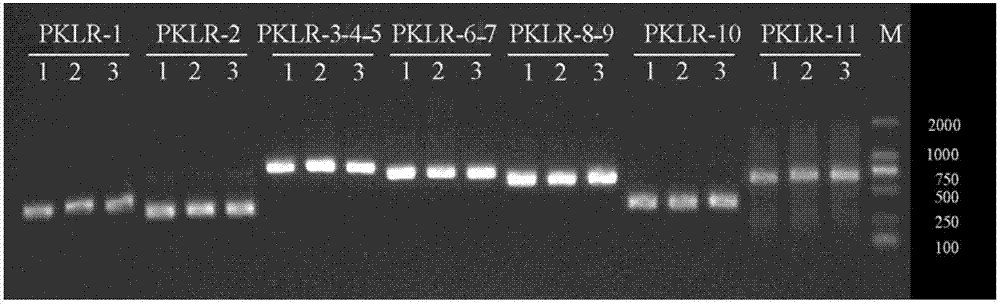
图2为PKLR-1F/PKLR-1R、PKLR-2F/PKLR-2R、PKLR-3-4-5F/PKLR-3-4-5R、PKLR-6-7F/PKLR-6-7R、PKLR-8-9F/PKLR-8-9R、PKLR-10F/PKLR-10R、PKLR-11F/PKLR-11R的电泳图。
图3、4、5、6、7、8、9分别为样本1的PKLR基因第1、2、3/4/5、6/7、8/9、10、11号外显子野生型测序截图。
具体实施方式
下面结合具体实施例和附图,进一步阐述本发明。应当注意的是,实施例中未说明的常规条件和方法,通常按照所属领域实验人员常规采用方法:譬如,奥斯柏和金斯顿主编的《精编分子生物学实验指南》第四版,或者按照制造厂商所建议的步骤和条件。
实施例1
一种检测PKLR基因多态突变位点的寡核苷酸,该寡核苷酸是针对PKLR基因至少一个外显子所设计的,包括至少一对扩增引物,所述至少一对扩增引物选自PKLR-1F/PKLR-1R、PKLR-2F/PKLR-2R、PKLR-3-4-5F/PKLR-3-4-5R、PKLR-6-7F/PKLR-6-7R、PKLR-8-9F/PKLR-8-9R、PKLR-10F/PKLR-10R,或PKLR-11F/PKLR-11R,其碱基序列为:
PKLR-1F:TGTAAAACGACGGCCAGTAGAGGAAATGCCAGGAGATGA;
PKLR-1R:AACAGCTATGACCATGTTCACCCTCATTTTCCTCCTAT;
PKLR-2F:TGTAAAACGACGGCCAGTAGAGGGTATGCTGAGAGACGAA;
PKLR-2R:AACAGCTATGACCATGAAGAAGCACCTCAAGAAATACCA;
PKLR-3-4-5F:TGTAAAACGACGGCCAGTGGGTTGCATCAGGGAATAAA;
PKLR-3-4-5R:AACAGCTATGACCATGGCCAAGGAGAAGGGAATGTG;
PKLR-6-7F:TGTAAAACGACGGCCAGTGACTATGGGTGGGTCGTTTCT;
PKLR-6-7R:AACAGCTATGACCATGCACCCACAGGTGTCCCTAAAA;
PKLR-8-9F:TGTAAAACGACGGCCAGTGTGTGGGTGTCAGAGAAGTAGC;
PKLR-8-9R:AACAGCTATGACCATGTGGCATTCTGTCTCTCCTGG;
PKLR-10F:TGTAAAACGACGGCCAGTGTGACACCTGGAACTGGAACA;
PKLR-10R:AACAGCTATGACCATGGACCACAGGAGAGAGGCAAG;
PKLR-11F:TGTAAAACGACGGCCAGTGCCAGGCTGGTCTCAAACT;
PKLR-11R:AACAGCTATGACCATGATGAGAATGGGAGACTGTGGA。
所述寡核苷酸还包括一对测序引物M13F和M13R,其碱基序列为:
M13F:TGTAAAACGACGGCCAGT;
M13R:AACAGCTATGACCATG。
一种检测PKLR基因突变的试剂盒,包括检测体系PCR扩增反应液和测序体系反应液,其中,
检测体系PCR扩增反应液包括:2×PCR Buffer(10.0μL);dNTPs(2mM);KOD FX DNA Polymerase(1U/μl);PKLR基因11个外显子的上、下游引物PKLR-1F(10μM)、PKLR-1R(10μM)、PKLR-2F(10μM)、PKLR-2R(10μM)、PKLR-3-4-5F(10μM)、PKLR-3-4-5R(10μM)、PKLR-6-7F(10μM)、PKLR-6-7R(10μM)、PKLR-8-9F(10μM)、PKLR-8-9R(10μM)、PKLR-10F(10μM)、PKLR-10R(10μM)、PKLR-11F(10μM)、PKLR-11R(10μM)。
测序体系反应液包括:测序纯化液(核酸外切酶I:0.6U,牛小肠碱性磷酸酶:1.2U);EDTA(125mM);无水乙醇;75%乙醇;HIDI(高度去离子甲酰胺);一对测序引物M13F(3.2μM)、M13R(3.2μM);Bigdye Terminator V3.1(购买自美国Applied Biosystems公司)。
优选地,该试剂盒还包括血液DNA抽提试剂。
优选地,该试剂盒还包括阳性对照品、阴性对照品和空白对照品。阳性对照品为含有人PKLR基因外显子DNA的溶液,严禁反复冻融。阴性对照品为ddH2O。空白对照品为2μl生理盐水或不加任何物质。
实施例2血液样本DNA抽提
血液样本DNA抽提(根据天根生物血液/细胞/组织基因DNA提取试剂盒说明书):抽提人血液样本DNA,具体抽提方法如下:
(1)抽取300μl血液加入900μl红细胞裂解液,颠倒混匀,室温放置5分钟,期间再颠倒混匀几次。12000rpm离心1min,吸去上清,留下白细胞沉淀,加200μl缓冲液GA,振荡至彻底混匀;
(2)加入20μl蛋白酶K溶液,混匀;
(3)加入200μl缓冲液GB,充分颠倒混匀,70℃放置10分钟,溶液应变清亮,简短离心以去除管盖内壁的水珠;
(4)加入200μl无水乙醇,充分振荡混匀15秒,此时可能会出现絮状沉淀,简短离心以去除管盖内壁的水珠;
(5)将上一步所得溶液和絮状沉淀都加入一个吸附柱CB3中(吸附柱放入收集管中),12000rpm离心30秒,倒掉废液,将吸附柱CB3放回收集管中;
(6)向吸附柱CB3中加入500μl缓冲液GD(使用前请先检查是否已加入无水乙醇),12000rpm离心30秒,倒掉废液,将吸附柱CB3放入收集管中;
(7)向吸附柱CB3中加入700μl漂洗液PW(使用前请先检查是否已加入无水乙醇),12000rpm离心30秒,倒掉废液,将吸附柱CB3放入收集管中;
(8)向吸附柱CB3中加入500μl漂洗液PW,12000rpm离心30秒,倒掉废液;
(9)将吸附柱CB3放回收集管中,12000rpm离心2分钟,倒掉废液,将吸附柱CB3置于室温放置数分钟,以彻底晾干吸附材料中残余的漂洗液;
(10)将吸附柱CB3转入一个干净的离心管中,向吸附膜的中间部位悬空滴加100μl洗脱缓冲液TE,室温放置2~5分钟,12000rpm离心2分钟,将溶液收集到离心管中。
实施例3样本DNA扩增
按照实施例2抽提的血液样本DNA,然后利用实施例1中的扩增引物扩增人PKLR基因外显子,获得扩增产物。扩增时在常规PCR仪上进行,可用仪器包括ABI veriti(美国Applied Biosystems公司)等。详情如下所示:
(i)按样品数n(样品数=待测样本数+阴性对照1个+阳性对照1个+空白对照1个)取测体系PCR扩增反应液,每管19μL分装于反应管中;
(ii)将上述处理好的待测样本和阴性对照品、阳性对照品各取1μL分别加入反应管中,混匀,低速离心数秒,进行PCR扩增,获得扩增产物。测体系PCR扩增反应液配制方法如表1所示。PCR扩增扩增反应条件如表2所示。每对扩增引物的详细信息如表3所示。
表1.测体系PCR扩增反应液配制
注:表中的PrimerF和PrimerR选自PKLR-1F/PKLR-1R、PKLR-2F/PKLR-2R、PKLR-3-4-5F/PKLR-3-4-5R、PKLR-6-7F/PKLR-6-7R、PKLR-8-9F/PKLR-8-9R、PKLR-10F/PKLR-10R,或PKLR-11F/PKLR-11R。
表2.PCR扩增反应条件
表3.每对扩增引物信息
实施例4 Sanger测序
取9μl实施例3中的扩增产物和2μl实施例1中的测序纯化液按照表4中所述的程序进行纯化,从而获得纯化产物。
表4纯化程序
将1μl所获得的纯化产物分别与实施例1中的测序引物M13F(3.2μM)、M13R(3.2μM)按照表5中的体系进行混合,然后按照表6中的测序反应程序进行测序。
表5
表6.测序反应程序
沉淀环节:
向完成测序反应的产物中加入2μl 125mM的EDTA,静置5min;加入15l无水乙醇,漩涡混匀;3700rpm离心30min;倒置离心15sec,加入50l 70%乙醇,漩涡混匀;3700rpm离心15min;倒置离心15sec,置于95℃金属浴上;加入10μl HIDI后进行变性试验。变性试验步骤为:95℃,5min;接着在-30℃2min,然后在4℃保存。
变性程序结束后,上测序仪(ABI3730)测序。
结果判断:
分别将测序结果与PKLR野生型参考序列(Genbank accn:NC_000001.11)进行比对,根据实际突变情况对结果进行报告。
实施例5临床样本检测
取3例临床血液样本(样本编号为1~3)先后按照实施例1、实施例2、实施例3和实施例4,配制试剂、抽提样本DNA、扩增(获得扩增产物)和测序。每份样本往检测体系PCR反应液中加入1μl。
利用所获得的扩增产物,开展DNA电泳,电泳条件为1.5%琼脂糖凝胶电泳,110V,25min,凝胶成像系统观察。电泳结果如图2所示。
图2为这3例血液样本以PKLR-1F/PKLR-1R、PKLR-2F/PKLR-2R、PKLR-3-4-5F/PKLR-3-4-5R、PKLR-6-7F/PKLR-6-7R、PKLR-8-9F/PKLR-8-9R、PKLR-10F/PKLR-10R和PKLR-11F/PKLR-11R等7对扩增引物扩增后所得扩增产物的电泳图谱,M为Marker DL 2000,1~3为送检的血液样本编号1~3号。这6对引物扩增的片段长度分别为335bp、322bp、838bp、766bp、662bp、373bp、644bp,通过电泳图的分析表明这7对引物扩增有效,且条带单一。
在这3例样品中,以样本1为例进行详细说明。样本1的测序结果如图3-9所示。
图3显示是样本1的PKLR基因第1号外显子野生型测序截图,说明样本1的1号外显子未发生突变。
图4显示是样本1的PKLR基因第2号外显子野生型测序截图,说明样本1的2号外显子未发生突变。
图5显示是样本1的PKLR基因第3、4、5号外显子野生型测序截图,说明样本1的3、4、5号外显子未发生突变。
图6显示是样本1的PKLR基因第6、7号外显子野生型测序截图,说明样本1的6、7号外显子未发生突变。
图7显示是样本1的PKLR基因第8、9号外显子野生型测序截图,说明样本1的8、9号外显子未发生突变。
图8显示是样本1的PKLR基因第10号外显子野生型测序截图,说明样本1的10号外显子未发生突变。
图9显示是样本1的PKLR基因第11号外显子野生型测序截图,说明样本1的11号外显子未发生突变。
从检测结果可以看出,本发明所述引物已经把PKLR基因共11个外显子序列包括在内了,能够扩展出PKLR基因全部11个外显子,并且测序结果完全准确。由检测结果可知,样本1的11个外显子均为野生型。另外,对PKLR基因外显子突变阳性样本的检测也表明本发明的寡核苷酸、方法和试剂盒能够检测出PKLR基因外显子突变的突变情况。
SEQUENCE LISTING
<110> 杭州艾迪康医学检验中心有限公司
<120> 检测PKLR基因突变的方法、试剂盒、寡核苷酸及其应用
<130>
<160> 16
<170> PatentIn version 3.5
<210> 1
<211> 39
<212> DNA
<213> 人工序列
<400> 1
tgtaaaacga cggccagtag aggaaatgcc aggagatga 39
<210> 2
<211> 38
<212> DNA
<213> 人工序列
<400> 2
aacagctatg accatgttca ccctcatttt cctcctat 38
<210> 3
<211> 40
<212> DNA
<213> 人工序列
<400> 3
tgtaaaacga cggccagtag agggtatgct gagagacgaa 40
<210> 4
<211> 39
<212> DNA
<213> 人工序列
<400> 4
aacagctatg accatgaaga agcacctcaa gaaatacca 39
<210> 5
<211> 38
<212> DNA
<213> 人工序列
<400> 5
tgtaaaacga cggccagtgg gttgcatcag ggaataaa 38
<210> 6
<211> 36
<212> DNA
<213> 人工序列
<400> 6
aacagctatg accatggcca aggagaaggg aatgtg 36
<210> 7
<211> 39
<212> DNA
<213> 人工序列
<400> 7
tgtaaaacga cggccagtga ctatgggtgg gtcgtttct 39
<210> 8
<211> 37
<212> DNA
<213> 人工序列
<400> 8
aacagctatg accatgcacc cacaggtgtc cctaaaa 37
<210> 9
<211> 40
<212> DNA
<213> 人工序列
<400> 9
tgtaaaacga cggccagtgt gtgggtgtca gagaagtagc 40
<210> 10
<211> 36
<212> DNA
<213> 人工序列
<400> 10
aacagctatg accatgtggc attctgtctc tcctgg 36
<210> 11
<211> 39
<212> DNA
<213> 人工序列
<400> 11
tgtaaaacga cggccagtgt gacacctgga actggaaca 39
<210> 12
<211> 36
<212> DNA
<213> 人工序列
<400> 12
aacagctatg accatggacc acaggagaga ggcaag 36
<210> 13
<211> 37
<212> DNA
<213> 人工序列
<400> 13
tgtaaaacga cggccagtgc caggctggtc tcaaact 37
<210> 14
<211> 37
<212> DNA
<213> 人工序列
<400> 14
aacagctatg accatgatga gaatgggaga ctgtgga 37
<210> 15
<211> 18
<212> DNA
<213> 人工序列
<400> 15
tgtaaaacga cggccagt 18
<210> 16
<211> 16
<212> DNA
<213> 人工序列
<400> 16
aacagctatg accatg 16
- 还没有人留言评论。精彩留言会获得点赞!