一种黄色长余辉发光材料及其制备方法与流程
本发明属于发光材料技术领域,涉及一种黄色长余辉发光材料,具体涉及经紫外光或可见光照射后,可发出持续可见黄色余辉的黄色长余辉发光材料;本发明还涉及一种该发光材料的制备方法。
背景技术:
长余辉发光材料是一类光致发光材料,经日光和长波紫外线等光源的短时间照射后,将一部分光能储存,关闭光源后,仍能在很长一段时间内持续缓慢地以可见光的形式释放这部分能量。长余辉发光材料的用途十分广泛,除作为夜光标志材料外,如用于紧急通道照明、火险的指示牌等其他需要弱照明指示设备上,即节能又环保,还可以应用于光电信息领域(高能粒子和缺陷损伤探测器,三维信息存储等)。传统的长余辉材料主要有硫化锌和硫化钙荧光体。自20世纪90年代以来,Eu2+铝酸盐体系和硅酸盐体系成为长余辉发光材料的主体,这两类长余辉发光材料在发光亮度、余辉时间、化学稳定性方面都优于传统硫化物体系的长余辉材料。这两类长余辉发光材料的发光颜色一般为绿色、蓝色、蓝绿色。长余辉发光材料中的长波发射长余辉材料,具有特殊的光学性质,在弱光照明和应急指示中具有比蓝、绿色短波长余辉材料更广阔的应用前景。但Eu2+铝酸盐体系和硅酸盐体系长余辉发光材料中只有少量的发黄光和红光的长余辉材料,且和其他商业性长余辉材料相比,大多数具有化学稳定性差,发光强度低和持续时间短的特点,难以满足实际需要。因此,研究一种新型的有效黄色长余辉材料非常有必要。此外,磷酸盐是一种很好的基质,稀土磷酸盐发光材料具有合成温度低的特点;其以独居石、磷钇矿等天然矿物的状态存在于自然界中,这决定了它非常稳定的化学性质;同时磷酸盐基质本身具有价廉、无毒、无污染、基质吸收带位于较短波长等优点。专利《橙黄色长余辉发光材料及生产方法》(申请号ZL200410020722.X,公告号CN1266250,公告日2006.07.26)和专利《红色稀土长余辉磷光体》(专利号ZL02125512.1,公告号CN1216125,公告日2005.08.24)公开了以硫化物为基质的长余辉发光材料,但这些长余辉发光材料的制备工艺比较复杂,而且制备过程中容易产生含硫的有害气体,会对人体和环境造成危害。专利《橙黄色长余辉荧光粉及其制备方法》(专利号200710056035.7,公告号CN100575452,公告日2009.12.30)公开了以Eu2+为激活离子的橙黄色长余辉发光材料SrSiO5:Eu2+,Dy3+,该材料在制备时需要较高的温度,一方面浪费能源,另一方面增加了材料的制造成本。专利《一种黄色长余辉发光材料及其制备方法》(申请号201410192345.1,公告号CN103952152A,公告日2014.07.30)公开了以Eu2+为激活离子的黄色长余辉发光材料Ba3-x-yP4O13:Eux,Gay,该材料的余辉时间较短,不利于产业化的应用。
技术实现要素:
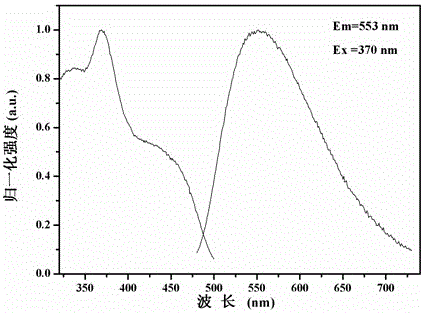
本发明的目的是提供一种新型黄色长余辉发光材料,在200nm~500nm波长光激发后能产生黄色长余辉,而且余辉时间较长。本发明的另一个目的是提供上述黄色长余辉发光材料的制备方法,采用较低的温度,节约能源,降低材料的制造成本。为实现上述目的,本发明所采用的技术方案是:一种黄色长余辉材料,化学表达式为Ca6-x-yBaP4O17:Eux,Ry;其中,0.005≤x≤0.08,0≤y≤0.12;R=Tb、Ce、Dy、Tm、Nd、Gd、Y、Er、La、Pr、Sm、Yb、Lu、Mn或Ho中的一种。本发明所采用的另一个技术方案是:一种上述黄色长余辉发光材料的制备方法,具体按以下步骤进行:步骤1:按Ca6-x-yBaP4O17:Eux,Ry化学表达式中各化学组成的化学计量比,分别称取以下原料:NH4H2PO4和Eu2O3,Tb2O3、CeO2、Dy2O3、Tm2O3、Nd2O3、Gd2O3、Y2O3、Er2O3、La2O3、Pr6O11、Sm2O3、Yb2O3、Lu2O3、MnCO3或Ho2O3中的一种,BaCO3和CaCO3,Ba和Ca的摩尔比为3︰17;将所取各原料组份研磨至微米级,制得原料粉末;步骤2:将步骤1制得的原料粉末置于温度为1200℃~1400℃的环境中,在还原气氛下煅烧9~12小时;步骤3:将煅烧后的原料粉末随炉冷却至室温,得到煅烧物;步骤4:将步骤3得到的煅烧物进行研磨,制得黄色长余辉发光材料。本发明制备方法采用低温煅烧,200nm~500nm波长光激发后能发出明亮黄色的长余辉发光材料,具有制备方法简单、无污染、成本低;发光强度高,余辉持续时间长等优点。附图说明图1是实施例1制得的长余辉发光材料的XRD图谱。图2是实施例1制得的长余辉发光材料的激发和发射光谱图。图3是实施例1制得的长余辉发光材料在激发停止2分钟和8分钟时的余辉光谱图。图4是实施例1制得的长余辉发光材料的余辉衰减曲线图。具体实施方式下面结合附图和具体实施方式对本发明进行详细说明。本发明黄色长余辉材料的化学表达式为Ca6-x-yBaP4O17:Eux,Ry;其中,0.005≤x≤0.08,0≤y≤0.12;R=Tb、Ce、Dy、Tm、Nd、Gd、Y、Er、La、Pr、Sm、Yb、Lu、Mn或Ho。该黄色长余辉材料的制备方法,具体按以下步骤进行:步骤1:按该黄色长余辉发光材料化学表达式中各化学组成的化学计量比分别称取以下原料:NH4H2PO4和Eu2O3,Tb2O3、CeO2、Dy2O3、Tm2O3、Nd2O3、Gd2O3、Y2O3、Er2O3、La2O3、Pr6O11、Sm2O3、Yb2O3、Lu2O3、MnCO3或Ho2O3中的一种,BaCO3和CaCO3,为了补偿煅烧过程中的挥发,在CaCO3用量不变的前提下,适当增加BaCO3的用量,使Ba和Ca的摩尔比为3︰17;将所取各原料组份研磨至微米级,制得原料粉末;步骤2:将步骤1制得的原料粉末置于温度为1200℃~1400℃的环境中,在还原气氛下煅烧9~12小时;还原气氛可以采用三种气体:第一种是氨气(NH3);第二种是按体积百分比由5~25%氢气(H2)和95~75%氮气(N2)组成的混合气体;第三种是按体积百分比由5~25%一氧化碳(CO)和95~75%氮气(N2)组成的混合气体;步骤3:将煅烧后的原料粉末随炉冷却至室温,得到煅烧物;步骤4:将步骤3得到的煅烧物进行研磨,制得黄色长余辉发光材料。Ca6BaP4O17是一种新的发光材料的基质,由于具有低的合成温度,合成过程中无污染,大的带隙和高的化学稳定性,且可以给Eu2+提供一种合适的晶体场环境。在该基质中加入激活离子Eu2+和共激活离子Tb3+等三价稀土离子共激活剂,能够实现理想的黄色长余辉发光特性。按照L.G.VANUITERT的经验公式,Eu2+的发光波长与其晶体场环境有如下关系:E是在晶体场中离子发射波长对应的波数,Q为自由离子发射波长对应的波数,V为价态,n为配位数,ea是电子亲合力,r是Eu2+离子的半径,λ为Eu2+离子发光的波长。通过简单的计算即可得出,Eu2+作为发光中心,在占据Ca2+的位置后可以产生峰值在553nm的黄光发射。而R主要是作为陷阱中心,捕获导带中的电子。在200nm~500nm波长光激发后,电子从价带被激发到导带,一部分电子通过Eu2+离子产生发光,并返回价带,另一部分电子被R产生的电子陷阱所捕获。当停止激发后,在室温的热扰动下,被捕获的电子缓慢地逃逸出电子陷阱的束缚,重新回到导带,再通过Eu2+产生持久的黄色余辉,并最终返回价带。采用本发明方法合成的黄色长余辉发光材料以Eu2+作为激活离子,Tb3+等三价稀土离子作为共激活离子,采用低温煅烧。在200nm~500nm波长光激发下,发出波长为470nm~750nm的黄光,该黄光宽带发射的峰值位于553nm,经紫外光照射后,去掉激发源,人眼可以观察到明亮的黄色余辉,余辉的初始亮度最高可达到0.8865cd/m2,能持续发出人眼可分辨的发光亮度在0.32mcd/m2以上的可见光近19小时。实施例1按Ca5.965BaP4O17:0.02Eu2+,0.015Gd3+分子式所示的化学计量比,分别称取NH4H2PO4、Eu2O3,CaCO3、BaCO3和Gd2O3,在CaCO3用量不变的前提下,使Ba和Ca的摩尔比为3︰17;将所取各原料组份研磨至微米级制得原料粉末;将该原料粉末置于温度为1200℃的环境中,在还原气氛下煅烧12小时;还原气氛由体积百分比5%的氢气和95%的氮气组成;将煅烧后的原料粉末随炉冷却至室温,得到煅烧物;研磨,制得黄色长余辉发光材料。图1所示为该黄色长余辉发光材料的XRD图谱,表明该黄色长余辉发光材料的物相为Ca6BaP4O17,没有其他的杂质相产生。该长余辉发光材料的激发和发射光谱图如图2所示,图中显示该长余辉发光材料发射光谱为宽带发射,峰值位于553nm附近,归属于Eu2+的4f65d1→4f7跃迁,采用CIE色度图计算得到该长余辉发光材料发射光的色坐标为x=0.43,y=0.54,位于黄光发射区域。从图2所示的发光材料的发射光谱和图3所示的发光材料的余辉光谱及计算出来的色坐标(0.43,0.54),可以说明制得的长余辉发光材料是黄色长余辉发光材料。长波发射材料是相对于性能优异的蓝绿色长余辉材料而言的,蓝光长余辉材料的发射主峰一般位于480nm以下,绿光长余辉材料的发射主峰一般位于500nm~540nm之间,而本发明的长余辉材料的发射主峰位于553nm,所以说本发明的长余辉材料是长波发射材料。用紫外灯照射,在停止照射后1分钟和8分钟时该发光材料的余辉光谱图如图3所示。暗处观察,材料呈现黄色余辉发光。图4为该发光材料的余辉衰减曲线图,从图中可看出,该发光材料能够持续发出近19小时的人眼可分辨的发光亮度在0.32mcd/m2以上的可见光。实施例2按Ca5.915BaP4O17:0.005Eu2+,0.08La3+分子式所示的化学计量比,分别称取CaCO3、BaCO3、NH4H2PO4、Eu2O3和La2O3,为了补偿煅烧过程中的挥发,在CaCO3用量不变的前提下,使Ba和Ca的摩尔比为3︰17,将称取的各原料研磨混合均匀后放入氧化铝坩埚,置于温度为1250℃的环境中,在氨气气氛下煅烧11小时,煅烧后的原料粉末随炉冷却至室温,得到煅烧物;研磨后,制得黄色长余辉发光材料。实施例3按Ca5.9825BaP4O17:0.01Eu2+,0.0075Tb3+分子式所示的化学计量比,分别称取CaCO3、BaCO3、NH4H2PO4、Eu2O3和Tb2O3,为了补偿煅烧过程中的挥发,在CaCO3用量不变的前提下,使Ba和Ca的摩尔比为3︰17,将称取的各原料研磨混合均匀后放入氧化铝坩埚,置于温度为1350℃的环境中,在还原气氛下煅烧9小时,还原气氛由体积百分比为15%一氧化碳和85%氮气组成,煅烧后的原料粉末随炉冷却至室温,得到煅烧物;研磨后,制得黄色长余辉发光材料。实施例4按Ca5.965BaP4O17:0.02Eu2+,0.06Tm3+分子式所示的化学计量比,分别取CaCO3、BaCO3、NH4H2PO4、Eu2O3和Tm2O3,为了补偿煅烧过程中的挥发,在CaCO3用量不变的前提下,使Ba和Ca的摩尔比为3︰17,将称取的各原料研磨混合均匀后放入氧化铝坩埚,置于温度为1280oC的环境中,还原气氛下煅烧10小时,还原气氛由体积百分比为75%的氮气和25%的氢气组成,煅烧后的原料粉末随炉冷却至室温,得到煅烧物。研磨后,制得黄色长余辉发光材料。实施例5按Ca5.995BaP4O17:0.005Eu2+分子式所示的化学计量比,分别取CaCO3、BaCO3、NH4H2PO4和Eu2O3,为了补偿煅烧过程中的挥发,在CaCO3用量不变的前提下,使Ba和Ca的摩尔比为3︰17,将该原料粉末置于温度为1400℃的环境中,在还原气氛下煅烧9小时;还原气氛由体积百分比15%的氢气和25%的氮气组成;将煅烧后的原料粉末随炉冷却至室温,得到煅烧物;研磨,制得黄色长余辉发光材料。实施例6按Ca5.8BaP4O17:0.08Eu2+,0.12Dy3+分子式所示的化学计量比,分别取CaCO3、BaCO3、NH4H2PO4、Eu2O3和Dy2O3,在CaCO3用量不变的前提下,使Ba和Ca的摩尔比为3︰17;将所取各原料组份研磨至微米级制得原料粉末;将该原料粉末置于温度为1300℃的环境中,在还原气氛下煅烧10.5小时;还原气氛由体积百分比5%的一氧化碳和95%的氮气组成;将煅烧后的原料粉末随炉冷却至室温,得到煅烧物;研磨,制得黄色长余辉发光材料。实施例7按Ca5.8575BaP4O17:0.0425Eu2+,0.1Mn2+分子式所示的化学计量比,分别取CaCO3、BaCO3、NH4H2PO4、Eu2O3和MnCO3,在CaCO3用量不变的前提下,使Ba和Ca的摩尔比为3︰17;将所取各原料组份研磨至微米级制得原料粉末;将该原料粉末置于温度为1380℃的环境中,在还原气氛下煅烧9.5小时;还原气氛由体积百分比25%的一氧化碳和75%的氮气组成;将煅烧后的原料粉末随炉冷却至室温,得到煅烧物;研磨,制得黄色长余辉发光材料。实施例8按Ca5.952BaP4O17:0.008Eu2+,0.05Nd3+分子式所示的化学计量比,分别取CaCO3、BaCO3、NH4H2PO4、Eu2O3和Nd2O3,然后按实施例1的方法制得黄色长余辉发光材料。实施例9按Ca5.92BaP4O17:0.06Eu2+,0.02Ce3+分子式所示的化学计量比,分别取CaCO3、BaCO3、NH4H2PO4、Eu2O3和CeO2,然后按实施例2的方法制得黄色长余辉发光材料。实施例10按Ca5.89BaP4O17:0.01Eu2+,0.1Y3+分子式所示的化学计量比,分别取CaCO3、BaCO3、NH4H2PO4、Eu2O3和Y2O3,然后按实施例3的方法制得黄色长余辉发光材料。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1