一种阪崎肠杆菌的LAMP引物组及试剂盒与使用方法与流程
技术领域:
本发明属于食品安全的分子生物学检测方法领域,特别涉及一种阪崎肠杆菌的LAMP引物组及试剂盒与使用方法。
背景技术:
:
阪崎肠杆菌(Enterobacter sakazakii)是人和动物肠道内寄生的一种革兰氏阴性无芽孢杆菌,属肠杆菌科。2002年国际食品微生物标准化委员会(ICMSF)把阪崎肠杆菌列为“严重危害特定人群,危害生命或慢性实质性后遗症或长期硬性”的一种致病菌。阪崎肠杆菌可以对任何年龄段的人群引起疾病,成人患病则明显轻微。但对1岁以下,特别是出生28d以内、早产儿、低体重儿或免疫缺陷的婴幼儿更容易被感染。能引起严重的新生儿脑膜炎、小肠结肠炎,并可能引起神经功能紊乱,造成严重的后遗症和死亡。婴儿配方奶粉是其主要的传播途径,而且婴儿配方奶粉中微量的阪崎肠杆菌污染(<3CFU/100g)也能导致感染的发生。
目前对阪崎肠杆菌的检测方法主要有传统检测方法和分子检测方法。传统检测实验步骤繁琐,检出时间长达6~7d,而且可操作性差;随着分子生物学的发展,越来越多的分子检测技术用于阪崎肠杆菌的检测,如免疫学法和实时PCR。免疫学方法具有操作简单、实验成本低的特点,通过制备克隆抗体的方式对传统检测提供辅助,但具有易发生交叉反应的缺点,特异性和灵敏度均不理想;实时PCR方法敏感、快速,但由于需要昂贵的仪器设备以及对操作人员的专业水平要求高,使其难以在基层普及和推广。
环介导等温扩增(loop-mediated isothermal amplification,LAMP),是2000年日本荣研化学株式会的Notomi等开发的一种新的核酸扩增方法。LAMP法是针对靶基因的6个区域设计4种特异的引物,利用一种链置换DNA聚合酶(Bst DNA ploypolymerase)在恒温条件下(65℃左右)保温几十分钟,即可完成核酸扩增反应,具有高特异性和等温快速扩增的特点,可以在1小时之内,将靶DNA片段扩增109~1010。因为LAMP技术是针对靶基因的6个区域设计两对引物进行扩增,所以比PCR具有更高的特异性,并且不需要温度改变,实验条件简单,有利于基层机构的现场检测。
技术实现要素:
:
本发明的目的在于提供一种阪崎肠杆菌的LAMP引物组,根据阪崎肠杆菌的16SrRNA基因(ES16S)保守区序列设计环介导等温扩增引物,应用PrimerExplorer V4(http://primerexplorer. jp/elamp4.0.0/index.html)在线设计特异引物组,利用LAMP技术扩增靶基因的特定区域,从分子水平上实现阪崎肠杆菌的快速检测,为阪崎肠杆菌检测提供了有效且快速的核酸筛查检测方法。
本发明的另一目的在于提供上述阪崎肠杆菌的LAMP检测试剂盒及使用方法。
一种阪崎肠杆菌的LAMP引物组,包括一对外引物、一对内引物和一对环引物,其核苷酸序列分别如下所示:
ES16S-F3:GTCACGTTTGAGATATTTGCTC,
ES16S-B3:AACGGTTCATATCACCTTACC;
ES16S-FIP: GTGCTGCGAGTTTGAGAGACTTTGAAACAGACATGCTGCT,
ES16S-BIP:TCTTCGGGTTGTGAGGTTAAGCCAGATTAGCACGTCCTTCAT;
ES16S-LF:CGCGCATTTCTTATTACGGAG,
ES16S-LB:CAAGCGTACACGGTGGAT。
上述阪崎肠杆菌的LAMP检测试剂盒,包括以下物质:(1)DNA聚合酶;(2)2×反应缓冲液;(3)荧光染料;(4)密封液;(5)标准阳性模板;(6)阴性对照;(7)上述的LAMP引物组。
在上述LAMP检测试剂盒中,所述LAMP引物组的浓度比例分别为:外引物、内引物、环引物的摩尔比为:1-2:4-8:2-4。
在上述LAMP检测试剂盒中,所述DNA聚合酶为Bst DNA聚合酶.
在上述LAMP检测试剂盒中,所述2×反应缓冲液包括buffer缓冲液、甜菜碱和dNTPs,三者的体积比为10:8:7。
在上述LAMP检测试剂盒中,所述荧光染料为浓度是0.02mM的SYTO-9。
在上述LAMP检测试剂盒中,所述密封液为矿物油。
在上述LAMP检测试剂盒中,所述的标准阳性模板为阪崎肠杆菌标准菌株基因组DNA;阴性对照为灭菌超纯水。
使用上述的LAMP试剂盒检测阪崎肠杆菌的方法,包括以下步骤:
(1)待检样品的提取:采用水煮法从待检样品中提取DNA;
(2)恒温基因扩增检测反应体系及条件:25μl反应体系含有:SAnuc-F3 0.2μM,SAnuc-B3 0.2μM,SAnuc-FIP 0.8μM,SAnuc-BIP 0.8μM,SAnuc-LF 0.4μM,SAnuc-LB 0.4μM,2×反应液12.5μl,DNA聚合酶8U,SYTO-9 0.5μl,待检样品2μl,用超纯水补齐至25μl;密封液加入体积为20μl,同时设置阳性对照和阴性对照;将配置好的PCR管混匀后离心,63℃反应30~45min,并在80℃持续2min;
(3)检测结果判断:将上述反应管置于荧光PCR仪(如ABI stepone、ZYD-S1)中,根据扩增曲线来判断检测结果,扩增曲线呈“S”形,检测结果为阳性,即检测样品中含有阪崎肠杆菌;无“S”形扩增曲线出现,检测结果为阴性,即检测样品不含有阪崎肠杆菌。
与现有技术相比,本发明具有如下有益效果
(1)本发明不需要特殊试剂,不需要预先进行双链DNA的变性,只需一恒定温度就能扩增反应。
(2)高特异性。本发明根据阪崎肠杆菌的16SrRNA基因(ES16S)保守区序列设计六条特异引物,对靶基因6个区域进行特异扩增,特异性强,且与其他菌株无交叉反应。
(3)快速、高效扩增,耗时短。扩增不需要加热变性,省去了热循环步骤,40~60min即可完成扩增反应。并且增加环引物的环介导等温扩增方法,使反应速度可提高1/2~1/3。
(4)鉴定简便。可通过观察扩增曲线直接判断阴阳性,不需要繁琐的电泳等其他任何分析步骤,适合现场检测。
附图说明:
图1为LAMP灵敏性实验结果示意图;其中,从左至右依次为浓度1ng/μl、100pg/μl和10 pg/μl阪崎肠杆菌基因组DNA模板LAMP反应结果。
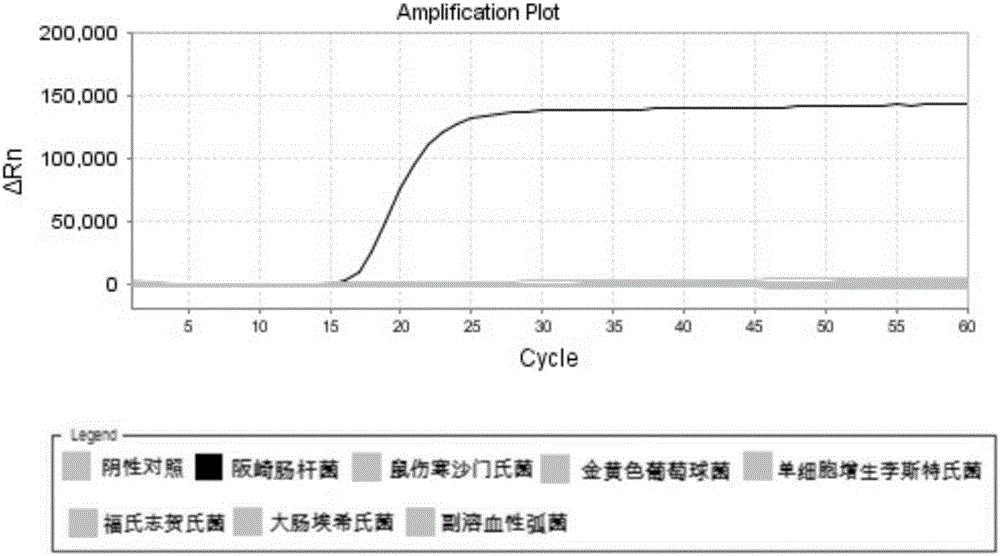
图2为LAMP特异性实验结果示意图;
具体实施方式:
下面结合附图和实施例对本发明做详细的说明,但不应该当作对本发明的限制。
实施例1:一种阪崎肠杆菌的LAMP引物的设计合成和检测试剂盒的建立
(1)LAMP引物的设计合成
根据文献报道,以阪崎肠杆菌ES16S基因作为靶基因,采用引物设计软件Primer Explorer 4.0设计包括环引物在内的6条LAMP引物。引物由生工生物工程(上海)股份有限公司合成,6条引物序列如下所示:
SEQ NO.1:ES16S-F3:GTCACGTTTGAGATATTTGCTC
SEQ NO.2:ES16S-B3:AACGGTTCATATCACCTTACC
SEQ NO.3:ES16S-FIP: GTGCTGCGAGTTTGAGAGACTTTGAAACAGACATGCTGCT
SEQ NO.4:ES16S-BIP:
TCTTCGGGTTGTGAGGTTAAGCCAGATTAGCACGTCCTTCAT
SEQ NO.5:ES16S-LF:CGCGCATTTCTTATTACGGAG
SEQ NO.6:ES16S-LB:CAAGCGTACACGGTGGAT
(2)阪崎肠杆菌LAMP检测试剂盒除包括上述LAMP引物组外,还包括DNA聚合酶、2×反应液、荧光染料、密封液、阳性对照和阴性对照。其中反应液包含buffer缓冲液、甜菜碱和dNTPs,各成分体积比为10:8:7。
(3)检测方法:
1)待检样品的提取:采用水煮法,将样品稀释液煮沸,上清液作为扩增反应DNA模板。
2)恒温基因扩增检测反应体系及条件:25μl反应体系含有:ES16S -F3 0.2μM,ES16S -B3 0.2μM,ES16S -FIP 0.8μM,ES16S -BIP 0.8μM,ES16S -LF 0.4μM,ES16S -LB 0.4μM,2×反应液12.5μl,DNA聚合酶8U,STO-9 0.5μl,待检样品2μl,用超纯水补齐至25μl。密封液加入体积为20μl。同时设置阳性对照和阴性对照。
将配置好的PCR管混匀后离心,63℃反应45~60min,并在80℃持续2min。
3)检测结果判断:将上述反应管置于荧光PCR仪(如ABI stepone、ZYD-S1)中,根据扩增曲线来判断检测结果。扩增曲线呈“S”形,检测结果为阳性,即检测样品中含有阪崎肠杆菌;无“S”形扩增曲线出现,检测结果为阴性,即检测样品不含有阪崎肠杆菌。
实施例2 LAMP灵敏度实验
将阪崎肠杆菌标准菌株接种于营养肉汤,36℃±1℃培养18小时。应用Magen细菌基因DNA提取试剂盒提取培养产物中的细菌DNA。将阪崎肠杆菌标准菌株抽提的DNA进行10倍梯度稀释,分别以1ng/μl、100pg/μl、10pg/μl、1pg/μl、100fg/μl五个梯度浓度DNA作为模板和阴性对照(灭菌超纯水)按照实施例1的反应体系和条件建立检测方法,以确定试剂盒检测方法的灵敏性。
参见图1,结果表明:将阪崎肠杆菌基因组DNA进行10倍梯度稀释后,建立实施例1的阪崎肠杆菌LAMP检测试剂盒可检测样品中10pg/μl的阪崎肠杆菌DNA。
实施例3 LAMP特异性实验
应用实施例1的LAMP检测试剂盒对金黄色葡萄球菌、鼠伤寒沙门氏菌、单细胞增生李斯特氏菌、福氏志贺氏菌、大肠埃希氏菌及副溶血性弧菌进行检测,检测结果如图2所示。设置阪崎肠杆菌基因组DNA为阳性对照,灭菌超纯水为阴性对照。从图2中可以看出,只有阪崎肠杆菌出现阳性结果,其他菌株为阴性结果直至反应时间延长至60min。说明实施例1的LAMP反应体系只对阪崎肠杆菌有特异性。
SEQUENCE LISTING
<110> 中华人民共和国广州机场出入境检验检疫局,暨南大学,广州双螺旋基因技术有限公司
<120> 一种阪崎肠杆菌的LAMP引物组及试剂盒与使用方法
<130>
<160> 6
<170> PatentIn version 3.5
<210> 1
<211> 22
<212> DNA
<213> 人工序列ES16S-F3
<400> 1
gtcacgtttg agatatttgc tc 22
<210> 2
<211> 21
<212> DNA
<213> 人工序列ES16S-B3
<400> 2
aacggttcat atcaccttac c 21
<210> 3
<211> 40
<212> DNA
<213> 人工序列ES16S-FIP
<400> 3
gtgctgcgag tttgagagac tttgaaacag acatgctgct 40
<210> 4
<211> 42
<212> DNA
<213> 人工序列ES16S-BIP
<400> 4
tcttcgggtt gtgaggttaa gccagattag cacgtccttc at 42
<210> 5
<211> 21
<212> DNA
<213> 人工序列ES16S-LF
<400> 5
cgcgcatttc ttattacgga g 21
<210> 6
<211> 18
<212> DNA
<213> 人工序列ES16S-LB
<400> 6
caagcgtaca cggtggat 18
- 还没有人留言评论。精彩留言会获得点赞!