可视化HLA‑B*5801基因分型检测试剂盒的制作方法
本发明属于分子生物技术和基因检测领域,具体是一种HLA-B*5801基因分型检测试剂盒。
背景技术:
别嘌呤醇是治疗痛风的一线药物,是目前惟一的黄嘌呤氧化酶抑制剂。该药可引起严重副反应,包括Stevens-John综合征(SJS)及中毒性表皮坏死症(TEN)。HLA-B*5801等位基因与别嘌呤醇引发的SJS或TEN的强相关性首先由中国台湾学者在汉族人群中发现,并被泰国、新加坡、香港和中国多个研究小组在汉族人群中证实,汉族人中HLA-B*5801等位基因频率为9-15%(呈地域差异)。
研究表明,HLA-B*5801等位基因与别嘌呤醇引发的严重皮炎副反应呈现很强的相关性,尤其在汉族人中高达100%,几乎所有副反应的患者都是HLA-B*5801的携带者,而别嘌呤醇耐受者中只有15%左右的HLA-B*5801携带者,检测HLA-B*5801等位基因可以预防别嘌呤醇引发的SJS或TEN。在2012年美国风湿病学会更新的痛风管理指南中也建议使用别嘌呤醇前,应对严重过敏反应的高危人群,建议进行HLA-B*5801等位基因检测。
然而,由于HLA-B*5801等位基因较为复杂,直接对其检测很不方便。有研究进一步证实,对于亚洲人种,PSORS1C1基因的SNP位点(rs9263726)与HLA-B*5801等位基因存在直接相关性,且相关性达到100%,因此,可以检测与HLA-B*5801等位基因关联的SNP位点来反映携带者是否携带HLA-B*5801等位基因。本项目通过检测PSORS1C1基因的SNP位点(rs9263726)来反映服用别嘌呤醇药物的临床携带者发生SJS/TEN的风险。
目前市场上已有的HLA-B*5801等位基因分型检测试剂盒基本都是基于荧光信号检测的PCR扩增技术,需要用到实时荧光PCR设备,其价格较为昂贵,不利于在设施条件差的医疗单位使用。而同时临床中,至今为止尚未有能够直接采用普通PCR循环仪器就能够实现可视化分型HLA-B*5801等位基因的闭管方法。
技术实现要素:
基于此,本发明的目的为提供一种对设施条件要求低、可视化、成本低廉的新型HLA-B*5801等位基因分型检测试剂盒。
实现上述目的的技术方案如下。
一种可视化HLA-B*5801基因分型检测试剂盒,包括有2条引物,4条常规探针、以及2条与纳米金颗粒连接的探针;
所述2条引物为:SEQ ID NO.1和SEQ ID NO.2;
所述4条常规探针分别为SEQ ID NO.3至SEQ ID NO.6,或所述4条常规探针分别为SEQ ID NO.3至SEQ ID NO.6的反向互补序列;
所述2条与纳米金颗粒连接的探针的碱基组成如SEQ ID NO.7至SEQ IDNO.8所示,或SEQ ID NO.7至SEQ ID NO.8的反向互补序列所示。
本发明利用了基于纳米金探针的可视化核酸检测技术,在将高灵敏的PCR扩增方法、高特异的酶切方法及可视化的纳米金探针检测方法相结合,构建了可视化HLA-B*5801基因分型检测试剂盒,可用于HLA-B*5801基因分型的可视化检测,实现低成本、高灵敏的HLA-B*5801基因分型检测。通过检测患者基因组DNA中的SNP位点(rs9263726)单核苷酸多态性位点,判定该患者的HLA-B*5801基因编码酶的药物代谢速率类型,并根据携带者的等位基因类型辅助医生对别嘌呤醇用药的不良反应发生风险进行评价,指导携带者的安全用药,为临床提供一种新型检测方法。
本发明具有以下有益效果。
采用本发明中的试剂盒对HLA-B*5801基因SNP位点进行分型检测无需使用荧光探针,试剂存放无需避光,不必担心荧光衰减的问题,因此存放条件更加稳定。
本发明采用的纳米金探针有比较成熟的方法合成,成本低;具备高稳定性,能够耐受强热循环和强机械冲击;具备强适用性,能够与各种酶反应液共存而不影响反应的正常进行。
利用本发明中的试剂盒可实现短时间高灵敏度的闭管核酸检测,能够有效的避免扩增产物的交叉污染。
本发明中的试剂盒能够采用普通PCR仪完成对HLA-B*5801基因SNP位点的分型检测,且结果区分特征明显。
附图说明
下列附图用于说明本发明的具体实施方案,不用于限定有权利要求所界定的本发明范围。
图1是本发明中引物探针设计原理。
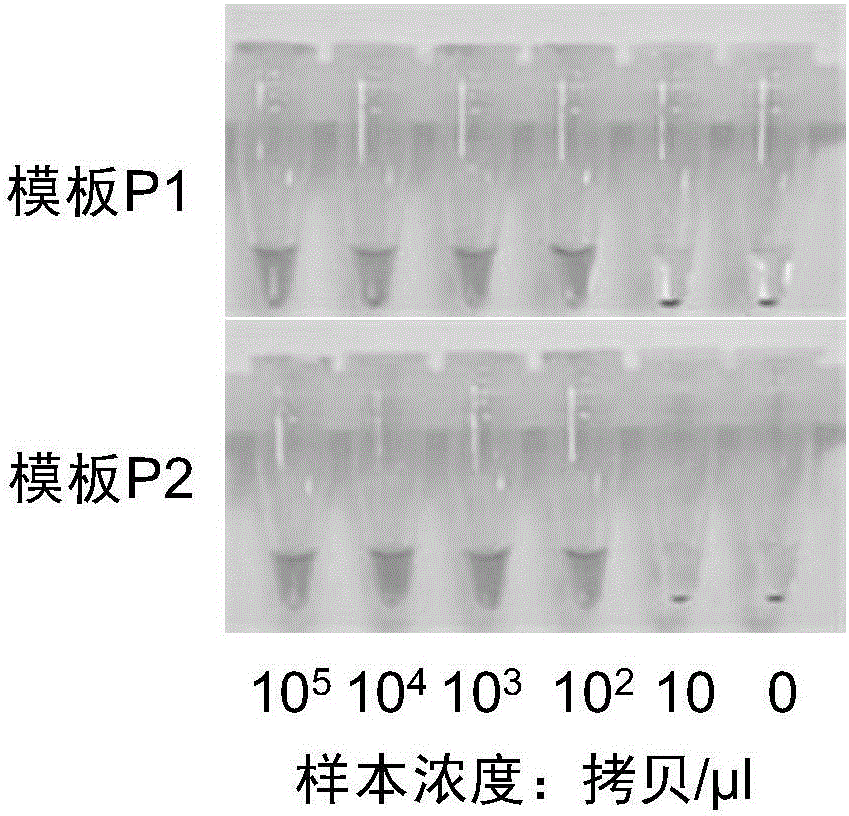
图2是实施例2中检测反应的灵敏度。
图3是实施例3中匹配基因型检测结果。
图4是实施例4中干扰实验检测结果。
图5是实施例5中代表性样本检测结果。
具体实施方式
除非另有定义,本发明所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不用于限制本发明。本发明所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
为了便于理解本发明,下面将参照相关附图对本发明进行更全面的描述。附图中给出了本发明的较佳实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。
实施例1引物探针
根据HLA-B*5801基因SNP位点的分别特异性设计对应的引物和探针,针对该位点分别由一对特异性的引物和探针决定其检测结果,其引物设计的位置和方法的原理如图1所示。
所述HLA-B*5801基因分型检测试剂盒,包含2条引物、4条常规探针、2条纳米金修饰探针、反应液、酶液。
引物、探针和纳米金探针序列如引物1-引物2、探针1-探针4、纳米金探针1-纳米金探针2,或为上述序列的互补序列:
引物1:GGA CCC CAG CTC CTT AAC A;SEQ ID NO.1
引物2:CCA TGT GGC AAA GTC GG;SEQ ID NO.2
探针1:CGC GCC GAG GGT CCC CCC C;SEQ ID NO.3
探针2:CGC GCC GAG GAT CCC CCC C;SEQ ID NO.4
探针3:AGA GTT TCC TCG GAG;SEQ ID NO.5
探针4:GTC TTG TGG TAC TGC ACT CGT CTC GGT TTT CCG AGA CGA GTC CTC GGC GCG ATC GTG ATG AAC CAT;SEQ ID NO.6
纳米金探针1:Au-AAA AAA AAA AGT TCA TGA TCA CGA T;SEQ ID NO.7
纳米金探针2:GCA GTA CCA CAA GAC AAA AAA AAA A-Au。SEQ ID NO.8
本实施例所述的试剂盒中,所述的纳米金探针的纳米金颗粒平均尺寸为1nm-200nm,较佳的纳米金颗粒平均尺寸为5nm-80nm,本实施例中所用的纳米金探针平均尺寸为10nm-30nm。上述纳米金颗粒市面上能够购买得到的合格产品即可。
所述的分型检测试剂盒,所述酶液有两种酶混合而成,两种酶分别为扩增酶和内切酶,扩增酶可以是Tth DNA聚合酶、pfu DNA聚合酶、Taq DNA聚合酶、Vent DNA聚合酶,内切酶可以是TaqPol、TthPol、TaqExo、AfuFEN、PfuFEN、MjaFEN或MthFEN。本实施例中所用的扩增酶是Taq DNA聚合酶,内切酶所用的是AfuFEN。
所述HLA-B*5801基因分型检测试剂盒对HLA-B*5801基因SNP位点进行分型检测每例样本需要2管反应实现结果分型的判读,分别针对HLA-B*5801 基因SNP位点野生型(P1)和突变型(P2),其步骤主要有以下三个阶段,而这三个阶段均是在同管闭管条件下完成的。第一阶段:模板扩增,通过引物对、扩增酶的参与,实现对目标模板的高灵敏扩增;第二阶段:通过探针和内切酶的参与,实现对目标模板向信号分子的高效率转化;第三阶段:通过纳米金探针实现对信号分子的高分辨识别。通过以上三个阶段的反应就可以实现在闭管条件下的高灵敏、高分辨、低成本的HLA-B*5801基因SNP位点进行分型检测。
所述的分型检测试剂盒,所述的检测结果判别方式可有肉眼直接判读,反应结束后反应液红色为阳性,反应液无色为阴性。
实施例2HLA-B*5801基因SNP位点分型检测灵敏度
本实施例应用实施例1所述的所述HLA-B*5801基因分型检测试剂盒,检测了不同浓度的HLA-B*5801基因SNP位点分型的模板,用来验证本发明所陈述的可视化检测方法的可行性。
反应条件:
该试剂盒每样本检测由2管反应构成,分别含有针对两种基因型的引物和探针,各管反应总体积均为20μL。HLA-B*5801基因SNP位点检测反应体系组成为:10mM Tris缓冲液(pH 8.5),1μM引物(引物1序列:SEQ ID NO.1;引物2序列:SEQ ID NO.2),1μM探针(探针1序列SEQ ID NO.3;探针2序列:SEQ ID NO.4;探针3序列:SEQ ID NO.5;探针4序列:SEQ ID NO.6),0.1μM纳米金探针(探针1:SEQ ID NO.7;探针2:SEQ ID NO.8),0.5U TaqDNA聚合酶和内切酶A,0.2mM dNTP。向该体系中分别加入105、104、103、102、10、1及0拷贝的待测核酸(模板序列P1为:5’-CAG GCA CAC AGA CCC CAG CTT TAC AAG GAC CCC AGC TCC TTA ACA CAG ATC CCA GCT CCG AGG AAA CTC GTC CCC CCC ACG TTA ATC CTG ACC GAC TTT GCC ACA TGG AGC CAG CAA ACC ATT TCT GGT GAG AGC CAA ATG CAC CTT CTG CAC CAT-3’,SEQ ID NO.9;模板序列P2为:5’-CAG GCA CAC AGA CCC CAG CTT TAC AAG GAC CCC AGC TCC TTA ACA CAG ATC CCA GCT CCG AGG AAA CTC ATC CCC CCC ACG TTA ATC CTG ACC GAC TTT GCC ACA TGG AGC CAG CAA ACC ATT TCT GGT GAG AGC CAA ATG CAC CTT CTG CAC CAT-3’,SEQ ID NO.10)。反应体系构成为反应程序为:94℃,2min;94℃,5s,72℃,40s,35循环;72℃,2min;63℃,10min;55℃,30min;10℃,2min。
反应结束后拍照,结果示于图2中。图2的结果显示本发明试剂盒可稳定的检测样本基因组DNA。
实施例3HLA-B*5801基因SNP位点分型检测匹配基因型样本检测
本实施例应用实施例1所述的所述HLA-B*5801基因分型检测试剂盒,检测了不同分型的外周血样本基因组DNA模板,分型结果分别为:突变杂合型(样本1)、野生纯合型(样本2)、突变纯合型(样本3),用来验证本发明所陈述的可视化检测方法检测实际样本的可行性。
反应条件:
该试剂盒每样本检测由2管反应构成,分别含有针对两种基因型的引物和探针,各管反应总体积均为20μL。HLA-B*5801基因SNP位点检测反应体系组成为:10mM Tris缓冲液(pH 8.5),1μM引物(引物1序列:SEQ ID NO.1;引物2序列:SEQ ID NO.2),1μM探针(探针1序列SEQ ID NO.3;探针2序列:SEQ ID NO.4;探针3序列:SEQ ID NO.5;探针4序列:SEQ ID NO.6),0.1μM纳米金探针(探针1:SEQ ID NO.7;探针2:SEQ ID NO.8),0.5U Taq DNA聚合酶和内切酶A,0.2mM dNTP。向该体系中分别加入待测样本DNA。反应体系构成为反应程序为:94℃,2min;94℃,5s,72℃,40s,35循环;72℃,2min;63℃,10min;55℃,30min;10℃,2min。
反应结束后拍照,结果参照图3(W代表野生,M代表突变)。图3的结果显示本发明试剂盒可以稳定进行样本检测。
实施例4HLA-B*5801基因SNP位点分型检测干扰实验验证
本实施例检测了加入不同干扰物质(血红蛋白、白蛋白、胆固醇、乙醇)的阳性样本,用来验证本发明所陈述的可视化检测方法检测实际样本时干扰物质对结果的影响。
反应条件:
该试剂盒每样本检测由2管反应构成,分别含有针对两种基因型的引物和探针,各管反应总体积均为20μL。HLA-B*5801基因SNP位点检测反应体系组成为:10mM Tris缓冲液(pH 8.5),1μM引物(引物1序列:SEQ ID NO.1;引物2序列:SEQ ID NO.2),1μM探针(探针1序列SEQ ID NO.3;探针2序列:SEQ ID NO.4;探针3序列:SEQ ID NO.5;探针4序列:SEQ ID NO.6),0.1μM纳米金探针(探针1:SEQ ID NO.7;探针2:SEQ ID NO.8),0.5U Taq DNA聚合酶和内切酶A,0.2mM dNTP。向该体系中分别加入不同干扰物质(0.1mg/ml血红蛋白、0.01mmol/L白蛋白、0.2mmol/L胆固醇、0.1%乙醇)的阳性样本。反应体系构成为反应程序为:94℃,2min;94℃,5s,72℃,40s,35循环;72℃,2min;63℃,10min;55℃,30min;10℃,2min。
反应结束后拍照,结果参加图4(W代表野生,M代表突变)。图4的结果显示不同干扰物质(血红蛋白、白蛋白、胆固醇、乙醇)不会影响本发明试剂盒的检测结果。
实施例5样本检测结果
本实施例检测10例临床样本,用来评价本发明所陈述的可视化检测方法检测实际样本。
反应条件:
该试剂盒每样本检测由2管反应构成,分别含有针对两种基因型的引物和探针,各管反应总体积均为20μL。HLA-B*5801基因SNP位点检测反应体系组成为:10mM Tris缓冲液(pH 8.5),1μM引物(引物1序列:SEQ ID NO.1;引物2序列:SEQ ID NO.2),1μM探针(探针1序列SEQ ID NO.3;探针2序列:SEQ ID NO.4;探针3序列:SEQ ID NO.5;探针4序列:SEQ ID NO.6),0.1μM纳米金探针(探针1:SEQ ID NO.7;探针2:SEQ ID NO.8),0.5U Taq DNA聚合酶和内切酶A,0.2mM dNTP。向该体系中分别加入10例临床样本DNA。反应程序为:94℃,2min;94℃,5s,72℃,40s,35循环;72℃,2min;63℃,10min;55℃,30min;10℃,2min。
反应结束后拍照,结果参见图5(W代表野生,M代表突变)。图5的结果显示本发明试剂盒能够正常的反应临床样本的结果。
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
SEQUENCE LISTING
<110> 广州市宝创生物技术有限公司
<120> 可视化HLA-B*5801基因分型检测试剂盒
<160> 10
<170> PatentIn version 3.3
<210> 1
<211> 19
<212> DNA
<213> 人工序列
<400> 1
ggaccccagc tccttaaca 19
<210> 2
<211> 17
<212> DNA
<213> 人工序列
<400> 2
ccatgtggca aagtcgg 17
<210> 3
<211> 19
<212> DNA
<213> 人工序列
<400> 3
cgcgccgagg gtccccccc 19
<210> 4
<211> 19
<212> DNA
<213> 人工序列
<400> 4
cgcgccgagg atccccccc 19
<210> 5
<211> 15
<212> DNA
<213> 人工序列
<400> 5
agagtttcct cggag 15
<210> 6
<211> 66
<212> DNA
<213> 人工序列
<400> 6
gtcttgtggt actgcactcg tctcggtttt ccgagacgag tcctcggcgc gatcgtgatg 60
aaccat 66
<210> 7
<211> 25
<212> DNA
<213> 人工序列
<400> 7
aaaaaaaaaa gttcatgatc acgat 25
<210> 8
<211> 25
<212> DNA
<213> 人工序列
<400> 8
gcagtaccac aagacaaaaa aaaaa 25
<210> 9
<211> 156
<212> DNA
<213> 人工序列
<400> 9
caggcacaca gaccccagct ttacaaggac cccagctcct taacacagat cccagctccg 60
aggaaactcg tcccccccac gttaatcctg accgactttg ccacatggag ccagcaaacc 120
atttctggtg agagccaaat gcaccttctg caccat 156
<210> 10
<211> 156
<212> DNA
<213> 人工序列
<400> 10
caggcacaca gaccccagct ttacaaggac cccagctcct taacacagat cccagctccg 60
aggaaactca tcccccccac gttaatcctg accgactttg ccacatggag ccagcaaacc 120
atttctggtg agagccaaat gcaccttctg caccat 156
- 还没有人留言评论。精彩留言会获得点赞!