一种肝癌的生物标记物ENSG00000248884及其应用的制作方法
本发明属于生物医药领域,涉及一种肝癌的生物标记物ensg00000248884及其应用,具体地涉及ensg00000248884在肝癌诊断和治疗中的应用。
背景技术:
肝细胞癌(hepatocellularcarcinoma,hcc)是临床上最常见的恶性肿瘤之一,虽然目前治疗手段多样,如肝移植、手术切除、化疗、放疗等,但因其恶性程度高、进展速度快、治疗复杂等特点,总体疗效不佳,预后差,死亡率高。近年来,肝癌分子生物学研究是迅速发展起来的一个崭新领域,使人们在分子水平对肿瘤的发生机制进行多方面研究,因其而生的肝癌分子靶向治疗已逐渐成为研究的热点,个别肝癌靶向药物(如索拉非尼)已进入临床应用并取得了良好的疗效,究其根本是从分子水平深入研究肝癌发生、发展中的作用机理,并将特征性分子作为抗肿瘤靶点,从而为肝癌的临床治疗开辟了新的途径。
基因组学研究表明,大约只有1%的基因可转录成有蛋白编码功能的rna,而大部分则转录成无蛋白编码功能的rna,即非编码rna。其中,长链非编码rna(longnon-codingrna,lncrna)是真核细胞中一类转录本长度大于200个核苷酸,但无或很少具有蛋白编码功能的rna,曾被认为是基因转录的副产物或“暗物质”,不具有生物学功能。随着lncrna功能学的进展,越来越多的研究表明lncrna在人类疾病中发挥重要作用。目前,研究表明lncrna具有复杂的生物学功能,如与细胞代谢、细胞凋亡、细胞周期、细胞黏附运动等有关,并可通过多种途径如调节dna甲基化、组蛋白修饰、染色质重构、作为mirna的前体、mrna降解、磷酸化作用、蛋白修饰等发挥功能,正如同内源性mirna研究已取得重要成果一样,lncrna在疾病诊断和治疗领域代表了另一类重要的分子来源,其研究前景巨大。
多项研究已证实lncrna在肿瘤领域发挥重要作用,主要体现在肿瘤的发生、发展、浸润、转移及复发等多个方面。目前,在肿瘤组织中发现的异常表达的lncrna可涉及全身各个系统,分布较为广泛,但是由于lncrna数量庞大,目前针对lncrna在癌症领域中的研究仍处在起步阶段。lncrna影响肿瘤发生和/或发展的机制尚有待进一步揭示,众多针对癌症治疗的潜在靶点也有待于研究者们不断发现。因为lncrna在肝癌的发生机制中的角色尚未阐明,因此探寻lncrna肝癌的分子基础具有重要意义。
技术实现要素:
为了弥补现有技术的不足,本发明的目的之一在于提供一种诊断产品,为实现肝癌的早期诊断提供基础。
本发明的目的之二,提供一种分子标记物,作为检测或治疗指标应用于临床。
本发明的目的之三,提供一种治疗手段和药物组合物,实现肝癌的精准分子治疗。
为了实现上述目的,本发明采用如下技术方案:
本发明提供了检测ensg00000248884的试剂在制备诊断肝癌的产品中的应用。
进一步,所述产品通过检测样本中ensg00000248884基因的表达水平来判断患者是否患有肝癌。其中,ensg00000248884基因在肝癌患者中表达下调。
所述“样本”包括细胞、组织、脏器、体液(血液、淋巴液等)、消化液、咳痰、肺胞支气管清洗液、尿、粪便等。优选的,所述样本为组织、血液。在本发明的具体实施方式中,所述样本为组织。
进一步,所述产品包括:通过rt-pcr、实时定量pcr、原位杂交、芯片或高通量测序平台检测ensg00000248884基因的表达水平以诊断肝癌。
其中,所述用rt-pcr诊断肝癌的产品至少包括一对特异扩增ensg00000248884基因的引物;所述用实时定量pcr诊断肝癌的产品至少包括一对特异扩增ensg00000248884基因的引物;所述用原位杂交诊断肝癌的产品包括:与ensg00000248884基因的核酸序列杂交的探针;所述用芯片诊断肝癌的产品包括与ensg00000248884基因的核酸序列杂交的探针。
进一步,所述用实时定量pcr诊断肝癌的产品至少包括一对特异性扩增ensg00000248884基因的引物。在本发明的具体实施方式中所述引物如seqidno.2和seqidno.3所示。
本发明提供了一种诊断肝癌的产品,所述产品能够通过检测样本中ensg00000248884基因的表达水平来诊断肝癌。
进一步,所述产品包括芯片、或试剂盒;其中,所述芯片包括基因芯片;所述试剂盒包括基因检测试剂盒。所述基因芯片包括固相载体以及固定在固相载体的寡核苷酸探针,所述寡核苷酸探针包括用于检测ensg00000248884基因转录水平的针对ensg00000248884基因的寡核苷酸探针;所述基因检测试剂盒包括用于检测ensg00000248884基因转录水平的试剂。
本发明中基因检测试剂盒或基因芯片可用于检测包括ensg00000248884基因在内的多个基因(例如,与肝癌相关的多个基因)的表达水平,将肝癌的多个标志物同时进行检测,可大大提高肝癌诊断的准确率。
本发明提供了ensg00000248884在制备治疗肝癌的药物组合物中的应用。
进一步,所述药物组合物包括ensg00000248884基因的促进剂。
本发明提供了一种治疗肝癌的药物组合物,所述药物组合物包括ensg00000248884基因的促进剂。
进一步,所述药物组合物还包括与所述促进剂相配伍的其他药类以及药学上可接受的载体和/或辅料。其中,药学上可接受的载体和/或辅料包括(但不限于)如缓冲剂、乳化剂、悬浮剂、稳定剂、防腐剂、生理食盐等。作为缓冲剂,能够使用磷酸盐、甘氨酸,山梨酸,山梨酸钟,饱和植物脂肪酸的部分甘油酯混合物,水,盐或电解质例如硫酸钾、磷酸氢二钠、磷酸氢钾、氯化钠、锌盐,胶态二氧化硅,三硅酸镁,聚乙烯吡咯烷酮,基于纤维素的物质,聚乙二醇,羧甲基纤维素钠,聚丙烯酸酯,蜡,聚乙烯-聚氧丙烯嵌段共聚物,聚乙二醇和羊毛脂等。作为乳化剂,能够使用阿拉伯树胶、海藻酸钠、西黄芪胶等。作为悬浮剂,能够使用单硬脂酸甘油、单硬脂酸铝、甲基纤维素、羧甲基纤维素、羟甲基纤维素、月桂基硫酸钠等。作为稳定剂,能够使用丙二醇、二亚乙基亚硫酸盐、抗坏血酸等。作为防腐剂,能够使用叠氮化钠、苯扎氯铵、对羟苯甲酸、氯丁醇等。本发明的药物组合物还可以包括离子交换剂如矾土,硬脂酸铝,卵磷脂,半乳化药物递送系统(sedds)例如dα一生育酚聚乙二醇1000琥珀酸盐,在药物剂型中使用的表面活性剂例如吐温或其它类似聚合递送基质,血清蛋白例如人血清白蛋白,也可以使用环糊精例如α-环糊精、β-环糊精、和γ-环糊精,或化学修饰的衍生物例如是羟基烷基环糊精,包括2-和3-羟基丙基-β-环糊精、或其它增溶衍生物来促进本发明化合物的递送。本发明所述携带基因的载体是本领域已知的各种载体,如市售的载体、包括质粒、粘粒、噬菌体、病毒等。
本发明的药物组合物还包括药学上可接受的赋形剂、填充剂、凝结剂与调和剂,如含水乳糖或无水乳糖、淀粉、葡萄糖、蔗糖、甘露醇、山梨醇、硅酸、微晶纤维素、羟甲基纤维素钠、淀粉甘醇酸钠及其衍生物等。
本发明的药物组合物还包含界面活性剂、乳化剂、扩散剂、消泡剂、涂层材料等。任何药学上或医学上可接受的界面活性剂、乳化剂、扩散剂、消泡剂等皆可被使用。
本发明所述药物组合物可口服给药、非胃肠道给药、通过吸入喷雾给药、局部给药、直肠给药、鼻给药、颊给药、阴道给药或通过植入的贮药装置给药。优选口服给药或注射给药。本发明药物组合物可含有任何常用的无毒可药用载体、辅料或赋形剂。在某些情况下,药用酸、碱或缓冲剂可用来调节制剂的ph以提高所配制的化合物或其给药剂型的稳定性。本文所用术语非胃肠道包括皮下、皮内、静脉内、肌内、关节内、动脉内、滑膜内、胸骨内、鞠内、损伤部位内、和颅内注射或输注技术。只要能达到目标组织,本发明所述药物组合物可以通过任何途径给予受体。
本发明药物组合物可以以任何口服剂型的形式口服给药,包括但不限于胶囊、片剂、乳剂和水悬浮液、分散剂和溶液。对于口服片剂,常用载体包括乳糖和玉米淀粉。一般还加入润滑剂例如硬脂酸镁。为了以胶囊形式口服给药,适用的稀释剂包括乳糖和无水玉米淀粉。当口服施用水悬浮液和/或乳液时,可将活性组分悬浮或溶解在油相中,并与乳化剂和/或悬浮剂合并。如果需要的话,可加入一些甜味剂和/或矫味剂和/或着色剂。适当时,可将用于口服给药的剂量单位制剂包微囊。例如,通过在聚合物、蜡等中将颗粒物质包衣或包埋,也可制备所述制剂已延长或维持释放。本发明的药物组合物可以用于补充内源性的ensg00000248884的缺失或不足,通过提高ensg00000248884基因的表达,从而治疗因ensg00000248884表达下调导致的肝癌。
本发明的药物还可与其他治疗肝癌的药物联用,其他治疗性化合物可以与主要的活性成分同时给药,甚至在同一组合物中同时给药。还可以以单独的组合物或与主要的活性成分不同的剂量形式单独给予其它治疗性化合物。主要成分的部分剂量可以与其它治疗性化合物同时给药,而其它剂量可以单独给药。在治疗过程中,可以根据症状的严重程度、复发的频率和治疗方案的生理应答,调整本发明药物组合物的剂量。
在本发明中,术语“生物标志物”是其在组织或细胞中的表达水平与正常或健康细胞或组织的表达水平相比发生改变的任何基因。
本领域技术人员将认识到,本发明的实用性并不局限于对本发明的标志物基因的任何特定变体的基因表达进行定量。作为非限制性的实例,标志物基因可具有seqidno.1指定的核苷酸序列。在一些实施方案中,其具有与所列的序列至少85%相同或相似的cdna序列诸如上述所列的序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或至少99%相同或相似的cdna序列。
本发明可以利用本领域内已知的任何方法测定基因表达。本领域技术人员应当理解,测定基因表达的手段不是本发明的重要方面。可以在转录水平上检测生物标志物的表达水平。
在本发明中,术语“芯片”包括:固相载体;以及有序固定在所述固相载体上的寡核苷酸探针,所述的寡核苷酸探针特异性地对应于ensg00000248884所示的部分或全部序列。
具体地,可根据本发明所述的lncrna,设计出适合的探针,固定在固相载体上,形成“寡核苷酸阵列”。所述的“寡核苷酸阵列”是指具有可寻址位置(即以区别性的,可访问的地址为特征的位置)的阵列,每个可寻址位置均含有一个与其相连的特征性寡核苷酸。根据需要,可将寡核苷酸阵列分成多个亚阵。
所述固相载体包括塑料制品、微颗粒、膜载体等。所述塑料制品可通过非共价或物理吸附机制与抗体或蛋白抗原相结合,最常用的塑料制品为聚苯乙烯制成的小试管、小珠和微量反应板;所述微颗粒是由高分子单体聚合成的微球或颗粒,其直径多为微米,由于带有能与蛋白质结合的功能团,易与抗体(抗原)形成化学偶联,结合容量大;所述膜载体包括硝酸纤维素膜、玻璃纤维素膜及尼龙膜等微孔滤膜。
术语“探针”指能与另一分子的特定序列或亚序列或其它部分结合的分子。除非另有指出,术语“探针”通常指能通过互补碱基配对与另一多核苷酸(往往称为“靶多核苷酸”)结合的多核苷酸探针。根据杂交条件的严谨性,探针能和与该探针缺乏完全序列互补性的靶多核苷酸结合。探针可作直接或间接的标记,其范围包括引物。杂交方式,包括,但不限于:溶液相、固相、混合相或原位杂交测定法。
所述探针具有与靶点基因的特定的碱基序列互补的碱基序列。这里,所谓“互补”,只要是杂交即可,可以不是完全互补。这些多核苷酸通常相对于该特定的碱基序列具有80%以上、优选90%以上、更优选95%以上、特别优选100%的同源性。这些探针可以是dna,也可以是rna,另外,可以为在其一部分或全部中核苷酸通过pna(polyamidenucleicacid,肽核酸)、lna(注册商标,lockednucleicacid,bridgednucleicacid,交联化核酸)、ena(注册商标,2′-o,4′-c-ethylene-bridgednucleicacids)、gna(glycerolnucleicacid,甘油核酸)、tna(threosenucleicacid,苏糖核酸)等人工核酸置换得到的多核苷酸。
在本发明中,针对ensg00000248884基因的寡核苷酸探针可以是dna、rna、dna-rna嵌合体、pna或其它衍生物。所述探针的长度没有限制,只要完成特异性杂交、与目的核苷酸序列特异性结合,任何长度都可以。所述探针的长度可短至25、20、15、13或10个碱基长度。同样,所述探针的长度可长至60、80、100、150、300个碱基对或更长,甚至整个基因。由于不同的探针长度对杂交效率、信号特异性有不同的影响,所述探针的长度通常至少是14个碱基对,最长一般不超过30个碱基对,与目的核苷酸序列互补的长度以15-25个碱基对最佳。所述探针自身互补序列最好少于4个碱基对,以免影响杂交效率。
在本发明中,所述ensg00000248884的促进剂是指任何可提高ensg00000248884基因或表达产物稳定性、上调ensg00000248884的表达、增加lncrnaensg00000248884的有效作用时间或促进ensg00000248884基因的转录的物质,这些物质均可用于本发明,作为对于上调ensg00000248884基因的表达有用的物质,从而可用于预防或治疗肝癌。作为本发明的一种优选方式,所述的ensg00000248884的促进剂是一种含有ensg00000248884的表达载体。所述的表达载体通常还含有启动子、复制起点和/或标记基因等。
本领域的技术人员熟知的方法能用于构建本发明所需的表达载体。这些方法包括体外重组dna技术、dna合成技术、体内重组技术等。所述的表达载体优选地包含一个或多个选择性标记基因,以提供用于选择转化的宿主细胞的表型性状,如卡拉霉素、庆大霉素、潮霉素、氨苄青霉素抗性。在本发明中,是本领域已知的各种载体,如市售的载体、包括质粒、粘粒、噬菌体、病毒等。表达载体向宿主细胞中的导入可以使用电穿孔法、磷酸钙法、脂质体法、deae葡聚糖法、显微注射、病毒感染、脂质体转染、与细胞膜透过性肽的结合等周知的方法。
本发明的药物组合物可以按药剂学上有效的量进行给药,本发明的用语“药剂学上有效的量”指的是以可适用于医学治疗或预防的合理的受惠/危险比率足以治疗或预防疾病的量,可根据包括疾病的严重程度、药物的活性、患者的年龄、体重、健康、性别、患者对药物的敏感度、所使用的本发明组合物的给药时间、给药途径及排出比率、治疗时间、与所使用的本发明的组合物配合或同时使用的药物的要素及其它医学领域中公知的要素来决定有效用量水平。本发明的药物组合物可作为单独的治疗剂进行给药,或是与其它治疗剂并用地进行给药,可以与以往的治疗剂依次地或同时地进行给药。此外,可单次或多次地进行给药。重要的是,需要对上述要素均加以考虑,并且以无副作用的最少的量可取得最大效果的量进行给药。
术语“治疗”是指不以治愈为目的,而是减缓(减少)靶定的病理状况或病症或防止复发。如果接受治疗有效量的治疗剂之后,患者成功地被“治疗”,患者显示出可观测到的和/或可度量的一种或多种特定疾病的迹象和症状的减少或消失。例如,癌细胞数目显著减少或癌细胞消失,减少肿瘤尺寸;抑制(即,在某种程度上减缓,及优选地停止)肿瘤转移;某种程度上抑制肿瘤生长;使在一定程度上减少和/或减轻与特定癌症相关联的一种或多种症状的时间增加;减少的发病率和死亡率,以及改善生活质量。疾病的迹象或症状的减轻能够为患者感知。治疗可以实现完全反应—定义为癌症的所有迹象消失,或部分反应—肿瘤尺寸减小,优选减小的比例超过50%、更优选75%。如果患者感受到疾病稳定,患者也被视为得到治疗。
本发明的优点和有益效果:
本发明首次发现了ensg00000248884在肝癌患者组织中差异表达,通过检测ensg00000248884的表达水平可以判断患者是否患有肝癌或者患病风险的高低。
本发明提供了一种肝癌的精准医疗手段,通过提高患者中ensg00000248884的转录水平,从而治疗肝癌患者。
本发明提供了一种肝癌的分子标记物,为肝癌的机理研究以及临床应用提供理论基础。
附图说明
图1是利用qpcr检测ensg00000245213在肝癌患者中的表达情况图;
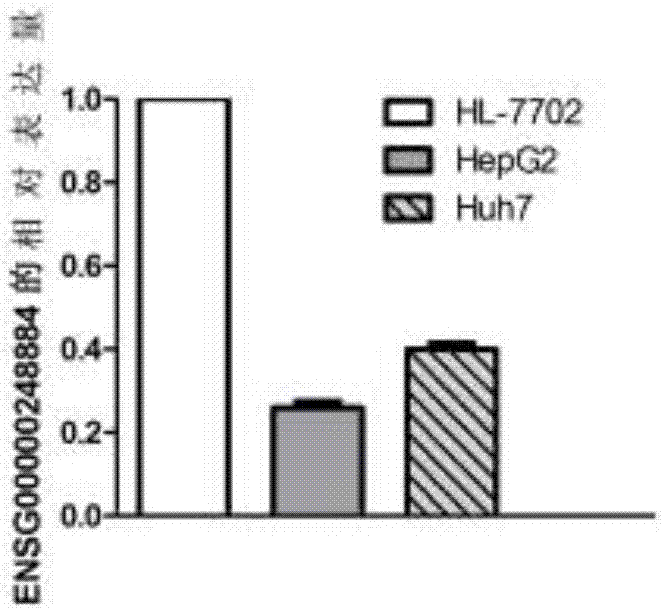
图2是利用qpcr检测ensg00000245213在肝癌细胞中的表达情况图;
图3是利用qpcr检测转染ensg00000245213在肝癌细胞中的转染情况图;
图4是利用cck8检测ensg00000245213对细胞增殖的影响图;
图5是利用利用软琼脂克隆形成实验检测ensg00000245213表达对肝癌细胞增殖能力的影响图。
具体的实施方式
下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。
实施例1筛选与肝癌相关的基因标志物
1、样品收集
各收集10例肝癌患者的癌组织以及癌旁组织,患者均知情同意,上述所有标本的取得均通过组织伦理委员会的同意。
2、rna样品的制备
利用qiagen的组织rna提取试剂盒进行组织rna的提取,按说明书的具体步骤进行操作。
3、逆转录和标记
用lowrnainputlinearamplificationkit将mrna逆转录成cdna,同时用cy3分别标记实验组和对照组。
4、杂交
基因芯片采用康城生物-humanlncrnaarray,按芯片使用说明书的步骤进行杂交。
5、数据处理
杂交后芯片用agilent扫描仪扫描,分辨率为5μm,扫描仪自动以100%和10%pmt各扫描1次,2次结果agilent软件自动合并。扫描图像数据采用featureextraction进行处理分析,得到的原始数据应用bioconductor程序包进行后续数据处理。最后ratio值为实验组和对照组。差异基因筛选标准:ratio≥4为上调基因,ratio≤0.25为下调基因。
6、结果
与癌旁组织相比,ensg00000248884基因在肝癌组织中的转录水平显著低于癌旁组织。
实施例2qpcr测序验证ensg00000248884基因的差异表达
1、对ensg00000248884基因差异表达进行大样本qpcr验证。按照实施例1中的样本收集方式肝癌组织和癌旁组织样本各60例。
2、rna提取步骤同实施例1。
3、逆转录:
采用25μl反应体系,每个样品取1μg总rna作为模板rna,在pcr管中分别加入以下组分:depc水,5×逆转录缓冲液,10mmdntp,0.1mmdtt,30μmoligodt,200u/μlm-mlv,模板rna。42℃孵育1h,72℃10min,短暂离心。
(3)qpcr扩增检验
引物序列:
ensg00000248884基因的引物序列为:
正向引物:5’-gcccaggatctacttcat-3’(seqidno.2)
反向引物:5’-acccgtttggatttgttt-3’(seqidno.3)
管家基因gapdh的引物序列为:
正向引物:5’-ccgggaaactgtggcgtgatgg-3’(seqidno.4)
反向引物:5’-aggtggaggagtgggtgtcgctgtt--3’(seqidno.5)
采用25μl反应体系,每个样本设置3个平行管,所有扩增反应均重复三次以上以保证结果的可靠性。
配制以下反应体系:sybrgreen聚合酶链式反应体系12.5μl,正反向引物(5μm)各1μl,模板cdna2.0μl,无酶水8.5μl。各项操作均于冰上进行。
扩增程序为:95℃60s,(95℃15s,60℃15s,72℃45s)×35个循环。
以sybrgreen作为荧光标记物,在lightcycler荧光实时定量pcr仪上进行pcr反应,通过融解曲线分析和电泳确定目的条带,δδct法进行相对定量。
3、统计学方法
实验都是按照重复3次来完成的,结果数据都是以平均值±标准差的方式来表示,采用spss18.0统计软件来进行统计分析的,两者之间的差异采用t检验,认为当p<0.05时具有统计学意义。
4、结果
结果如图1所示,与癌旁组织相比,ensg00000248884基因在肝癌组织中表达下调,差异具有统计学意义(p<0.05),同rna-sep结果一致。
实施例3ensg00000248884基因在肝癌细胞系中的差异表达
1、细胞培养
人肝癌细胞株hepg2、huh7和正常肝细胞系hl-7702,以含10%胎牛血清和1%p/s的培养基dmem在37℃、5%co2、相对湿度为90%的培养箱中培养。2-3天换液1次,使用0.25%含edta的胰蛋白酶常规消化传代。
2、rna的提取
1)胰酶消化贴壁细胞,吹打获得的细胞经离心、重悬、清洗后,以含10%fbs的dmem培养基重悬;
2)将重悬的细胞转移至6孔板,添加培养基至2ml/孔,轻摇6孔板使细胞均匀重悬;
3)细胞贴壁生长48h,去培养基;
4)以1mltrizol试剂裂解细胞,反复吹打6孔板壁,尽量使细胞完全裂解;
5)转移细胞裂解液至1.5mldepc处理过的ep管中,置于冰上。加入0.2m1氯仿,剩余操作步骤同组织中rna提取过程。
3、逆转录
具体步骤同实施例2.
4、统计学方法
实验都是按照重复3次来完成的,结果数据都是以平均值±标准差的方式来表示,采用spss18.0统计软件来进行统计分析的,两者之间的差异采用t检验,认为当p<0.05时具有统计学意义。
5、结果
结果如图2所示,与正常肝细胞系相比,ensg00000248884基因在肝癌细胞hepg2、huh7中表达均下调,差异具有统计学意义(p<0.05),同rna-sep结果一致。
实施例4ensg00000248884基因的过表达
1、细胞培养
人肝癌细胞株hepg2,以含10%胎牛血清和1%p/s的培养基dmem在37℃、5%co2、相对湿度为90%的培养箱中培养。2-3天换液1次,使用0.25%含edta的胰蛋白酶常规消化传代。
2、ensg00000248884基因的过表达
2.1ensg00000248884基因表达载体的构建
根据ensg00000248884的cdna序列(如seqidno.1所示)合成特异的pcr扩增引物,在5’端引物和3’端引物分别添加kpni和xhoi两个限制性酶切位点。以肝癌患者血液提取和反转录得到的cdna作为扩增模板,上述cdna序列经限制性内切酶kpni和xhoi双酶切后插入到经kpni和xhoi双酶切的真核细胞表达载体pcdna3.0中,连接获得的重组载体pcdna3.0-1用于后续实验。
2.2转染
将肝癌细胞分为三组,分别为空白对照组(hepg2)、对照组(转染pcdna3.0空载体)、和ensg00000248884过表达组(转染pcdna3.0-1)。使用脂质体2000进行载体的转染,具体转染方法按照说明书的指示进行。pcdna3.0空载体和pcdna3.0-1的转染浓度均为0.5μg/ml。
2.3ensg00000248884稳定株的筛选
1)肝癌细胞hepg2细胞筛选浓度的确定
首先按照每孔5万的细胞数铺于6孔板内,次日待细胞贴壁后换用含g418的培养液继续培养细胞,g418浓度梯度为500、600、700、800、900、1000和1100mg/l。以1周后6孔板内的细胞刚好完全死亡的浓度为筛选浓度,最终确定最佳g418筛选浓度为1000mg/l。
2)ensg00000248884稳定株的筛选
按照2.2转染步骤hepg2细胞,转染后培养至24h,按1:16和1:32的比率传代接种于直径80mm的培养皿中,待细胞贴壁后加入1000mg/l的g418,培养2周后,利用套环法及有限稀释法将存活下来的细胞株接种于96孔板中获得稳定转染的单克隆,同时改用维持浓度500mg/l的6418继续扩大培养。
3)ensg00000248884基因表达rt-pcr鉴定
按照实施例3的方法提取总rna并采用ensg00000248884的扩增引物检测ensg00000248884的表达情况。挑选ensg00000248884高表达细胞株。
2.3qrt-pcr检测
采用实时定量pcr检测上步中的阳性克隆细胞ensg00000248884表达水平高低具体步骤同实施例2,挑选高表达细胞株用于后续的功能实验研究。
3、统计学方法
实验都是按照重复3次来完成的,结果数据都是以平均值±标准差的方式来表示,采用spss18.0统计软件来进行统计分析的,两者之间的差异采用t检验,认为当p<0.05时具有统计学意义。
4、结果
如图3所示,与空白对照组和转染pcdna3.0空载体的细胞相比,转染pcdna3.0-1的细胞中ensg00000248884的含量显著上调,差异具有统计学意义(p<0.05)。
实施例5cck8检测细胞增殖实验
1、细胞培养与转染步骤同实施例3
2、cck8检测细胞增殖
1)将对数增殖期的hepg2细胞接种于96孔板,每孔2×103个细胞;
2)实验分三组,分别是空白组、转染pcdna3.0组和转染pcdna3.0-1,每组设6个复孔;
3)分别在转染0h、24h、48h、72h后加入10μl/孔cck8试剂;
4)2h后使用酶标仪检测a450的吸光值。
3、统计学方法
实验都是按照重复3次来完成的,采用spss13.0统计软件来进行统计分析,两者之间的差异采用t检验,认为当p<0.05时具有统计学意义。
4、结果
图4所示的结果显示:空白组同空载组无明显差异,而转染pcdna3.0-1组的细胞生长速度明显低于转染pcdna3.0空载体组的细胞生长速度,差异具有统计学意义(p<0.05),上述结果表明ensg00000248884的表达能够抑制肝癌细胞的生长。
实施例6软琼脂克隆形成实验
1、用0.25%胰蛋白酶消化处于对数生长期的细胞,轻轻吹打使之成为单细胞悬液,离心收集细胞沉淀。
2、用含20%胎牛血清的dmem完全培养基重悬,适当稀释后计数,调整细胞浓度为5×103个/ml。
3、制备两个浓度分别为1.2%和0.7%的低溶点琼脂糖液,高压灭菌后,维持在40℃水浴中。
4、1.2%的琼脂糖和2×dmem培养基1:1混合,加入2×抗生素和20%的小牛血清,取3ml混合液注入直径6cm平皿中放置5min冷却凝固,作为底层琼脂置于co2温箱中备用。
5、在无菌试管中1:1混合0.7%的琼脂糖和2×dmem培养基,再向管中加入0.2ml浓度为5×103个/ml的稳定感染细胞悬液,充分混匀,注入上述平皿中,逐渐形成双琼脂层,每个实验组重复4个样本。
6、待上层琼脂凝固后,置入37℃5%co2温箱中培养,每3天加培养基1.5ml。7、培养14天后取出培养皿,用1ml浓度为0.005%的龙胆紫染色90min。把平皿放置在倒置显微镜下观察,每组细胞随机选取10个低倍视野,镜下技术形成的细胞克隆数。
8、结果
结果如图5所示,与其他组相比,转染pcdna3.0-1的细胞组单细胞克隆集落形成数显著降低。
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
sequencelisting
<110>王冬国
<120>一种肝癌的生物标记物ensg00000248884及其应用
<160>5
<170>patentinversion3.5
<210>1
<211>410
<212>dna
<213>人源
<400>1
taagggcttccctgacatagacgacttgcttctttcaaatttggtcatcgccctcttgcc60
ttcctgtgtgagtcagcgtggctgcccttgtgcacgccaggctcctgtctgtgctccggg120
gcctgtttcctggcctccccagatgaggaaactgaggcacaaaaaggtgaagtcctgagc180
tcacagtcatgcaaccagcaggtggtgaaacacacctccaagctgcctgcctcctaagca240
tcaagctttgtggcccaggatctacttcatgctccaaatattcatggaccttcccaggac300
ctcaacaaaacaaaaccatgaagaaaaaccttgacatgaaccccaaaaaaacccagtcag360
caatattttaagttaaattttgaaacaaatccaaacgggttcctccccat410
<210>2
<211>18
<212>dna
<213>人工序列
<400>2
gcccaggatctacttcat18
<210>3
<211>18
<212>dna
<213>人工序列
<400>3
acccgtttggatttgttt18
<210>4
<211>22
<212>dna
<213>人工序列
<400>4
ccgggaaactgtggcgtgatgg22
<210>5
<211>25
<212>dna
<213>人工序列
<400>5
aggtggaggagtgggtgtcgctgtt25
- 还没有人留言评论。精彩留言会获得点赞!