一种pH响应与协同治疗的靶向小分子前药的制备方法与流程
本发明涉及化学药物领域,具体涉及一种ph响应与协同治疗的靶向两亲性小分子前药的制备与用途。
背景技术:
氨甲蝶呤(methotrexate,mtx,别名:(+)-氨甲蝶呤,甲氨基叶酸,分子式:c20h22n8o5,cas号:60388-53-6),是叶酸拮抗剂,与叶酸差异仅在n10上的nh上的氢改为甲基(ch3),以及环上c4酮基改为氨基(nh2),故可与叶酸竞争同一酵素,通过对二氢叶酸还原酶的抑制而达到阻碍肿瘤细胞dna的合成,从而抑制肿瘤细胞的生长与繁殖,抗代谢疗法的抗癌药物。同时由于与叶酸结构相近,氨甲蝶呤可与细胞表面的叶酸受体进行特异性结合使药物能够集中在叶酸受体比较多的癌细胞内。此外,氨甲蝶呤与叶酸性质相似,具有较好的亲水性。盐酸阿霉素(doxorubicin,dox)别名多柔比星,阿霉素等。分子式:c27h29no11,cas号:23214-92-8),是一种抗肿瘤抗生素,有效抑制rna和dna的合成,具有广泛的抗谱性,对急性白血病,乳腺癌以及肝癌等多种肿瘤具有很好的治疗效果。研究证明,dox药物呈交叉耐药性,并与mtx具有一定的协同治疗作用,因此设计一种集mtx和dox于一体的智能型药物递送系统对于解决治疗效率低,药物耐药性强等问题具有非常强的现实意义。
由于抗癌药物往往表现出水中溶解度低以及药物靶向递送性弱等特点,在实际化疗过程中,对正常组织或细胞有较大的细胞毒性,影响了肿瘤治疗的难度与周期,因而提高药物水溶性及其靶向性等具有重大的科学与实际意义。小分子药物递送系统可有效结合小分子药物和生物纳米技术等优点,可选择性地将药物递送至病灶,减低毒副作用的同时可有效提高了药物的医疗疗效。一些研究报道中,通常将抗癌药物与亲水性的聚合物例如聚乙二醇等通过酯键或酰胺键结合形成纳米粒子,酯键与酰胺键往往需要体内的酯酶或酰胺酶的存在才可断裂,而酯酶在体内是广泛分布的,酰胺酶含量较低,因而难以实现药物的可控释放,此外这种策略由于存在较大比例的载体成分,药物上载量不高,不能实现无载体的药物递送。例如:cn103285400b公开了一种酸敏感聚合物前药的合成及应用,抗癌药物阿霉素与a-b型两嵌段聚合物通过缩醛键链接,并制得聚乙二醇亲水嵌段为外表面,疏水药物为疏水核的前药胶束纳米颗粒,并通过物理包埋的形式包埋另外一种抗癌药物,增强了对癌细胞的杀伤能力。
技术实现要素:
本发明旨在针对现有抗肿瘤药物载体含量高,药物上载量低及药物释放不可控等缺陷,提供一种ph响应与协同治疗的靶向两亲性小分子前药的制备及应用。本发明具体技术方案如下。
一种ph响应与协同治疗的靶向两亲性小分子前药制备方法包括以下步骤:
(1)在冰浴和氩气(ar)氛围条件下,将氨甲喋呤(mtx)溶于无水n,n-二甲基甲酰胺(dmf)中,往溶液中分别加入n-羟基丁二酰亚胺(nhs)和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc·hcl);
(2)将步骤(1)得到的溶液在冰水浴中搅拌30min;
(3)再往步骤(2)的溶液中加入肼基甲酸丁酯(bh)的无水dmf溶液,室温避光搅拌24h,在去离子水中进行沉淀,抽滤并用丙酮清洗,获得中间产物,即ph响应的氨甲喋呤前驱体(mtx-bh)。
(4)将步骤(3)得到的mtx-bh加入二氯甲烷(dcm)和三氟乙酸(tfa)体积比为1:1的混合液中,避光搅拌30min;旋转蒸发除去溶剂,得到黄色的固体;
(5)将步骤(4)得到的固体尽可能分散于甲苯中,旋转蒸发除去甲苯,重复三次,最后再用乙醚清洗三次,旋转蒸发除去乙醚,这样得到脱叔丁氧羰基保护的mtx-bh药物前驱体;
(6)将步骤(5)得到的脱叔丁氧羰基保护的mtx-bh药物前驱体溶于无水dmf中,加入dox的甲醇溶液,室温避光反应72h,最后在甲醇中透析除去未反应的dox即可得到所需产物(mtx-dox),即ph响应与协同治疗的靶向两亲性小分子前药mtx-dox。
进一步的,步骤(1)中mtx、nhs、edc·hcl三者物质的量的比为1:1:1-1:1.5:1.5,需要将mtx、nhs、edc·hcl三者完全溶解在dmf中。
进一步的,步骤(3)中bh与步骤(1)中mtx的物质的量的比为1:1-1.5:1。步骤(4)中每1mmolmtx-bh需要dcm和tfa混合溶液为20ml。
进一步的,步骤(6)中脱叔丁氧羰基保护的mtx-bh药物前驱体与dox物质的量比为1:2-1:3。
进一步的,步骤(4)、(5)和(6)需要连续进行;所述步骤(5)和(6)中的脱叔丁氧羰基保护后的mtx-bh放置时间不可超过一周。
本发明的主要优点有:
1.针对目前小分子前药递送系统存在的问题,本发明创造性地提出一种兼具小分子前药和纳米药物优势于一体的基于ph响应两亲性小分子前药自组装的递送系统,能有效提高药物上载量和双药协同效应,解决当前小分子前药递送系统靶向传递以及药物选择性的可控释放问题,推动肿瘤的精确诊断与高效治疗。
2、在本发明中,氨甲蝶呤药物分子的引入,形成的纳米粒子可暂时屏蔽药物分子的荧光,内吞作用下进入细胞,纳米粒子解组装,药物分子的荧光可得到还原,实现药物的追踪,药物在刺激响应下释放出两种药物,实现癌症的治疗与药物的追踪也是本项目的最大特色之一。
附图说明
为了使本发明的目的、技术方案和有益效果更加清楚,本发明提供如下附图:
图1为本发明实施例1中ph响应的靶向两亲性小分子前药(mtx-dox)的合成示意图。
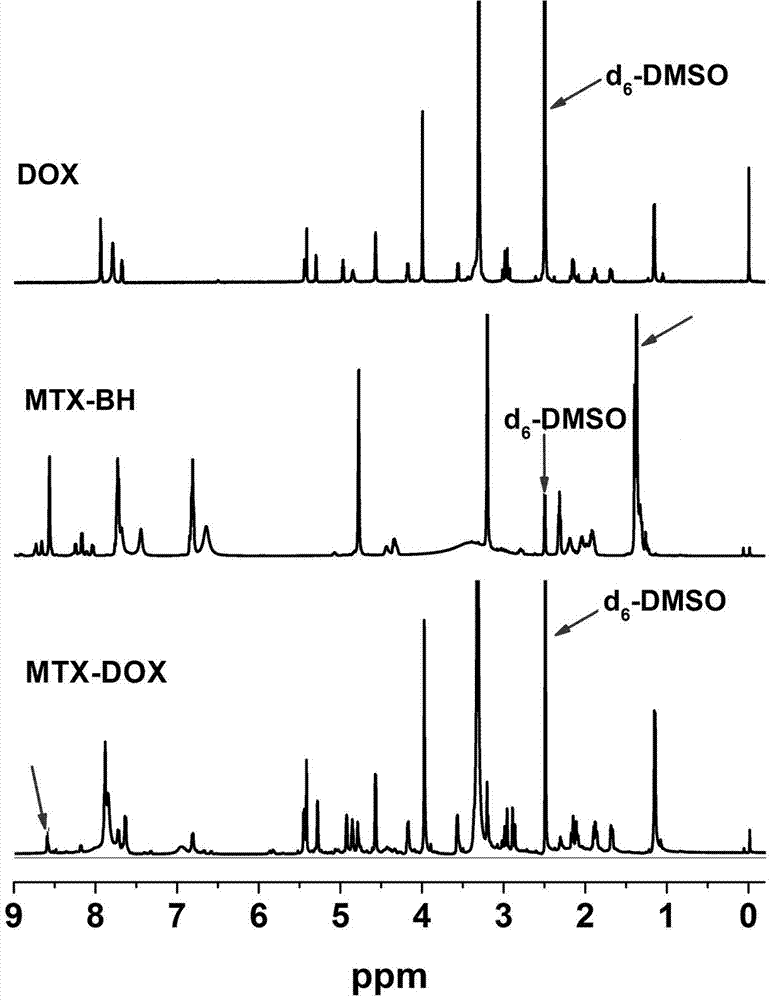
图2为本发明实施例1中ph响应的靶向两亲性小分子前药(mtx-dox)的核磁示意图。
图3为本发明实施例1中ph响应的靶向两亲性小分子前药(mtx-dox)的红外示意图。
图4为本发明实施例1中小分子前药纳米胶束的dls图。
图5为本发明实施例1中ph响应的靶向两亲性小分子前药(mtx-dox)纳米粒子的体外释药示意图。
图6为本发明实施例1中小分子药物纳米胶束对kb癌细胞作用48h的体外毒性图(a)及其对a549细胞和kb细胞的对比作用图(b)。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1制备ph刺激响应的mtx-dox两亲性小分子前药
(1)在冰浴,氩气(ar)氛围条件下,首先将1.034gmtx溶于25ml无水n,n-二甲基甲酰胺(dmf)中,接着分别加入260.5mgn-羟基丁二酰亚胺(nhs)和447.0mg1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc·hcl);冰水浴中搅拌30min后,将325.3mg肼基甲酸丁酯(bh)溶于5ml无水dmf溶液,加入上述反应溶液中,室温避光搅拌24h;在去离子水中进行沉淀,抽滤并用丙酮清洗,即可获得稳定产物ph响应的氨甲喋呤前驱体(mtx-bh)308.0mg,产率为23.82%。
(2)首先mtx-bh中氨基的脱叔丁氧羰基保护反应,将步骤(1)反应的部分产物mtx-bh85.4mg加入1.5mldcm和tfa体积比为1:1的混合液中,避光搅拌30min;旋转蒸发除去溶剂,得到的固体尽可能分散于2.5ml甲苯中,旋蒸除去甲苯,重复三次,最后再用2.5ml乙醚清洗三次,旋蒸出去乙醚,得到脱叔丁氧羰基保护的mtx药物前驱体;将得到的全部脱叔丁氧羰基保护的mtx药物前驱体溶于5ml无水dmf中,加入含180.1mgdox的甲醇溶液5ml,避光反应72h,甲醇中透析即可得到所需产物ph响应与协同治疗的靶向两亲性小分子前药mtx-dox86.4mg,产率57.97%。其合成过程见图1;核磁表征结果见图2,mtx-bh中1.37ppm的峰即为叔丁氧羰基的氢谱峰,mtx-dox中8.6ppm处的出峰为肼基氢谱峰;红外表征图见图3,1600-1575cm-1处的出峰即为肼基氢的峰。
(3)制备小分子前药纳米胶束:室温情况下,配备5mg/ml的mtx-dox的二甲基亚砜(dmso)溶液,加入极少量的三乙胺(tea)搅拌均匀(1mgmtx-dox加1μltea),缓慢滴加到去离子水中,搅拌一定时间后,二次水中透析获得浅红色的小分子前药纳米胶束。如图4,其dls结果显示前药纳米胶束为70.27nm,其粒径分布系数为0.205。对所得纳米粒子的体外释放进行测定,由图5可得当ph为5.04时,药物的累计释放率可达85%,而当ph增大至6.80,7.44时,释放率显著降低。图6a是所得纳米胶束与游离药物对kb肿瘤细胞作用48h的体外毒性对比示意图,图6b是纳米胶束靶向毒性示意图(kb细胞表面相对a549细胞有较多的叶酸受体),由图可知mtx-dox纳米药物对肿瘤细胞毒性随浓度增大而增加,且对a549肿瘤细胞的毒性相对kb肿瘤细胞要小。
最后说明的是,以上优选实施例仅用以说明本发明的技术方案而非限制,尽管通过上述优选实施例已经对本发明进行了详细的描述,但本领域技术人员应当理解,可以在形式上和细节上对其作出各种各样的改变,而不偏离本发明权利要求书所限定的范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 阻断UBE2M介导Neddylation修饰在肾细胞癌治疗中的应用的制造方法与工艺
- 无载体共组装肿瘤靶向抗癌纳米药物及其制备方法与应用与流程
- 一种用于判断靶向单克隆抗体治疗肿瘤疗效的预测分子的制造方法与工艺
- 一种靶向CD47的免疫检查点抑制剂药物组合物及其制备方法与流程
- 具有淋巴靶向功能的生物自组装纳米晶注射剂及制备方法与流程
- 用于检测肝癌的基因标志物及其用途的制造方法与工艺
- 特异性shRNA筛选及其靶向Ang‑2基因抑制肺癌细胞的验证方法与流程
- 一种多功能自动化生物细胞提取分离控制系统及采用该系统实现的细胞提取分离方法与流程
- 一种融合蛋白及光敏剂复合物及其制备方法和应用与流程
- 具有可视化和显示光斑边界功能的光动力治疗系统的制造方法与工艺
- 肿瘤靶向核磁共振/荧光双模态成像造影剂及其制备和应用的制造方法与工艺
- pH氧化还原双敏感的PAMAM靶向纳米给药载体及其制备方法与制造工艺
- 具有卵巢肿瘤靶向D构型多肽及其基因递释系统的制造方法与工艺
- 靶向survivin纳米抗体及其制备方法和应用与制造工艺
- 用于PSMA靶向的成像和放射疗法的金属/放射性金属标记的PSMA抑制物的制造方法与工艺
- 一种线粒体靶向的粘度荧光探针及其制备方法和应用与制造工艺
- 一种兼具荧光可视、磁靶向和pH敏多功能的复合空心微球药物载体及其制备方法与制造工艺
- 一种用于修饰微泡的多肽以及靶向GBM的药物制剂的制造方法与工艺
- 白果内酯作为脑靶向增效剂在制备防治脑肿瘤药物的应用的制造方法与工艺
- 机器人辅助精确靶向穿刺软组织目标柔性针夹紧固定装置的制造方法