化合物FuramycinsⅠ和Ⅱ及其制备方法和应用与流程
本发明涉及化合物furamycinsⅰ、ⅱ的结构、制备方法,以及furamycinsⅰ、ⅱ在制备抗菌药物及生物农药中的应用。
背景技术:
由于抗生素的滥用,耐药菌以及由耐药菌,特别是革兰氏阴性耐药菌引起的感染在全世界范围内已经到了前所未有的程度,包括亚太地区、拉丁美洲、欧洲、北美等等。世界卫生组织(worldhealthorganization)已经将耐药菌感染列为危害人类健康的三大因素之一。而且根据美国传染病协会(infectiousdiseasessocietyofamerica)的研究以及欧洲疾病预防控制中心(europeancentrefordiseasepreventionandcontrol)与欧洲药品管理局(europeanmedicinesagency)的报道,现在可用于临床有效治疗耐药菌的候补抗生素已经越来越少。于是,美国传染病协会在2010年发起了一个“10×20”的提议:到2020年发现10个新颖、安全、高效的抗生素用于临床治疗。可见,新抗生素的发现已经成为全球科学研究人员的关注热点。
本发明所涉及的化合物furamycinsⅰ和ⅱ是本发明申请人从一株海洋放线菌streptomycesgriseussp.kcb-132中纯化制备的一个新化合物,研究发现该化合物furamycinsⅰ和ⅱ具有光谱抗菌活性,可明显的抑制真菌及细菌得生长,具有新型抗菌药物开发的价值。该化合物的化学结构、制备方法及其抗癌活性均为首次公开。
技术实现要素:
本发明提供一种新化合物的制备方法,及其在制备抗菌药物及生物农药中的应用。
本发明所涉及的用于制备抗菌药物及生物农药的化合物为furamycinsⅰ和ⅱ,其化学式是:c20h18o6,具有ⅰ和ⅱ式结构式。
本发明所涉及的化合物i,即furamycinsⅰ和ⅱ的制备方法,工艺流程为:
将海洋链霉菌streptomycesgriseussp.kcb-132划线接种于固体培养基上,28℃培养3~4d,直至长出白色的孢子,接种到液体培养基,28℃,150~220rpm/min,摇床培养8~12d收获发酵物。过滤发酵物获得发酵液和菌丝体,发酵液经大孔吸附树脂柱提取,菌丝体经丙酮破碎提取,减压浓缩提取物,合并后利用有机溶剂萃取,减压浓缩得总浸膏。总浸膏经硅胶柱层析,进行梯度洗脱,收集洗脱液体积比1:25的洗脱组分,将收集的洗脱组分进行ods反相柱层析,收集60~70%有机醇洗脱部分,浓缩,进行hplc制备得到化合物i和ii。
本工艺中所用涉及的培养基,为半海水isp2培养基、纯海水isp2培养基的一种,优选为半海水isp2培养基。
本工艺中所涉及的用作提取溶剂的有机醇,为甲醇、乙醇中的一种,优选为乙醇。
本工艺中所涉及的大孔吸附树脂柱,为弱极性或非极性的大孔吸附树脂,优选弱极性。
本工艺中所涉及的用作萃取的溶剂,为乙酸乙酯、正丁醇中的一种,优选为乙酸乙酯。
本工艺中所涉及的高效液相色谱溶剂,可用甲醇、乙醇、乙腈等溶剂中的一种或几种,优选甲醇,其与水的配比优选60%。
本发明还提供了该化合物在制备抗菌药物及生物农药中的应用。
本发明涉及的化合物,其化学结构、制备方法及其抗菌活性,均为首次公开,不存在由其他化合物给出任何启示的可能,具备突出的实质性特点,且有望用于一种新型抗菌药物或生物农药的开发。
附图说明
图1furamycinsⅰ正离子质谱图(hr-esi-ms)。
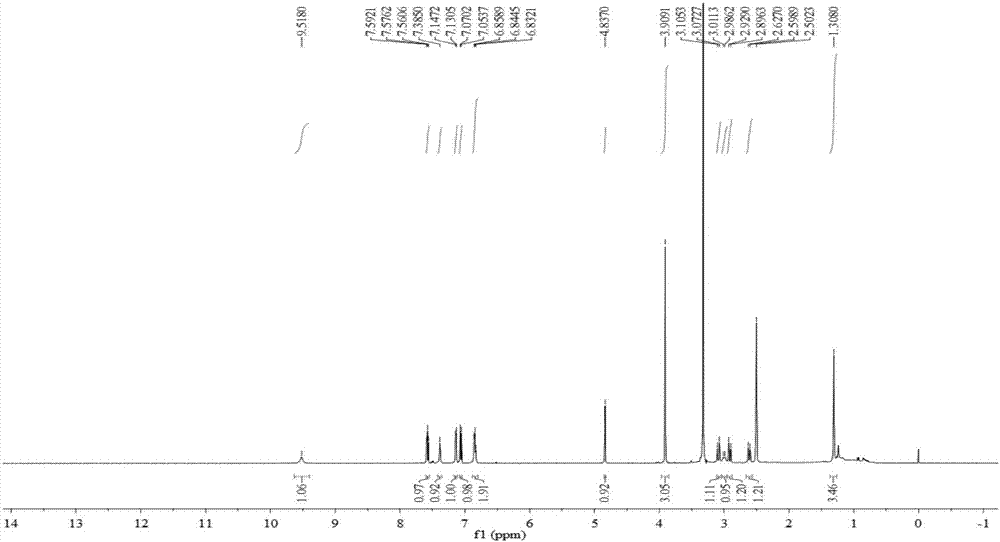
图2furamycinsⅰ1hnmr谱图(溶剂:dmso-d6)。
图3furamycinsⅰ13cnmr谱(溶剂:dmso-d6)。
图4furamycinsⅰdept-135谱(溶剂:dmso-d6)。
图5furamycinsⅰ1h-1hcosy谱(溶剂:dmso-d6)。
图6furamycinsⅰhmbc谱(溶剂:dmso-d6)。
图7furamycinsⅰnoesy谱(溶剂:dmso-d6)。
图8furamycinsⅰhsqc谱(溶剂:dmso-d6)。
图9furamycinsⅱ正离子质谱图(hr-esi-ms)。
图10furamycinsⅱ1hnmr谱图(溶剂:dmso-d6)。
图11furamycinsⅱ13cnmr谱(溶剂:dmso-d6)。
图12furamycinsⅱdept-135谱(溶剂:dmso-d6)。
图13furamycinsⅱ1h-1hcosy谱(溶剂:dmso-d6)。
图14furamycinsⅱhmbc谱(溶剂:dmso-d6)。
图15furamycinsⅱnoesy谱(溶剂:dmso-d6)。
图16furamycinsⅱhsqc谱(溶剂:dmso-d6)。
具体实施方式
下面的实施例用以解释本发明,但是并非对本发明实质内容的限制。
实施例1.furamycinsⅰ和ⅱ的制备
将海洋链霉菌streptomycesgriseussp.kcb-132划线接种于isp2半海水固体培养基上,28℃培养3d后,取1cm2菌苔接种到isp2半海水isp2液体培养基中,28℃,180rpm/min,摇床培养10d收获发酵物。过滤发酵物获得发酵液和菌丝体,发酵液经xad-16大孔吸附树脂柱提取,菌丝体经丙酮破碎提取,减压浓缩提取物,合并后利用乙酸乙酯萃取,减压浓缩得总浸膏。总浸膏经硅胶柱层析,进行梯度洗脱,收集甲醇:二氯甲烷为1:20(体积比)的洗脱组分,将收集的洗脱组分进行ods反相柱层析,收集20~30%甲醇水洗脱部分,浓缩,冷藏结晶,过滤,减压干燥,即得到furamycinsⅰ和ⅱ粗晶。将粗晶溶于甲醇和二氯甲烷的混合溶剂中形成过饱和溶液,4℃低温保存,重结晶,得纯度达99%以上的furamycinsⅰ和ⅱ样品。
实施例2.furamycinsⅰ的结构确证
1.仪器与材料
jascop-1020数字式旋光仪,agilenttof/6500高分辨率质谱,岛津uv-2401型可见-紫外分光光度计,核磁为brukeavanceiii500nmrspectrometer,为按上述实施例1步骤制备。
2.化合物结构鉴定
白色粉末,易溶于二甲亚砜、甲醇,丙酮、氯仿、微溶于水,[α]d25+154.1(dmso,c0.082);uv(acetonitrile),λmax(logε)208(3.7),301(2.6),320(2.4)nm;hresims[m-h]-,m/z353.1034(δ0.3mmu)。1d和2dnmr数据见表一,图谱分别见图1是furamycinsⅰ正离子质谱图(hr-esi-ms)。图2是furamycinsⅰ1hnmr谱图(溶剂:dmso-d6)。图3是furamycinsⅰ13cnmr谱(溶剂:dmso-d6)。图4是furamycinsⅰdept-135谱(溶剂:dmso-d6)。图5是furamycinsⅰ1h-1hcosy谱(溶剂:dmso-d6)。图6是furamycinsⅰhmbc谱(溶剂:dmso-d6)。图7是furamycinsⅰnoesy谱(溶剂:dmso-d6)。图8是furamycinsⅰhsqc谱(溶剂:dmso-d6)。
表一:furamycinsⅰ的核磁数据(1hnmr500mhz,13cnmr125mhz)。
据此确定该化合物结构。
实施例3.furamycinsⅱ的结构确证
1.仪器与材料
jascop-1020数字式旋光仪,agilenttof/6500高分辨率质谱,岛津uv-2401型可见-紫外分光光度计,核磁为brukeavanceiii500nmrspectrometer,为按上述实施例1步骤制备。
2.化合物结构鉴定
无色粉末,易溶于二甲亚砜、甲醇,丙酮、氯仿、微溶于水,[α]d25–316.3(dmso,c0.086);uv(acetonitrile)λmax(logε)208(3.6),299(2.6),326(2.4)nm;hresims[m+na]+,m/z377.1000(δ-0.1mmu)。1d和2dnmr数据见表一,图谱分别见图1是furamycinsⅰ正离子质谱图(hr-esi-ms)。图2是furamycinsⅱ1hnmr谱图(溶剂:dmso-d6)。图3是furamycinsⅱ13cnmr谱(溶剂:dmso-d6)。图4是furamycinsⅱdept-135谱(溶剂:dmso-d6)。图5是furamycinsⅱ1h-1hcosy谱(溶剂:dmso-d6)。图6是furamycinsⅱhmbc谱(溶剂:dmso-d6)。图7是furamycinsⅱnoesy谱(溶剂:dmso-d6)。图8是furamycinsⅱhsqc谱(溶剂:dmso-d6)。
表二:furamycinsⅱ的核磁数据(1hnmr500mhz,13cnmr125mhz)。
据此确定该化合物结构。
实施例4.抗菌瘤活性初步测评
菌株的发酵:将生长良好的斜面培养物分别接种于含100mlyim38#培养基的500ml三角瓶中,180rpm旋转摇床,28℃培养7d。
发酵液的处理及样品制备:
1)发酵液在4500rpm离心20min,将菌丝体与发酵液分开;
2)菌体的处理:加适量的丙酮浸泡菌体过夜后,过滤,将丙酮通过旋转蒸发仪蒸干,菌丝弃掉;
发酵液的处理:以50%发酵液体积的乙酸乙酯萃取,合并后蒸干;
3)将蒸干后的粗提物用甲醇溶解在5ml的螺口瓶中,低温保存备用。
检定菌平板的制备:
1)测活平板的制备方法1(适用于白色念珠菌、鲍曼不动杆菌、粪肠球菌、肺炎克雷伯菌、金黄色葡萄球菌、大肠埃希氏菌和铜绿假单胞菌):菌株在斜面培养基上37℃生长约1天,接种于lb、mh或ypd液体培养基中,37℃摇床培养12h,以1%的量加入融化并冷却至40℃左右的lb、mh或ypd的固体培养基中,摇匀后迅速倒入已经含有相应固体培养基作为底层的9cm培养皿中。
2)测活平板的制备方法2(适用于马尔尼菲青霉菌、葡萄炭疽菌):菌株在bhi斜面培养基上37℃生长3-5天,直到至菌丝覆盖整个斜面。从真菌的斜面上刮取尽量多的菌体于5ml无菌水中,使用磨菌器将菌丝磨碎,得到菌悬液。将菌悬液以1%的量加入融化并冷却至40℃左右的bhi培养基中,摇匀后迅速倒入已经含有相应固体培养基作为底层的9cm培养皿中。抗菌活性测定:
吸取甲醇溶解的乙酸乙酯萃取物和菌丝体丙酮浸提物(部分菌株)60μl,分2次加到直径为5mm的圆形无菌滤纸片上,待甲醇挥干后,贴于含有指示菌的检定平板上,同时以甲醇为阴性对照,以双抗(1000unit/ml青霉素和1000mg/ml链霉素)作为阳性对照,细菌于37℃培养12h、真菌37℃培养48h,观察并记录抑菌圈的大小。
3.结论:
furamycinsⅰ对白色念珠菌、大肠埃希氏菌、马尔尼菲青霉菌及葡萄炭疽菌有较好抑制活性。furamycinsⅱ对白色念珠菌、马尔尼菲青霉菌及葡萄炭疽菌有较好抑制活性。
表三furamycinsⅰ和ⅱ的抑菌活性
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明披露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!