一种EB病毒特异性TCR及其重组慢病毒载体与应用的制作方法
本发明涉及抗肿瘤免疫技术领域,尤其是一种EB病毒特异性TCR及其重组慢病毒载体与应用。
背景技术:
EB病毒(epstein-barr virus,EBv),是Epstein和Barr于1964年首次成功地将Burkitt非洲儿童淋巴瘤细胞通过体外悬浮培养而建株,并在建株细胞涂片中用电镜观察到疱疹病毒颗粒,认为该病毒是多种恶性肿瘤(如鼻咽癌)的病因之一,它主要感染人类口咽部的上皮细胞和B淋巴细胞。在中国南方鼻咽癌患病人群中大多都检测到有EB病毒基因组存在。
鼻咽癌(nasopharyngeal carcinoma,NPC)是中国南部常见的恶性肿瘤之一。流行病学调查显示,鼻咽癌可见于世界的许多国家和地区,但是大部分地区发病率较低,一般在1/10万以下。我过南部(广东、广西、福建、香港、湖南和江西)是世界鼻咽癌的高发区,其发病率高达50/10万,其中以广东省为最高。世界卫生组织(WTO)于1991年提出将鼻咽癌分为:角化性鳞状细胞癌、非角化性癌和未分化癌,其中非角化性癌在鼻咽癌高发区常见。
EB病毒与非角化性鼻咽癌密切相关。表现在:鼻咽癌患者活检组织中可发现EB病毒DNA基因产物表达,特别是在非角质化癌中EB病毒检出率几乎为100%,应用原位杂交或多聚酶链反应(PCR),鼻咽癌患者的血清/血浆中科院定量检测到游离的EBV DNA,EB病毒的DNA水平可预测鼻咽癌预后和生存率;在鼻咽癌血清/血浆中可检测到较高滴度的EBV特异性抗体,尤其是EBV早期抗原(EA)和病毒衣壳抗原(VCA)的IgA抗体的阳性率很高。EB病毒相关的肿瘤感染都处于潜伏期,EB病毒的潜伏感染分为3种类型:I型感染表达EBNA1和EBERs,相关的恶性肿瘤是Burkitt’s淋巴瘤;II型感染表达EBNA1、LMP1、LMP2及Bam HI片段的转录产物,见于非角化性NPC和何杰氏病(HD);III型感染表达所有潜伏期基因,包括6种核抗原(EBNA1、EBNA2、EBNA3A、EBNA3B、EBNA3C、EBNA-LP),2种潜伏膜蛋白(LMP1、LMP2)和2种小核糖核酸(EBER1、EBER2),见于传染性单核细胞增多症(IM)、PTLD及部分艾滋病(AIDS)相关淋巴瘤等。鼻咽癌中病毒以潜伏II型方式存在,表达EBNA1、LMP1、LMP2及Bam HI片段的转录产物等病毒产物。EBNA1在维持病毒感染中具有重要作用,是唯一在EB病毒阳性细胞中始终表达的抗原。EBNA1内部存在甘氨酸-丙氨酸重复区域,其抑制蛋白酶体复合物对抗原的加工和MHC-I类分子限制的抗原递呈作用,从而逃避杀伤性T细胞介导的细胞免疫。LMP1是明确的癌基因,有促进细胞转化及恶变的作用,参与了EB病毒致癌过程。LMP2基因编码两种蛋白:LMP2A和LMP2B,两者仅N端第一个外显子不同。BamHI的一段区域的这种转录在所有EB病毒阳性的肿瘤中都存在,特别是NPC中。这段转录产物编码至少三个多肽(BARF0,RPMS1和A73),但是这些当爱是否真的存在还没有得到最终确证。
鼻咽癌患者针对EBNA、VCA、EA、MA及DNase均产生相应的IgG和IgA抗体,体液免疫能阻止外源性病毒感染,却不能消灭病毒的潜伏感染,研究这些抗体,对早期筛查和诊断鼻咽癌及监测疗效具有重要意义。应用多聚酶链反应(PCR),并且结核VCA-IgA还可以提高诊断鼻咽癌的灵敏度。
鼻咽癌患者机体可以产生针对EB病毒的特异性CTL细胞应答,CTL在清楚病毒、控制潜伏感染状态的细胞、防止肿瘤发生中具有重要作用。EB病毒潜伏感染时免疫优势表位位于EBNA3家族,鼻咽癌中EBV处于II潜伏感染,主要表达弱免疫原性的EBNA1、LMP1、LMP2蛋白,而不表达EBNA3家族蛋白。EBNA1由于大量甘氨酸-丙氨酸重复序列,阻止HLA-I类分子对其加工、处理和递呈。LMP1是癌基因,具有独立转化细胞的能力,而且在鼻咽癌病人中易发生突变,使转化细胞的能力增强,并逃避体内CTL的识别。故EBNA1和LMP1不合适作为鼻咽癌免疫治疗的靶抗原。LMP2A本身不是转化基因,无致癌性,在鼻咽癌肿瘤细胞能稳定表达,LMP2A的大量HLA限制的T细胞表位已被鉴定出,且能诱导CTL发挥作用。因此,目前认为LMP2A是鼻咽癌免疫治疗最理想的靶抗原。
鼻咽癌的传统治疗方式是手术结合放疗及化疗,这两种治疗手段特别是放疗对鼻咽癌早期患者敏感,但中晚期鼻咽癌患者对放疗及化疗均不敏感,治疗后复发率高。因此以EBV为靶点的细胞免疫治疗为鼻咽癌的综合治疗提供了有力的手段。鼻咽癌(NPC)具备免疫治疗的基本要素。第一,鼻咽癌细胞几乎100%地感染EB病毒。其次,NPC细胞表面有正常表达HLAI类分子以及CD54、CD70等表面标识分子,并且可以通过HLAI累途径将内源性的抗原呈递给CTL识别。第三,尽管EBV诱导多种细胞因子表达,鼻咽癌微环境对CTL活性无明显抑制作用。这些特点提示鼻咽癌是一种适合于免疫治疗的肿瘤。2002年,香港林成龙用已知CTL识别的LMP2多肽(SSC、TYG、IED)负载自体的DC回输治疗晚期鼻咽癌患者,结果显示,16例患者中有9例患者产生持续3个月的抗原表位特异性CTL反应,其中2例有肿瘤的减小。2004年P.Comoli报道用部分HLA匹配的健康携带者的EBV特异性CTL的过继性免疫治疗鼻咽癌。2005年straathof和P.Comoli分别报道了应用自体EBV特异性细胞毒性T淋巴细胞(CTL)对一些晚期鼻咽癌患者进行过继性免疫治疗。
肿瘤特异性T淋巴细胞(CTL)即细胞毒性T淋巴细胞,是从抗原呈递细胞接受了抗原信息,并经过克隆扩增的可特异性识别和杀伤抗原特异性靶细胞的效应T淋巴细胞,CTL是机体清除癌变细胞的主要机制,在抗肿瘤免疫过程中发挥着主要作用。CTL不仅能通过颗粒酶和穿孔素等物质直接杀死肿瘤细胞,还可以通过分泌一些细胞因子和IFN-γ和TNFα等间接地杀伤肿瘤细胞。随着生物医学,基因工程技术的发展,肿瘤特异性T淋巴细胞治疗近年来日益受到重视,显示出良好的应用前景,多种特异性CTL诱导培养方案应运而生。早在2000年日本用过继性T淋巴细胞移植治疗肝癌获得了很好的疗效,复发率降低,生存率提高,研究发表在医学权威杂志《柳叶刀》上;2004年,Rosenburg教授研究的肿瘤浸润淋巴细胞(TIL,特异性CTL的一类)在治疗转移性黑色素瘤上获得了良好的结果。肿瘤特异性CTL治疗肿瘤疾病具有安全,靶向,高效的特点。这主要是由T淋巴细胞表面特异性识别肿瘤抗原的T细胞受体(T Cell Receptor,TCR)决定的。然而机体内针对各种抗原的TCR千差万别,2014年《科学》杂志发表Rosenberg教授的文章,利用TCR免疫组库深度测序技术从转移性胆管上皮细胞癌患者的肿瘤浸润T淋巴细胞群中,筛选并得到了肿瘤抗原特异性的TCR序列,根据序列合成了TCR的DNA,并通过基因工程技术转导在患者自体T细胞表面,获得了良好的治疗效果。
T细胞受体(TCR)是细胞表面受体,参与T细胞的活化以响应抗原的呈现。一般来说,TCR由α和β两条链(其装配以形成异源二聚体)注册,并且与CD3转导亚基相连以在细胞表面上呈现形成T-细胞受体复合物。TCR的每条α和β链由免疫球蛋白样N-端可变(V)和恒定(C)区、疏水跨膜结构域和短的细胞质区域组成。关于免疫球蛋白分子,α和β链的可变区由V(D)J重组产生,在T细胞群中产生抗原特异性的大量多样性。然而,同识别完整抗原的免疫球蛋白相比,T细胞被与MHC分子相关的经处理肽片段活化,通过T细胞将另外的特征引入至抗原识别,被称为MHC限制性。
技术实现要素:
本发明要解决的技术问题是:为了解决上述背景技术中存在的问题,提供一种改进的EB病毒特异性TCR及其重组慢病毒载体,利用慢病毒载体将其转染到T细胞中,获得表达针对EB病毒特异TCR的T细胞。
本发明解决其技术问题所采用的技术方案是:一种EB病毒特异性TCR,包括α链和β链,所述的α链的序列如下:
atgtaggacgcccctccggtcacggcatttctgatagtgcatcgacgtgactcacccgccgacacaggaagagggtggagaaccgtctcgggttccaatggctttttcctagtgttttgagggaaagaaacaatctatatatatactcttctaggcgggcgcccccttcccctcaaactcttttttttcctcctctgccaagctttgtttgttgagaaaaaacaaaaaattcgctcctggtaactctctttccgcctccaggggagtccccaacccggaaaaaacccccccccccccccccccaagtttttttaatctaggtaggcccgcggttggaaaactccccccccccccccccctgaagcctcacacagcccagtaactttgctagtacctcttgagtgcaaggtggagaattaagatctggatttgagacggagcacggaacatttcactcaggggaagagctatgaacatgctgactgccagcctgttgagggcagtcatagcctccatctgtgttgtatccagcatggctcagaaggtaactcaagcgcagactgaaatttctgtggtggagaaggaggatgtgaccttggactgtgtgtatgaaacccgtgatactacttattacttattctggtacaagcaaccaccaagtggagaattggttttccttattcgtcggaactcttttgatgagcaaaatgaaataagtggtcggtattcttggaacttccagaaggatcgctgaagacagaaagtccagtaccttgatcctgcaccgtgctaccttgagagatgctgctgtgtactactgttcagccggtggtgctacaaacaagctcatctttggaactggcactctgcttgctgtccagccaaatatccagaaccctgaccctgccgtgtaccagctgagagactctaaatccagtgacaagtctgtctgcctattcaccgattttgattctcaaacaaatgtgtcacaaagtaaggattctgatgtgtatatcacagacaaaactgtgctagacatgaggtctatggacttcaagagcaacagtgctgtggcctggagcaacaaatctgactttgcatgtgcaaacgccttcaacaacagcattattccagaagacaccttcttccccagcccagaaagttcctgtgatgtcaagctggtcgagaaaagctttgaaacagatacgaacctaaactttcaaaacctgtcagtgattgggttccgaatcctcctcctgaaagtggccgggtttaatctgctcatgacgctgcggctgtggtccagc,所述的β链的序列如下:
ccatcctgccctgaccctgccatgggcaccaggctcctcttctgggtggccttctgtctcctgggggcagatcacacaggagctggagtctcccagtcccccagtaacaaggtcacagagaagggaaaggatgtagagctcaggtgtgatccaatttcaggtcatactgccctttactggtaccgacagagcctggggcagggcctggagtttttaatttacttccaaggcaacagtgcaccagacaaatcagggctgcccagtgatcgcttctctgcagagaggactgggggatccgtctccactctgaccctacacgccctgcagcCAGAAGACTCAGCCCTGTATCTCTGCGCCAGCAGCCAAGACTGGACACCTAATGAGCAGTTCTTCGGGCCAGGGACACGGCTCACCGTGCTAGAGGACCtgaaaaacgtgttcccacccgaggtcgctgtgtttgagccatcagaagcagagatctcccacacccaaaaggccacactggtatgcctggccacaggcttctaccccgaccacgtggagctgagctggtgggtgaatgggaaggaggtgcacagtggggtcagcacagacccgcagcccctcaaggagcagcccgccctcaatgactccagatactgcctgagcagccgcctgagggtctcggccaccttctggcagaacccccgcaaccacttccgctgtcaagtccagttctacgggctctcggagaatgacgagtggacccaggatagggccaaacctgtcacccagatcgtcagcgccgaggcctggggtagagcagactgtggcttcacctccgagtcttaccagcaaggggtcctgtctgccaccatcctctatgagatcttgctagggaaggccaccttgtatgccgtgctggtcagtgccctcgtgcatggccatggtcaagagaaaggattccagaggctagctccaaaaccatcccaggtcattcttcatcctcacccaggattctcctgtacctgctcccaatctgtgttcctaaaagtgattctcactctgcttcatctcctacttacatgaatacttctctcttttttctgtttccctgaagattgagctcccaacccccaagtacgaaataggctaaaccaataaaaaaatggtgtgtt。
一种EB病毒特异性TCR重组慢病毒载体的应用,分别釆取HLA-A2阳性和阴性的健康人的PBMC,以lxl06/ml的密度接种到24孔板,加入600lU/mlIL-2、50ng/mlanti-CD3(OKT-3)的含10%人AB血清AIM-V培养基培养2~3d。Jurkat细胞按Ixl06细胞/ml混于上述慢病毒上清液放于24孔板中,在32℃以l000g速度离心90min,4h后,用新鲜培养液重悬细胞,37℃孵育过夜。两种细胞的感染复数(multiplicity of infection,MOI)均为0,15~0.5,重复感染2次,孵育48~72h后用上流式机检测。
本发明的有益效果是,本发明的一种EB病毒特异性TCR及其重组慢病毒载体与应用筛选出EB病毒抗原特异的TCR,利用慢病毒载体将其转染到T细胞中,获得表达针对EB病毒特异TCR的T细胞。
附图说明
下面结合附图和实施例对本发明进一步说明。
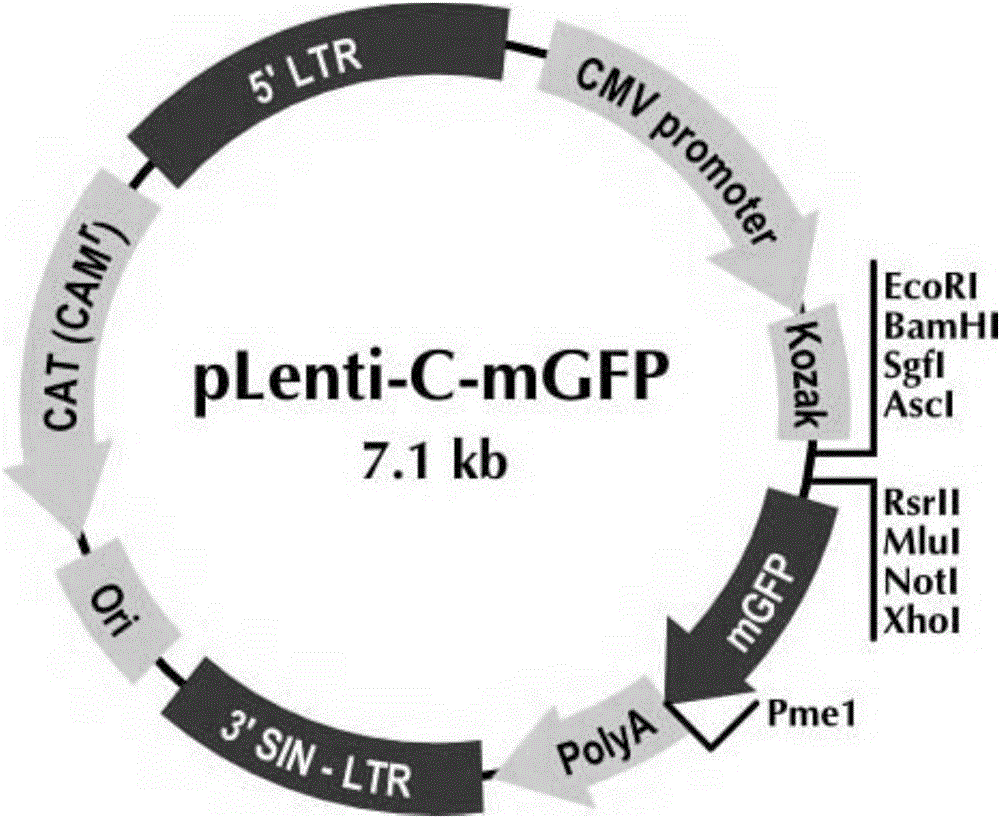
图1是本发明中pLenti-C-mGFP空载体的示意图。
图2是本发明中TCRα和β链重组载体示意图。
具体实施方式
现在结合附图对本发明作进一步详细的说明。这些附图均为简化的示意图,仅以示意方式说明本发明的基本结构,因此其仅显示与本发明有关的构成。
图1和图2所示的一种EB病毒特异性TCR,包括α链和β链,所述的α链的序列如下:
atgtaggacgcccctccggtcacggcatttctgatagtgcatcgacgtgactcacccgccgacacaggaagagggtggagaaccgtctcgggttccaatggctttttcctagtgttttgagggaaagaaacaatctatatatatactcttctaggcgggcgcccccttcccctcaaactcttttttttcctcctctgccaagctttgtttgttgagaaaaaacaaaaaattcgctcctggtaactctctttccgcctccaggggagtccccaacccggaaaaaacccccccccccccccccccaagtttttttaatctaggtaggcccgcggttggaaaactccccccccccccccccctgaagcctcacacagcccagtaactttgctagtacctcttgagtgcaaggtggagaattaagatctggatttgagacggagcacggaacatttcactcaggggaagagctatgaacatgctgactgccagcctgttgagggcagtcatagcctccatctgtgttgtatccagcatggctcagaaggtaactcaagcgcagactgaaatttctgtggtggagaaggaggatgtgaccttggactgtgtgtatgaaacccgtgatactacttattacttattctggtacaagcaaccaccaagtggagaattggttttccttattcgtcggaactcttttgatgagcaaaatgaaataagtggtcggtattcttggaacttccagaaggatcgctgaagacagaaagtccagtaccttgatcctgcaccgtgctaccttgagagatgctgctgtgtactactgttcagccggtggtgctacaaacaagctcatctttggaactggcactctgcttgctgtccagccaaatatccagaaccctgaccctgccgtgtaccagctgagagactctaaatccagtgacaagtctgtctgcctattcaccgattttgattctcaaacaaatgtgtcacaaagtaaggattctgatgtgtatatcacagacaaaactgtgctagacatgaggtctatggacttcaagagcaacagtgctgtggcctggagcaacaaatctgactttgcatgtgcaaacgccttcaacaacagcattattccagaagacaccttcttccccagcccagaaagttcctgtgatgtcaagctggtcgagaaaagctttgaaacagatacgaacctaaactttcaaaacctgtcagtgattgggttccgaatcctcctcctgaaagtggccgggtttaatctgctcatgacgctgcggctgtggtccagc,所述的β链的序列如下:
ccatcctgccctgaccctgccatgggcaccaggctcctcttctgggtggccttctgtctcctgggggcagatcacacaggagctggagtctcccagtcccccagtaacaaggtcacagagaagggaaaggatgtagagctcaggtgtgatccaatttcaggtcatactgccctttactggtaccgacagagcctggggcagggcctggagtttttaatttacttccaaggcaacagtgcaccagacaaatcagggctgcccagtgatcgcttctctgcagagaggactgggggatccgtctccactctgaccctacacgccctgcagcCAGAAGACTCAGCCCTGTATCTCTGCGCCAGCAGCCAAGACTGGACACCTAATGAGCAGTTCTTCGGGCCAGGGACACGGCTCACCGTGCTAGAGGACCtgaaaaacgtgttcccacccgaggtcgctgtgtttgagccatcagaagcagagatctcccacacccaaaaggccacactggtatgcctggccacaggcttctaccccgaccacgtggagctgagctggtgggtgaatgggaaggaggtgcacagtggggtcagcacagacccgcagcccctcaaggagcagcccgccctcaatgactccagatactgcctgagcagccgcctgagggtctcggccaccttctggcagaacccccgcaaccacttccgctgtcaagtccagttctacgggctctcggagaatgacgagtggacccaggatagggccaaacctgtcacccagatcgtcagcgccgaggcctggggtagagcagactgtggcttcacctccgagtcttaccagcaaggggtcctgtctgccaccatcctctatgagatcttgctagggaaggccaccttgtatgccgtgctggtcagtgccctcgtgcatggccatggtcaagagaaaggattccagaggctagctccaaaaccatcccaggtcattcttcatcctcacccaggattctcctgtacctgctcccaatctgtgttcctaaaagtgattctcactctgcttcatctcctacttacatgaatacttctctcttttttctgtttccctgaagattgagctcccaacccccaagtacgaaataggctaaaccaataaaaaaatggtgtgtt。
一种EB病毒特异性TCR重组慢病毒载体的应用,分别釆取HLA-A2阳性和阴性的健康人的PBMC,以lxl06/ml的密度接种到24孔板,加入600lU/mlIL-2、50ng/mlanti-CD3(OKT-3)的含10%人AB血清AIM-V培养基培养2~3d。Jurkat细胞按Ixl06细胞/ml混于上述慢病毒上清液放于24孔板中,在32℃以l000g速度离心90min,4h后,用新鲜培养液重悬细胞,37℃孵育过夜。两种细胞的感染复数(multiplicity of infection,MOI)均为0,15~0.5,重复感染2次,孵育48~72h后用上流式机检测。
本发明的有益效果是,本发明的一种EB病毒特异性TCR及其重组慢病毒载体与应用筛选出EB病毒抗原特异的TCR,利用慢病毒载体将其转染到T细胞中,获得表达针对EB病毒特异TCR的T细胞。
在正常的T细胞中,T细胞受体从由不成熟的胸腺细胞表达的前-T细胞受体(pTCR)放出,并且对于从双阴性(CD4-CD8-)至双阳性(CD4+CD8+)阶段的T细胞发展是至关重要的。在TCRβ基因座成功地有效重排的前T细胞表达功能性TCRβ链,该TCRβ链与不变的前Tα链和CD3信号组件配对以形成前TCR复合物。
T细胞抗原受体(T cell receptor,TCR)是所有T细胞表面的特征性标志,在T细胞抗原识别中起关键作用。TCR是由α、β两条肽链构成的异二聚体,每条肽链又可分为可变区(V区),恒定区(C区),跨膜区和胞质区等几部分;其胞质区很短,信号传递主要通过与其以非共价键结合的aD3分子进行。TaR分子属于免疫球蛋白超家族,其抗原特异性存在于V区;V区(Vα、Vβ)又各有三个高变区aDRl、aDR2、aDR3,其中以aDR3变异最大,直接决定了TCR的抗原结合特异性。在TCR识别MHC-抗原肽复合体时,CDRl、CDR2识别和结合MHC分子抗原结合槽的侧壁,而CDR3直接与抗原肽相结合。
根据TCR Vα、Vβ基因的同源性,可将80多个TCR Vα基因分为32个家族、60多个TCR Vβ基因分为24个家族。利用每个T细胞克隆均有其独特CDR3序列的特点,采用CDR3谱型分析技术,可测定各TCR家族各CDR3出现的频率,由此反映T细胞的克隆性。未接受抗原刺激的T细胞中,针对各种抗原的T细胞克隆分布均匀,表现为多家族和多克隆性,具体地,表现为各家族均出现呈高斯分布的约8个CDR3峰;抗原刺激则引起识别该抗原的某一个或几个特异TCR家族T细胞反应性增生,表现为该家族CDR3成员出现少于4个峰的寡克隆或单克隆分布,其中具有单克隆CDR3分布(表现为单峰)的TCR家族即是抗原特异单克隆增生的TCR家族。对该家族PCR产物进行测序,可获得抗原特异TCR CDR3序列。
1.5 EBV表位特异性CD8+T细胞的获得
1.5.1 Ficoll-Paque梯度离心法分离鼻咽癌患者外周血单个核细胞(PBMC)
1.5.1.1将淋巴细胞分离液按1:1比例加入到离心管中,离心1500rpm,10min,去上层血清。
1.5.1.2按照血细胞:PBS=1:3的比例,将用PBS稀释后的血细胞溶液缓慢加入到装有淋巴细胞分离液的离心管中,离心2500rpm,25min。
1.5.1.3离心后管内分为4层,最上层为血衆,最下层为红细胞,其上有一薄层粒细胞,中间为淋巴细胞分离液,血裝与分离液之间有一层白膜层即为单个核细胞,单个核细胞包括单核细胞和T/B淋巴细胞。用玻璃吸管吸出白膜层液体至10ml离心管中,加PBS至10ml,离心2000rpm,10min。
1.5.1.4弃上清,加PBS至10ml,吹打混勾,用台盼蓝染色计数,离心1500rpm,10min。
1.5.1.5弃上清后,加含10%FBS的RPMI-1640重悬细胞,调整细胞浓度至lxl07/ml备用。
1.5.2特异性CD8+T细胞的诱导扩增
用LMP2A356-364(多肽序列:FLYALALLL)抗原多肽诱导患者的PBMC,以使特异性的CD8+T细胞增殖达到一定的量,足够用于下一步的实验所需要的细胞数量。将新鲜分离的PBMC按5X109/L悬于AIM-V培养基中,加入抗原肽孵育6h,然后于各孔中加入含80ml/L人类AB血清的RPMI 1640培养液,并添加细胞因子IL-2 40U/mK IL-7 20U/ml以及抗CD28抗体2mg/L。每隔7d半量换液。隔周取少量细胞进行Pentamer染色后用流式细胞术(FCM)检测特异性CD8+T细胞频率,其余细胞半量换液,继续培养。
1.5,3 MACS磁珠和流式细胞术(flow cytometry,FCM)分选特异性CD8+T细胞。
应用MACS磁珠分选试剂盒富集出CD8+T细胞,用突光标记的抗CD3抗体、抗CD8抗体和Pentamer染色,用FCM分选出CD3+CD8+pentamer+T细胞,染色步骤如下:
1.5.3.1在预冷的离心机离心,转速14000g,时间为5-10min。(保持试剂在冰上避光)。
1.5.3.2每次染色以1X106~2X106细胞为准。
1.5.3.3用2ml Wash buffer(0.1%sodium azide,0.1%BSA的PBS)清洗细胞后,以500g的转速离心5min,弃上清,用残余液重悬(<50μl)。始终保持预冷状态。
1.5.3.4每次加入10ul pentamer来标记细胞,用吸管混勾。
1.5.3.5室温避光孵育10min。
1.5.3.6同步骤1.5.3.3.
1.5.3.7加入适量抗CD8抗体,抗CD3抗体,用吸管混匀。
1.5.3.8冰上避光孵育20min。
1.5.3.9清洗细胞两次,步骤同步骤1.5.3.3,混勻每个管。
1.5.3.10加入200μl固定液。上机检测。(固定液可使细胞不聚团,上机前将样品可放于冰箱避光。固定后细胞形态变化,故在进行上机分析前离开样品3h是合理的。样品最多可以保存2天)。
而后继续用抗原多肽诱导其余的PBMC以使特异性CD8+T细胞增殖。将CD3+CD8+Pentamers+T细胞分选到96孔U型培养板中培养,分选前用抗CD3抗体(1mg/L)包被96孔U型培养板过夜。细胞分选的细胞数分别为每孔1、5、20、100、500、1000个CD3+CD8+Pentamers+T细胞,分选后于每孔中加入150ul含100ml/L胎牛血清(FBS)的GIBECO RPMI 1640培养液,添加细胞因子IL-2 1000U/ml,抗CD28抗体200μg/L,培养10-14d。
1.7CDNA5'末端快速扩增(5'RACE)TCR基因双链及分析
1.7.15'RACE cDNA的制备
1.7.1.1准备好如下缓冲液混合物,2μl 5X First-Strand buffer,1.0μl DTT,1.0μl dNTPMix,共4μl,混合好后简要离心一下,室温放置。
1.7.1.2把步骤1.6获得的RNA2.75μl及1.0μl 5'-CDS引物A加入到200μl离心管中,充分混匀并瞬时离心。
1.7.1.3 72℃孵育离心管3min,然后42℃冷却2min,4℃放置。冷却后,14000g离心10s,收集混合物到管底。
1.7.1.4准备好如下主要混合液,室温下按顺序混合以下试剂:4.0μl步骤1的混合物缓冲液,0.25μl RNA酶抑制剂(40U/μl)、1.0μlSMARTScibe逆转录酶共5.25μl。
1.7.1.5把上述5.25μl主混合物与第五步的变性RNA及SMARTer IIA引物lμl混在一起构成10μl体系;
1.7.1.6轻吹混勾体系,瞬时离心使试剂富集管底;
1.7.1.7 42℃孵育90min;70℃加热10分钟;用Tricine-EDTA稀释产物,总RNA<200ng,则加20μl,否则,加100μl;保存产物于-20℃。获得的cDNA 5'端均含有片段UMP(CTAATACGACTCACTATAGGGCAAGCAG-TGGTATCAACGCAGAGT),可作为下一步实验的引物。
1.7.2用5'RACE获得TCR分子α链和β链的可变区基因
应用UMP(CTAATACGACTCACTATAGGGCAAGCAGTGGTATCAACGCAGAGT)作为上游外引物,及其上游内引物NUP(AAGCAGTGGTATCAACGC-AGAGT,取自UMP上),而α、β链上则采取αdown3、αdown4和βdown4、βdown4作为下游内外引物。应用5μl 1.6获得的cDNA为模板,应用SMARTer II A试剂盒的反应液(含有TAP酶、dNTP等,具体不详),构成5μl反应体系。第一轮PCR反应引物为上述的外引物,条件为:94℃5min;94℃30s,72℃3min 5个循环;94℃30s,70℃30s,72℃3min5个循环;94℃30s,66℃30s,72℃3min 27循环;72℃5min,68℃5min,4℃保存。
1.8将获得的α链和β链全长基因连入pLenti-C-mGFP载体,应用Xho Ⅰ内切酶把1.10获得TCR Vβ链从T-easy载体上切下,用Sal Ⅰ酶将pLenti-C-mGFP载体(如图2)上的Sal Ⅰ限制位点切开,酶切产物电泳后按1.9.1的方法胶回收目的条带,然后进行去磷酸化反应,将反应液放入37℃温箱30min,然后置65℃水浴30min,加热灭活。
实施例:重组病毒转导TCR在细胞表面的表达
分别釆取HLA-A2阳性和阴性的健康人的PBMC,以lxl06/ml的密度接种到24孔板,加入600lU/ml IL-2、50ng/ml anti-CD3(OKT-3)的含10%人AB血清AIM-V培养基培养2~3d。Jurkat细胞按Ixl06细胞/ml混于上述慢病毒上清液放于24孔板中,在32℃以l000g速度离心90min,4h后,用新鲜培养液重悬细胞,37℃孵育过夜。两种细胞的感染复数(multiplicity of infection,MOI)均为0,15~0.5,重复感染2次。孵育48~72h后用上流式机检测。应用CD3-percp,CD8-FITC/CD8-APC,HLA-A201-LMP2A356-364pentamer-PE,anti-vpl3TCR-PE,染色,上机检测验证重组TCR分子的表达情况。pentamer染色步骤同1.5.3所示方法,对于不染pentamer的抗体染色步骤具体如下:
1.13.3.1准备1xPBS(无需孵育),流式管,所染抗体。
1.13.3.2将所需染色的足量细胞加入流式管中,再加入ImlPBS,短暂震荡后,以1500rpm,离心5min。
1.13.3.3离心后迅速弃去上清,加入适量抗体(anti-vβl3.1TCR-PE 10μl/test,CD3-Percp 5μl/test,CD8-FITC/CD8-APC 5μl/test),短暂震荡后,室温避光20min。
1.13.3.4加入1ml 1xPBS,短暂震荡,1500rpm,5min离心。重复一次。
1.13.3.5加入200μl固定液1%的多聚甲酸,震荡,上机检测。
以上述依据本发明的理想实施例为启示,通过上述的说明内容,相关工作人员完全可以在不偏离本项发明技术思想的范围内,进行多样的变更以及修改。本项发明的技术性范围并不局限于说明书上的内容,必须要根据权利要求范围来确定其技术性范围。
α链的序列如下:
atgtaggacgcccctccggtcacggcatttctgatagtgcatcgacgtgactcacccgccgacacaggaagagggtggagaaccgtctcgggttccaatggctttttcctagtgttttgagggaaagaaacaatctatatatatactcttctaggcgggcgcccccttcccctcaaactcttttttttcctcctctgccaagctttgtttgttgagaaaaaacaaaaaattcgctcctggtaactctctttccgcctccaggggagtccccaacccggaaaaaacccccccccccccccccccaagtttttttaatctaggtaggcccgcggttggaaaactccccccccccccccccctgaagcctcacacagcccagtaactttgctagtacctcttgagtgcaaggtggagaattaagatctggatttgagacggagcacggaacatttcactcaggggaagagctatgaacatgctgactgccagcctgttgagggcagtcatagcctccatctgtgttgtatccagcatggctcagaaggtaactcaagcgcagactgaaatttctgtggtggagaaggaggatgtgaccttggactgtgtgtatgaaacccgtgatactacttattacttattctggtacaagcaaccaccaagtggagaattggttttccttattcgtcggaactcttttgatgagcaaaatgaaataagtggtcggtattcttggaacttccagaaggatcgctgaagacagaaagtccagtaccttgatcctgcaccgtgctaccttgagagatgctgctgtgtactactgttcagccggtggtgctacaaacaagctcatctttggaactggcactctgcttgctgtccagccaaatatccagaaccctgaccctgccgtgtaccagctgagagactctaaatccagtgacaagtctgtctgcctattcaccgattttgattctcaaacaaatgtgtcacaaagtaaggattctgatgtgtatatcacagacaaaactgtgctagacatgaggtctatggacttcaagagcaacagtgctgtggcctggagcaacaaatctgactttgcatgtgcaaacgccttcaacaacagcattattccagaagacaccttcttccccagcccagaaagttcctgtgatgtcaagctggtcgagaaaagctttgaaacagatacgaacctaaactttcaaaacctgtcagtgattgggttccgaatcctcctcctgaaagtggccgggtttaatctgctcatgacgctgcggctgtggtccagc
β链的序列如下:
ccatcctgccctgaccctgccatgggcaccaggctcctcttctgggtggccttctgtctcctgggggcagatcacacaggagctggagtctcccagtcccccagtaacaaggtcacagagaagggaaaggatgtagagctcaggtgtgatccaatttcaggtcatactgccctttactggtaccgacagagcctggggcagggcctggagtttttaatttacttccaaggcaacagtgcaccagacaaatcagggctgcccagtgatcgcttctctgcagagaggactgggggatccgtctccactctgaccctacacgccctgcagcCAGAAGACTCAGCCCTGTATCTCTGCGCCAGCAGCCAAGACTGGACACCTAATGAGCAGTTCTTCGGGCCAGGGACACGGCTCACCGTGCTAGAGGACCtgaaaaacgtgttcccacccgaggtcgctgtgtttgagccatcagaagcagagatctcccacacccaaaaggccacactggtatgcctggccacaggcttctaccccgaccacgtggagctgagctggtgggtgaatgggaaggaggtgcacagtggggtcagcacagacccgcagcccctcaaggagcagcccgccctcaatgactccagatactgcctgagcagccgcctgagggtctcggccaccttctggcagaacccccgcaaccacttccgctgtcaagtccagttctacgggctctcggagaatgacgagtggacccaggatagggccaaacctgtcacccagatcgtcagcgccgaggcctggggtagagcagactgtggcttcacctccgagtcttaccagcaaggggtcctgtctgccaccatcctctatgagatcttgctagggaaggccaccttgtatgccgtgctggtcagtgccctcgtgcatggccatggtcaagagaaaggattccagaggctagctccaaaaccatcccaggtcattcttcatcctcacccaggattctcctgtacctgctcccaatctgtgttcctaaaagtgattctcactctgcttcatctcctacttacatgaatacttctctcttttttctgtttccctgaagattgagctcccaacccccaagtacgaaataggctaaaccaataaaaaaatggtgtgtt
- 还没有人留言评论。精彩留言会获得点赞!