一种锗酸盐绿色长余辉发光材料及其制备方法与流程
本发明涉及一种绿色长余辉发光材料,特别是涉及能在紫外区有宽谱带吸收并在绿光区域呈宽谱带发射的高效能的长余辉发光材料,具体涉及一种亮度是长辉绿粉2(1-i)ZnO.(1+x)GeO2.yMgF2:iMn2+,亮度是Zn2GeO4:Mn2+的两倍,是商业长辉绿粉SrAl2O4:Eu2+,Dy3+的三倍,且余辉比Zn2GeO4:Mn2+显著增强,余辉时间长达1~5小时。
背景技术:
从20世纪初以来,长余辉发光材料都因其广泛的应用价值而倍受人们关注。其中与我们生活密切相关的有紧急照明、交通标志、平面艺术、室内装潢等,目前人们也不断的开发并实现其信息存储及蓄电池的应用价值。[T.Matsuzawa,Y.Aoki,N.Takeuchi,Y.Murayama,J.Electrochem.Soc.143(1996)2670;M.Kowatari,D.Koyama,Y.Satoh,K.Linuma,S.Uchida,Nucl.Instr.Methods.Phys.Res.Sect.A.480(2002)431-439.]常见的长余辉材料可以分为传统的硫化物、稀土掺杂的硫化物、稀土掺杂的硅酸盐、及稀土掺杂的碱土铝酸盐。传统的硫化物(如ZnS:Cu)和稀土掺杂的硫化物(如CaS:Eu2+)虽发射区域可覆盖蓝光到红光的可见光范围而使发光颜色多样性,但是其化学稳定性差、在紫外光照射下易分解且经光衰试验后荧光粉效率严重下降,更有硫溢出而逐渐被化学性质稳定的稀土掺杂的硅酸盐所取代,但是硅酸盐其发光性能远远不及目前已到达商业化生产的稀土掺杂的碱土铝酸盐长余辉材料。最具有代表性的铝酸盐有发蓝光的CaAl2O4:Eu2+,Nd3+、发红光的Y2O2S:Eu3+,Ti4+,Mn2+及发绿光的SrAl2O4:Eu2+,Dy3+。[T.Aitasalo,P.Deren,J.Holsa,H.Jungner,J.C.Krupa,M.Lastusaari,J.Legendziewicz,J.Niittykoski,W.Strek,J.Solid.State.Chem.171(2003)114;T.Matsuzawa,Y.Aoki,N.Takeuchi,Y.Murayama,J.Electrochem.Soc.143(1996)2670;Y.Murazaki,K.Arai,K.Ichinomiya,Jpn.Rare.Earths.35(1999)41.]
对于长余辉绿粉SrAl2O4:Eu2+,Dy3+主要通过Dy3+不等价置换Sr2+离子创造了合适深度的电子陷阱与空穴陷阱而具有高效能的发光效率及超强余辉而占据着商业市场,但是该商业绿粉遇水易水解[X.D.Lü,Mater.Chem.Phys.93(2005)526-530.]且耐热性差在650℃就易发生相变[M.Avdeev,S.Yakovlev,A.A.Yaremchenko,V.V.Kharton,J.Solid State Chem.180,(2007)3535.]而大大的限制了其的应用范围,从而无法满足市场的各种照明的需求。
研究报道Zn2GeO4因其独特的化学结构可作为过渡金属离子有效敏化的很好的基质材料,绿粉Zn2GeO4:Mn2+具有电致发光与阴极射线发光性质,比如可有效被锰离子进行激发而发射明亮的绿光,而可广泛应用到各种显示器及TFELDs。[T.Minami,T.Maeno,Y.Kuroi,S.Takata,Jpn.J.Appl.Phys.,Part 2,34(1995)L684;L.E.Shea,R.K.Datta,J.J.J.Brown,J.Electrochem.Soc.,141,2198(1994);S.Itoh,H.Toki,K.Morimoto,T.Kishino,J.Electrochem.Soc.,138(1991)1509.]
技术实现要素:
本发明的目的在于克服现有技术的缺点,利用最易实现大规模应用的高温固相法,在空气中直接合成一种达到商业化应用要求的绿色长余辉发光材料,其亮度是Zn2GeO4:Mn2+的两倍,是商业长辉绿粉SrAl2O4:Eu2+,Dy3+的三倍,且余辉比Zn2GeO4:Mn2+显著增强,余辉时间长达1~5小时。本发明的产品基质稳定,完全克服了商业长辉绿粉SrAl2O4:Eu2+,Dy3+的遇水易水解及高温相变的缺点,从而可大大满足人们对长余辉绿粉的市场需求。
本发明的目的通过如下技术方案实现:
一种绿色长余辉发光材料的化学组成为:2(1-i)ZnO.(1+x)GeO2.yMgF2:iMn2+,其中0.1≤x≤5,0.01≤y≤0.16,0.001≤i≤0.08。
该材料激发光谱在紫外区域呈宽谱带(250~400nm),发射光谱(490~570nm)在绿光区域呈宽谱带。对于该发光材料,在Mn2+掺杂浓度相同的情况下,在Zn2GeO4基质中加入适量的GeO2与MgF2,即当原料配比为ZnO/GeO2/MgF2=2∶2.5∶0.08.时,亮度是Zn2GeO4:Mn2+的两倍,是商业长辉绿粉SrAl2O4:Eu2+,Dy3+的三倍,且余辉比Zn2GeO4:Mn2+显著增强,余辉时间长达1~5小时,而且基质稳定不易水解。
所述绿色长余辉发光材料的制备方法为高温固相法,即将用氧化锌、氧化锗、氟化镁及醋酸锰,按照计量比ZnO∶GeO2∶MgF2∶Mn2+=2(1-i)∶(1+x)∶y∶i,其中0.1≤x≤5,0.01≤y≤0.16,0.001≤i≤0.08。将固体原料准确称量并研磨30~45分钟使其混合均匀,分别在600~800℃与900~1100℃空气中烧结3~5小时,冷却即得产品。与现有技术相比,本发明具有以下优点和效果:
(1)本发明的一种绿色长余辉发光材料亮度高达商业长辉绿粉SrAl2O4:Eu2+,Dy3+的三倍,余辉远远超过绿粉Zn2GeO4:Mn2+的余辉长度的绿光材料,而且基质稳定不易水解。
(2)本产品激发光谱在紫外区域呈宽谱带(250~400nm),发射光谱(490~570nm)在绿光区域呈宽谱带,发光效率高。
(3)本产品利用高温固相法,使得制备方法简单、易操作,制备过程中无毒害气体产生从而无污染,而且在空气中合成,使得对设备的要求降低更有利于大规模的工业生产,合成条件温和,更有利于中试与投产。
附图说明
图1:(a)已知的绿光材料2(1-0.02)ZnO.1.5GeO2:0.02Mn2+的XRD谱图;(b)为本发明实施例4中所得绿光材料2(1-0.02)ZnO.1.5GeO2:0.02Mn2+的XRD谱图;(c)为本发明实施例8中所得绿光材料2(1-0.02)ZnO.1.5GeO2.0.08MgF2:0.02Mn2+的XRD谱图。(注明:″*″表示GeO2,″○″表示MgGeO3)
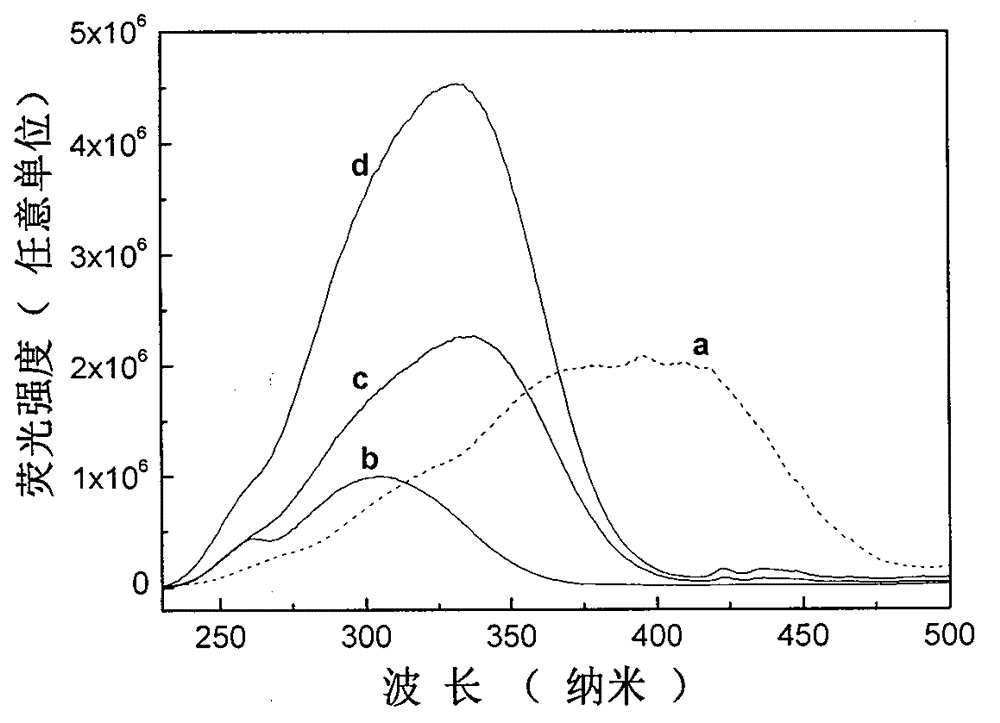
图2:(a)为商业绿粉SrAl2O4:Eu2+,Dy3+、(b)为已知的绿光材料2(1-0.02)ZnO.1.5GeO2:0.02Mn2+、(c)为本发明实施例4中所得绿光材料2(1-0.02)ZnO.2GeO2:0.02Mn2+、(d)为本发明实施例9中所得绿光材料2(1-0.02)ZnO.2GeO2.0.1MgF2:0.02Mn2+在336nm波长激发下的发射谱图。
图3:(a)为商业绿粉SrAl2O4:Eu2+,Dy3+在513nm波长监测下的激发谱图;(b)已知的绿光材料2(1-0.02)ZnO.1.5GeO2:0.02Mn2+、(c)为本发明实施例4中所得绿光材料2(1-0.02)ZnO.2GeO2:0.02Mn2+、(d)为本发明实施例9中所得绿光材料2(1-0.02)ZnO.2GeO2.0.1MgF2:0.02Mn2+在530nm波长监测下的激发谱图。
图4:(a)为已知的绿光材料2(1-0.02)ZnO.1.5.GeO2:0.02Mn2+、(b)为本发明实施例9中所得绿光材料2(1-0.02)ZnO.2GeO2.0.1MgF2:0.02Mn2+、(c)为本发明实施例4中所得绿光材料2(1-0.02)ZnO.2GeO2:0.02Mn2+的、(d)为本发明实施例12中所得绿光材料2(1-0.02)ZnO.1.5GeO2.0.1MgF2:0.02Mn2+的热释光谱。
具体实施方式
下面结合实施例和附图对本发明作进一步详细的描述,但本发明要求保护的范围并不局限于实施例表示的范围。
【该材料的化学组成为2(1-i)ZnO.(1+x)GeO2.yMgF2:iMn2+,其中0.1≤x≤5,0.01≤y≤0.16,0.001≤i≤0.08。用氧化锌、氧化锗、氟化镁及醋酸锰为原料,利用高温固相法,将固体原料研磨混合均匀,分别在600~800℃与900~1100℃空气中烧结3~5小时。该材料在紫外灯的照射下,发明亮绿光,亮度远高于Zn2GeO4:Mn2+与SrAl2O4:Eu2+,Dy3+,余辉时间长达1~5小时.】【这段定稿的时候会删除。红色的是范围,在实施例中至少要出现首、尾、中间三个数据。实施例可增加(数量不限)。】
实施例1
按照ZnO∶GeO2∶Mn2+=2(1-0.02)∶1.5∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、0.7845固体氧化锗GeO2(分析纯)、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨30分钟,使混合均匀得混合物。在空气条件下,将混合物置于700℃的马弗炉中熔融5小时,冷却后取出,再次研磨10分钟,得前驱物,将前驱物放入与-1100℃的空气中烧结3小时,冷却取出,即得产品。利用XRD粉末衍射仪(Bruker D8Advance)在室温条件下检测产品的物相,如图1a所示,XRD显示产物是纯的Zn2GeO4相;该材料在紫外灯照射下发射明亮绿光;利用Fluoromax-4荧光光谱仪(HORIBA Jobin Yvon Inc.),在室温条件下检测产品的发光性能,该产品在336nm波长激发发射在绿光区域490~570nm的宽谱带(具体可见图2b),由于该产品激发光谱在紫外区域呈宽谱带(250~400nm),则可应用于近紫外 白光LEDs(具体可见图3b)。从热释光谱显示(如图4a),其余辉强度较弱。
实施例2
按照ZnO∶GeO2∶Mn2+=2(1-0.001)∶1.5∶0.001摩尔比,分别准确称量0.8131g固体氧化锌ZnO(分析纯)、0.7845g固体氧化锗GeO2(分析纯)、0.0012g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨20分钟,使混合均匀得混合物。在空气条件下,将混合物置于600℃的马弗炉中熔融4小时,冷却后取出,再次研磨20分钟,得前驱物,将前驱物放入与1000℃的空气中烧结4小时,冷却取出,即得产品。利用XRD粉末衍射仪(Bruker D8Advance)在室温条件下检测产品的物相,显示产物是纯的Zn2GeO4相;利用Fluoromax-4荧光光谱仪(HORIBA Jobin Yvon Inc.),在室温条件下检测产品的发光性能,该产品在336nm波长激发发射在绿光区域490~570nm的宽谱带,且该产品激发光谱在紫外区域呈宽谱带(250~400nm),则可应用于近紫外白光LEDs。其发光强度弱于实施例1中得到的产品的发光强度。
实施例3
按照ZnO∶GeO2∶Mn2+=2(1-0.08)∶1.5∶0.08摩尔比,分别准确称量0.7487g固体氧化锌ZnO(分析纯)、0.7845g固体氧化锗GeO2(分析纯)、0.0980g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨30分钟,使混合均匀得混合物。在空气条件下,将混合物置于800℃的马弗炉中熔融3小时,冷却后取出,再次研磨20分钟,得前驱物,将前驱物放入与900℃的空气中烧结5小时,冷却取出,即得产品。利用XRD粉末衍射仪(Bruker D8Advance)在室温条件下检测产品的物相,显示产物是纯的Zn2GeO4相;利用Fluoromax-4荧光光谱仪(HORIBA Jobin Yvon Inc.),在室温条件下检测产品的发光性能,该产品在336nm波长激发发射在绿光区域490~570nm的宽谱带,且该产品激发光谱在紫外区域呈宽谱带(250~400nm),则可应用于近紫外白光LEDs。其发光强度也弱于实施例1中得到的产品的发光强度。
实施例4
按照ZnO∶GeO2∶Mn2+=2(1-0.02)∶2∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、1.0460g固体氧化锗GeO2(分析纯)、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨20分钟,使混合均匀得混合物。在空气条件下,将混合物置于800℃的马弗炉中熔融4小时,冷却后取出,再次研磨20分钟,得前驱物,将前驱物放入与1100℃的空气中烧结4小时,冷却取出,即得产品。利用XRD粉末衍射仪(Bruker D8Advance)在室温条件下检测产品的物相,如图1b所示,XRD显示产物是Zn2GeO4相和GeO2的混合相;该材料在紫外灯照射下发射明亮绿光,且亮度比商业绿粉SrAl2O4:Eu2+,Dy3+稍强,余辉强度(如图4c)稍超过绿粉Zn2GeO4:Mn2+;利用Fluoromax-4荧光光谱仪(HORIBA Jobin Yvon Inc.), 在室温条件下检测产品的发光性能,该产品在336nm波长激发发射在绿光区域490~570nm的宽谱带(具体可见图2c),由于该产品激发光谱在紫外区域呈宽谱带(250~400nm),则可应用于近紫外白光LEDs(具体可见图3c)。GeO2在体系中起着助熔剂的作用,降低结晶温度,提高多晶颗粒的结晶度,非常有利于提高Zn2GeO4:Mn2+发光材料的发光强度。
实施例5
按照ZnO∶GeO2∶Mn2+=2(1-0.02)∶1.1∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、0.5753g固体氧化锗GeO2(分析纯)、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨30分钟,使混合均匀得混合物。在空气条件下,将混合物置于600℃的马弗炉中熔融3小时,冷却后取出,再次研磨10分钟,得前驱物,将前驱物放入与1000℃的空气中烧结5小时,冷却取出,即得产品。利用Fluoromax-4荧光光谱仪(HORIBA Jobin Yvon Inc.),在室温条件下检测产品的发光性能,该产品同样在336nm波长激发发射在绿光区域490~570nm的宽谱带,由于该产品激发光谱在紫外区域呈宽谱带(250~400nm),则可应用于近紫外白光LEDs。该产品的发光强度稍高于实施例1中所得的产品的发光强度。
实施例6
按照ZnO∶GeO2∶Mn2+=2(1-0.02)∶6∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、3.138g固体氧化锗GeO2(分析纯)、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨20分钟,使混合均匀得混合物。在空气条件下,将混合物置于700℃的马弗炉中熔融5小时,冷却后取出,再次研磨20分钟,得前驱物,将前驱物放入与1000℃的空气中烧结3小时,冷却取出,即得产品。利用XRD粉末衍射仪(Bruker D8Advance)在室温条件下检测产品的物相,显示产物也是Zn2GeO4相和GeO2的混合相:利用Fluoromax-4荧光光谱仪(HORIBA Jobin Yvon Inc.),在室温条件下检测产品的发光性能,该产品同样在336nm波长激发发射在绿光区域490~570nm的宽谱带,该产品激发光谱在紫外区域呈宽谱带(250~400nm),则可应用于近紫外白光LEDs。
实施例7
按照ZnO∶GeO2∶Mn2+=2(1-0.02)∶1.1∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、0.5753g固体氧化锗GeO2(分析纯)、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨30分钟,使混合均匀得混合物。在空气条件下,将混合物置于800℃的马弗炉中熔融4小时,冷却后取出,再次研磨10分钟,得前驱物,将前驱物放入与900℃的空气中烧结4小时,冷却取出,即得产品。利用Fluoromax-4荧光光谱仪(HORIBA Jobin Yvon Inc.),在室温条件下检测产品的发光性能,该产品同样在336nm波长激发发射在绿光区域 490~570nm的宽谱带,由于该产品激发光谱在紫外区域呈宽谱带(250~400nm),则可应用于近紫外白光LEDs。该产品的发光强度稍高于实施例1中所得的产品的发光强度。
实施例8
按照ZnO∶GeO2∶MgF2∶Mn2+=2(1-0.02)∶1.5∶0.08∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、0.7845g固体氧化锗GeO2(分析纯)、0.0249g固体氟化镁MgF2、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨30分钟,使混合均匀得混合物。在空气条件下,将混合物置于600℃的马弗炉中熔融4小时,冷却后取出,再次研磨10分钟,得前驱物,将前驱物放入与1000℃的空气中烧结4小时,冷却取出,即得产品。利用XRD粉末衍射仪(Bruker D8Advance)在室温条件下检测产品的物相,如图1c所示,XRD显示产物是Zn2GeO4相和MgGeO3的混合相,结果表明MgF2在此体系中不仅起到起着助熔剂的作用,降低了结晶温度,提高多晶颗粒的结晶度,而且MgF2并未以MgF2形式生存在而是与GeO2成了MgGeO3,从而降低了Mn离子之间的无辐射弛豫,从而提高Zn2GeO4:Mn2+发光材料的发光强度。
实施例9
按照ZnO∶GeO2∶MgF2∶Mn2+=2(1-0.02)∶1.5∶0.1∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、0.7845g固体氧化锗GeO2(分析纯)、0.0312g固体氟化镁MgF2、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨30分钟,使混合均匀得混合物。在空气条件下,将混合物置于800℃的马弗炉中熔融4小时,冷却后取出,再次研磨20分钟,得前驱物,将前驱物放入与1000℃的空气中烧结5小时,冷却取出,即得产品。如图4d所示,该产品的余辉强度大大超过了Zn2GeO4:Mn2+的强度。
实施例10
按照ZnO∶GeO2∶MgF2∶Mn2+=2(1-0.02)∶1.5∶0.01∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、0.7845g固体氧化锗GeO2(分析纯)、0.0031g固体氟化镁MgF2、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨20分钟,使混合均匀得混合物。在空气条件下,将
混合物置于600℃的马弗炉中熔融5小时,冷却后取出,再次研磨20分钟,得前驱物,将前驱物放入与1100℃的空气中烧结4小时,冷却取出,即得产品。该产品的发光强度稍高于实施例1中所得的Zn2(1-0.02)GeO4:0.02Mn2+的发光强度。
实施例11
按照ZnO∶GeO2∶MgF2∶Mn2+=2(1-0.02)∶1.5∶0.16∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、0.7845g固体氧化锗GeO2(分析纯)、0.0499g固体氟化镁MgF2、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨30分钟,使混合均匀得混合物。在空气条件下,将混合物置于700℃的马弗炉中熔融5小时,冷却后取出,再次研磨10分钟,得前驱物,将前驱物放入与900℃的空气中烧结5小时,冷却取出,即得产品。利用XRD粉末衍射仪(Bruker D8Advance)在室温条件下检测产品的物相,显示产物同样是Zn2GeO4相和MgGeO3的混合相,结果表明MgF2在此体系中不仅起到起着助熔剂的作用,降低了结晶温度,提高多晶颗粒的结晶度,而且MgF2并未以MgF2形式生存在而是与GeO2成了MgGeO3,从而降低了Mn离子之间的无辐射弛豫,从而提高Zn2GeO4:Mn2+发光材料的发光强度。
实施例12
按照ZnO∶GeO2∶MgF2∶Mn2+=2(1-0.02)∶2∶0.1∶0.02摩尔比,分别准确称量0.7976g固体氧化锌ZnO(分析纯)、1.0460g固体氧化锗GeO2(分析纯)、0.0312g固体氟化镁MgF2、0.0245g固体醋酸锰Mn(Ac)2·4H2O(分析纯),充分研磨30分钟,使混合均匀得混合物。在空气条件下,将混合物置于600℃的马弗炉中熔融5小时,冷却后取出,再次研磨20分钟,得前驱物,将前驱物放入与900℃的空气中烧结5小时,冷却取出,即得产品。该材料在紫外灯照射下发射明亮绿光,且亮度比商业绿粉SrAl2O4:Eu2+,Dy3+强,余辉强度(如图4b)远远超过绿粉Zn2GeO4:Mn2+。利用Fluoromax-4荧光光谱仪(HORIBA Jobin Yvon Inc.),在室温条件下检测产品的发光性能,由于该产品激发光谱在紫外区域呈宽谱带(250~400nm),则可应用于近紫外白光LEDs(具体可见图3d),该产品在336nm波长激发发射在绿光区域490~570nm的宽谱带(具体可见图2d),且亮度是长辉绿粉SrAl2O4:Eu2+,Dy3+的三倍,而且基质稳定不易水解,完全有潜能成为一直新型的商业绿色长余辉发光材料。图4表示实施例1、4、9、12中的样品各取0.03克样做热释光谱。从图可见,纯的Zn2GeO4:0.5%Mn2+的热释峰温度过低,在150℃至350℃间也有峰,说明有很深的陷阱能级,但这个陷阱太深,对余辉不贡献。在仪器范围内只测到半个峰,有半个峰在更低的温度。可见余辉是很短的。当加MgF2后,峰往高温区移动,说明加了MgF2后,陷阱深度增加,而且这个范围仍在100℃以内,对余辉是有贡献的,与这我们观察到余辉时间增强一致。当另加了100mol%的GeO2后,热释峰强 度大大增强,而且峰明显往高温区移,说明陷阱深度大大增加,且陷阱密度也大大增加,但高于100℃的陷阱过深,并不利于余辉。当同时另加100mol%的GeO2与5mol%的MgF2,热释峰强度大大增强,并且位于100℃以内,热释峰约出现在70℃,说明陷阱深度非常有利于余辉的产生,而且陷阱的密度也大大增强,与观察到的余辉强度结果一致。
- 还没有人留言评论。精彩留言会获得点赞!