一种寨卡病毒人源单克隆抗体及其应用的制作方法
本发明涉及一种寨卡病毒人源单克隆抗体及其应用,属于医药技术领域。
背景技术:
越来越多的证据表明寨卡病毒(Zika virus,ZIKV)可引起新生儿小头症以及神经发育异常,如“格林-巴氏综合征”等。ZIKV,属于黄病毒,主要由蚊虫叮咬传播,但是血液传播,性传播以及母胎传播途径也有报道。1947年,人们首次在乌干达丛林的猕猴分离到ZIKV。该病毒主要流行于非洲以及亚洲的热带地区。2015年,巴西暴发寨卡疫情,随着人群流动扩散至其他国家。目前此次疫情已导致超过60个国家或地区超过80,000例感染病例。然而,针对该病毒仍缺乏有效的疫苗及治疗手段。
中和抗体特异性高、能阻断病毒的入侵,是治疗病毒感染的有效手段。黄病毒囊膜蛋白E蛋白介导病毒与宿主细胞的结合和入侵,是病毒最主要的保护性抗原。X-射线晶体学结构显示黄病毒E蛋白有三个结构域:DI,DII和DIII。一般认为DIII负责介导病毒与受体的结合,之前的研究结果表明大多数有效的中和抗体都是识别DIII的中和表位。然而,近期的数据显示病毒表面的E蛋白二聚体以及与相邻二聚体中也存在高中和表位。DII头部(98-110位氨基酸)包含一个高度保守的融合区(fusion loop,FL),在病毒入侵的膜融合过程中起关键作用。不同黄病毒FL区域保守性非常高,在病毒感染过程中,免疫细胞会产生大量的针对FL的抗体。
已有研究发现有一些登革等黄病毒的中和抗体具有广谱中和活性,可以中和寨卡病毒,如:2A10G6、A11、C8等,这些抗体一般结合在保守的融合肽上或附近的区域。最近有报道从寨卡康复病人PBMC中分离到结合在E蛋白DIII的中和抗体。也有利用小鼠杂交瘤细胞,筛选到能够结合DIII的寨卡特异性中和抗体。这些抗体不同程度地能够保护小鼠免受致死剂量的病毒攻击。然而,RNA病毒在抗体压力下,具有高突变的特性,尽管已经有些中和抗体被鉴定,但是更多的针对不同表位的新的抗体对于治疗是必不可少的。本发明的目的是鉴定特异的具有保护作用的新的ZIKV中和抗体。
技术实现要素:
为了解决上述问题,本发明首先以大肠杆菌表达的ZIKV-E蛋白作为抗原,通过流式分选,从一例康复期ZIKV患者的PBMCs中筛选到可以特异结合ZIKV-E蛋白的记忆B细胞,然后对筛选的单一B细胞进行RT-PCR,获得抗体的可变区序列与片段,并进一步与恒定区连接至表达载体中。经哺乳动物细胞表达、纯化后,进行一系列的功能检测,包括与ZIKE-E蛋白的结合力,体外中和效果,体内保护能力等检测,获得了3株具有完全或部分保护寨卡病毒感染的人源单克隆抗体。
本发明的第一个目的是提供一种抗体,所述抗体命名为Z3L1、Z20或者Z23;其中Z3L1的重链可变区的氨基酸序列为SEQ ID NO:1且轻链可变区氨基酸序列为SEQ ID NO:2,Z20的重链可变区的氨基酸序列为SEQ ID NO:3且轻链可变区氨基酸序列为SEQ ID NO:4,Z23的重链可变区的氨基酸序列为SEQ ID NO:5且轻链可变区氨基酸序列为SEQ ID NO:6。
在本发明的一种实施方式中,所述Z3L1的重链的核苷酸序列为SEQ ID NO:7、轻链的核苷酸序列为SEQ ID NO:8。
在本发明的一种实施方式中,所述Z20的重链的核苷酸序列为SEQ ID NO:9、轻链的核苷酸序列为SEQ ID NO:10。
在本发明的一种实施方式中,所述Z23的重链的核苷酸序列为SEQ ID NO:11、轻链的核苷酸序列为SEQ ID NO:12。
在本发明的一种实施方式中,所述抗体的重链,包括重链可变区和重链恒定区,其中重链恒定区的氨基酸序列如SEQ ID NO:13所示。
在本发明的一种实施方式中,所述抗体Z20或者Z23的轻链为κ链,Z3L1的轻链为λ链;轻链包括轻链可变区和轻链恒定区;κ链的轻链恒定区的氨基酸序列如SEQ ID NO:15所示,λ链的轻链恒定区的氨基酸序列如SEQ ID NO:17所示。
本发明的三个抗体,来源于同一病患者,并且均靶向寨卡病毒特有的囊膜蛋白-E蛋白,通过抑制E蛋白介导的受体结合和/或膜融合过程,抑制病毒对细胞的感染。
本发明的第二个目的是提供所述抗体在制备治疗和/或预防寨卡病毒的药物方面的应用。
本发明的第三个目的是提供一种药物组合物,所述药物组合物含有所述的人源单克隆抗体Z3L1、Z20和/或Z23。
在本发明的一种实施方式中,所述药物组合物还含有医学生可接受的载体。
本发明的第四个目的是提供一种试剂盒,所述试剂盒中含有所述抗体的抗原,或者编码所述抗原的DNA分子,或者表达所述抗原的重组载体/表达盒/转基因细胞系/重组菌。
本发明的第五个目的是提供编码所述人源单克隆抗体Z3L1、Z20或者Z23的基因序列。
所述抗体的重链,包括重链可变区和重链恒定区,其中重链恒定区的氨基酸序列如SEQ ID NO:13所示(核苷酸序列如SEQ ID NO:14所示)。
在本发明的一种实施方式中,编码所述抗体的重链的序列,依次包括CMV启动子序列、EcoR I酶切位点序列、前导序列、编码重链可变区的序列、编码重链恒定区的序列、Xho I酶切位点序列。
在本发明的一种实施方式中,所述抗体的轻链,为κ链和/或λ链;轻链包括轻链可变区和轻链恒定区。
在本发明的一种实施方式中,编码所述抗体的轻链的序列,依次包括CMV启动子序列、第一酶切位点序列、前导序列、编码轻链可变区的序列、编码轻链恒定区的序列、酶切位点序列Xho I。
在本发明的一种实施方式中,所述κ链,其轻链恒定区的氨基酸序列如SEQ ID NO:15所示(核苷酸序列如SEQ ID NO:16所示),其中第一酶切位点为Sac I。
在本发明的一种实施方式中,所述λ链,其轻链恒定区的氨基酸序列如SEQ ID NO:17所示(核苷酸序列如SEQ ID NO:18所示),其中第一酶切位点为EcoR I。
在本发明的一种实施方式中,所述前导序列的氨基酸序列如SEQ ID NO:19所示(核苷酸序列如SEQ ID NO:20所示)。
本发明还要求保护含有所述基因序列或者表达所述抗体的表达载体、细胞。
本发明的有益效果:
本发明获得了3株人源高中和活性的ZIKV抗体:Z3L1、Z20与Z23。这3株抗体与已经报道的ZIKV抗体序列完全不同,是3株新发现的抗体。这三株抗体与ZIKV-E的结合常数分别为5.39μM(Z3L1),0.16μM(Z20)和0.44μM(Z23)。三株人源抗体均有很强的ZIKV中和活性。并且,Z3L1、Z20与Z23可以完全或部分保护小鼠免受致死剂量的ZIKV的攻击。本发明的三株人源抗体有着临床治疗和预防ZIKV的应用价值。
附图说明
图1:ZIKV-E蛋白纯化分子筛与SDS-PAGE结果;
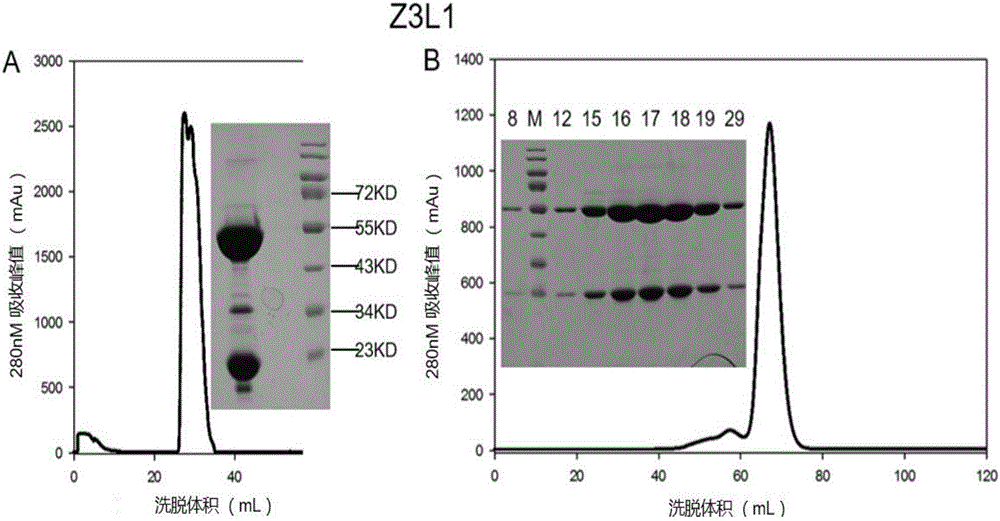
图2:Z3L1纯化的ProteinA(A)及分子筛层析(B)结果;
图3:Z20纯化的ProteinA(A)及分子筛层析(B)结果;
图4:Z23纯化的ProteinA(A)及分子筛层析(B)结果;
图5:Z20(A)、Z23(B)与Z3L1(C与D)与ZIKV-E的动力学曲线;
图6:抗体对C6/36扩增的ZIKV的中和曲线;
图7:抗体对Vero扩增的ZIKV的中和曲线;
图8:三株抗体对感染ZIKV小鼠的保护效果;A为小鼠存活率,B为存活小鼠体重变化。
具体实施方式
实施例1:寨卡E蛋白的表达与纯化
ZIKV E(氨基酸序列如SEQ ID NO:21所示、核苷酸序列如SEQ ID NO:22所示)胞外区DNA片段通过NdeI和XhoI酶切后,连接到pET21a载体上。其中ZIKV E蛋白编码区的3’端连上6个组氨酸标签(hexa-His-tag)的编码序列及翻译终止密码子。再将连接产物转化到BL21大肠杆菌感受态细胞。单克隆接种到40mL LB培养基中,培养6-8小时。接种到4L的LB培养基中,37℃培养至OD600=0.4-0.6,加入IPTG至终浓度1mM,37℃继续培养4-6小时。收获包涵体,通过稀释法复性包涵体。复性液浓缩后换成20mM Tris,150mM NaCl,pH8.0缓冲液。将浓缩后的蛋白溶液进一步以分子排阻层析纯化,使用AKTA-purifier(GE)和superdex200Hiload 16/60柱子(GE),使用缓冲液A(20mM Tris,150mM NaCl,pH8.0),同时监测280nm的紫外吸收值,收取目的蛋白,并通过SDS-PAGE鉴定蛋白纯度。结果如图1。实施例2:ZIKV-E蛋白特异性记忆B细胞的分离
在病人的知情同意下,采集15mL的血液,分离PBMCs。将分离的PBMCs以107/mL的密度与终浓度是100nM的ZIKV-E蛋白冰上孵育结合半小时,然后用PBS洗2次,再与下列抗体孵育:anti-human CD3/PE-Cy5,anti-human CD16/PE-Cy5,anti-humanCD235a/PE-Cy5,anti-human CD19/APC-Cy7,anti-human CD27/Pacific Blue,anti-humanCD38/APC,anti-human IgG/FITC,以及anti-His/PE。抗体冰上孵育半小时后,用PBS洗2次。
经FACSAria III分选收集PE-Cy5- APC- APC-Cy7+ Pacific Blue+ FITC+ PE+的细胞,直接收集到96孔板内,1细胞/孔。
实施例3:单一B细胞PCR、序列分析及人源抗体设计
将实施例2获得的B细胞通过Superscript III reverse transcriptase(Invitrogen)逆转录,逆转录引物如表1(序列如SED ID NO.23至SED ID NO.30所示),55℃反应60min。
表1.逆转录反应引物
将此逆转录产物作为模板,用HotStar Tap Plus酶(QIAgen)进行PCR,扩增抗体可变区序列(PCRa)。设计相应的引物,反应条件如下:95℃,5min;95℃30s,55℃(重链/κ链)/50℃(λ链)30s,72℃90s,35个循环;72℃,7min。将此作为模板再进行1轮PCR(PCRb),条件如下:95℃,5min;95℃30s,58℃(重链)/60℃(κ链)/64℃(λ链)30s,72℃90s,35个循环;72℃,7min。
1.2%的琼脂糖凝胶电泳,分离PCR产物。条带大小在400-500bp的切胶回收后送测序公司测序。测序结果用IMGT在线软件进行分析。
分析正确的可变区序列与相应的重链/κ链/λ链的恒定区通过搭桥PCR连接,克隆至表达载体pCAGGS中。其中重链与λ链以EcoRI和XhoI连接,κ链以SacI与XhoI连接。B细胞测序及表达质粒构建如下:
人源抗体设计策略如下:
重链:CMV promoter-EcoRI-Leader sequences-重链可变区-CH-Xho I;
轻链(κ):CMV promoter-Sac I-Leader sequences-轻链可变区-CL(κ)-Xho I;
轻链(λ):CMV promoter-EcoR I-Leader sequences-轻链可变区-CL(λ)-Xho I。
其中,Leader sequences的氨基酸序列如SEQ ID NO:19(核苷酸序列如SEQ ID NO:20)。
实施例4:抗体的表达及纯化
用含10%FBS的DMEM培养293T细胞。用含有特定抗体轻、重链编码基因的质粒共转染293T。转染4-6小时后给细胞换液成无血清的DMEM继续培养3天,收集上清,并补加DMEM,再培养4天,收集上清。
收集的上清经过5000rpm离心30min后,与含有20mM磷酸钠(pH 8.0)的缓冲液等体积混合,经过0.22μm滤膜过滤后,与proteinA预装柱结合(5mL,GE Healthcare)。以10mM甘氨酸(pH 3.0)洗脱结合的蛋白。收集此蛋白浓缩后进行分子筛层析。目的峰通过SDS-PAGE确定,结果如图2、3以及4,说明目标蛋白得到正常表达。
最终,得到了三个能与ZIKV E蛋白结合且中和活性较强的抗体Z3L1、Z20、Z23。
其中Z3L1的重链可变区的氨基酸序列为SEQ ID NO:1(核苷酸序列如SEQ ID NO:7)且轻链可变区氨基酸序列为SEQ ID NO:2(核苷酸序列如SEQ ID NO:8)。Z3L1的轻链为λ型,轻链恒定区CL(λ)的氨基酸序列为SEQ ID NO:17(核苷酸序列如SEQ ID NO:18)
Z20的重链可变区的氨基酸序列为SEQ ID NO:3(核苷酸序列如SEQ ID NO:9)且轻链可变区氨基酸序列为SEQ ID NO:4(核苷酸序列如SEQ ID NO:10),Z23的重链可变区的氨基酸序列为SEQ ID NO:5(核苷酸序列如SEQ ID NO:11)且轻链可变区氨基酸序列为SEQ ID NO:6(核苷酸序列如SEQ ID NO:12)。Z20和Z23的轻链均为κ型,轻链恒定区CL(κ)的氨基酸序列为SEQ ID NO:15(核苷酸序列如SEQ ID NO:16)
所述抗体Z3L1、Z20、Z23的重链恒定区CH的的氨基酸序列为SEQ ID NO:13(核苷酸序列如SEQ ID NO:14)。
与已经报道的具有中和ZIKV活性的人源抗体进行序列比对,发现本发明中的三株人源抗体:Z20(IGVH 4-4*02-IGVD 3-3*01–IGVJ 4*02)与Z3L1(IGVH 3-30-3*03-IGVD 6-13*01–IGVJ 4*02)重链均具有独特的V-D-J基因重排方式;与Z23使用相同的IGVH胚系基因的抗体有3株,如表2所示。但是4株抗体使用的IGVD胚系基因均各不相同,与Z23氨基酸序列的同源性分别仅88.24,84.3和90.76%。
表2 与Z23相同IGVH基因的ZIKV中和抗体比较
实施例5:人源抗体的性能检测
(1)表面等离子共振技术检测与ZIKV-E的结合能力
表面等离子共振分析利用Biacore T100(Biacore Inc.)进行。具体步骤如下:
首先,将anti-human IgG的抗体以氨基偶联的方式固定在CM5芯片的通道(flow cell,Fc)1与Fc2。固定量控制在10,000响应值(response units,RU)左右。将通道调至Fc2,然后以抗体捕获的方式结合纯化的抗体,此时,液流速度控制在10μL/min,进样1min,抗体捕获量在100RU左右。再以10mM HEPES,150mM NaCl,pH 7.4溶液倍比稀释ZIKV-E蛋白,流速调至30μL/min,通道调至Fc2-Fc1的模式后,从低浓度开始逐一上样ZIKA-E蛋白。曲线组成图如图5所示的动力学曲线。结果如表3所示。结合动力学常数的计算是利用BIAevaluation software T100(Biacore,Inc.)软件进行。SPR的结果显示,三株抗体均可以与ZIKV-E蛋白结合,解离常数0.16μM~5.39μM。
表3 人源抗体与ZIKV E蛋白结合的动力学常数
(2)中和试验
将纯化的抗体3倍倍比稀释,与1:150稀释的ZIKV(C6/36或是Vero扩增)混合,37℃共孵育60分钟。然后将混合液加入到已铺满Vero细胞的24孔板中,300μL/孔。37℃孵育1小时后,每孔补充培养基(DMEM,10%FBS)1mL,继续培养30小时后染色。收集细胞,用含4%多聚甲醛,0.05%的soponin的PBS处理细胞,冰上避光静置30min。然后以solution溶液(PBS,1%BSA,0.01%soponin)洗涤细胞2次,与2μg/mL的Z1抗体冰上孵育30min后,solution溶液洗涤细胞2次,再与1:200稀释的anti-human IgG避光冰上孵育30min。solution溶液洗2次后,用FACSCanto检测细胞阳性比例。根据不同浓度下阳性比例,计算抗体对ZIKV的中和能力,结果如图6与7,结果统计如表4。
表4 三株抗体对不同来源病毒中和效果
a半抑制浓度;b判定系数
(3)动物保护试验
I型干扰素受体(InterferonαβR)敲除小鼠(B6.129S2-Ifnar1<tm1Agt>/Mmjax,Jackson Laboratories),以3-5只分组。每只小鼠腹腔注射1×106PFU的ZIKV(GenBank accession number:KX087101.2)。感染24小时后单一剂量10mg/kg的抗体Z3L1、Z20、Z23或等体积的PBS通过腹腔注射给感染的小鼠。记录14天内小鼠的存活与体重变化。体重变化超过20%或是出现瘫痪症状的小鼠处死。结果如图8显示。由图8可知,注射PBS的3只小鼠在感染后第7天均死亡,注射对照抗体2G4的5只小鼠中,也有4只在感染后第8天死亡(图8A)。相比之下,注射Z3L1以及Z23抗体的各三只小鼠均存活(图8A),并且体重仍处于生长中(图8B),注射Z20抗体的5只小鼠中也有四只存活,并且存活的四只小鼠体重也处于上升过程中。这组实验结果表明,三株人源单抗在小鼠体内可以完全(Z3L1和Z23)或部分(Z20)治疗受ZIKV感染的小鼠。
目前,已发表的在小鼠模型中对ZIKV感染有治疗作用的人源抗体只有一株,即ZKA64,其与ZIKV-E的结合能力为半最大效应浓度EC50=65ng/mL,半抑制浓度IC50=0.155μg/mL。本实验中三株人源抗体的IC50为0.17~0.89μg/mL。并且,在动物保护实验中,本发明使用的抗体剂量为10mg/kg,远小于文献报道的ZKA64的抗体剂量15mg/kg。本发明的三个抗体为预防RNA病毒在抗体压力下发生突变提供更多的针对不同表位的新的抗体。
综上,本发明通过筛选康复病人的ZIKV-E特异结合的记忆B细胞,获得3株人源高中和活性的ZIKV抗体:Z3L1、Z20与Z23。这3株抗体与已经报道的寨卡抗体序列完全不同,是3株新发现的抗体。这三株抗体与ZIKV-E的结合常数分别为5.39μM(Z3L1),0.16μM(Z20)和0.44μM(Z23)。三株人源抗体均有很强的寨卡病毒中和活性。并且,Z3L1、Z20与Z23可以完全或部分保护小鼠免受致死剂量的寨卡病毒的攻击。这提示,三株人源抗体有着临床治疗和预防寨卡的应用价值。
虽然本发明已以较佳实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可做各种的改动与修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
- 还没有人留言评论。精彩留言会获得点赞!