基因突变体及其应用的制作方法
本发明涉及基因突变体及其应用。具体地,本发明涉及分离的核酸、分离的多肽、筛选易感原发性纤毛运动障碍征的生物样品的方法、筛选易感原发性纤毛运动障碍征的生物样品的系统、用于筛选易感原发性纤毛运动障碍征的生物样品的试剂盒、构建体以及重组细胞。
背景技术:
原发性纤毛运动障碍(primary ciliary dyskinesia,PCD),又称纤毛不动综合征(immobile cilia syndrome),是因纤毛结构缺陷导致活动障碍引起纤毛清除功能降低及其他功能障碍的基因遗传病。该病临床表现多样,可累及多个器官组织,其诊断和鉴别诊断存在困难。PCD现阶段,寻找致病基因对疾病诊断或治疗意义重大。虽然目前已发现一些PCD的致病基因,但热点率相对较低,且目前已报道的PCD亚型多达18个,涉及数十几个基因,因此,仍存在着相当一部分未知致病基因位点。
因而,目前对原发性纤毛运动障碍征的研究仍有待深入。
技术实现要素:
本发明旨在至少解决现有技术中存在的技术问题之一。为此,本发明的一个目的在于提出一种能够有效筛选易感原发性纤毛运动障碍征的生物样品的方法。
本发明是基于发明人的下列工作而完成的:发明人通过高通量外显子组测序联合候选基因突变验证的方法确定了原发性纤毛运动障碍征的致病基因上的新突变。
根据本发明的第一方面,本发明提出了一种分离的核酸。根据本发明的实施例,与SEQ ID NO:1相比,该核酸具有c.G8030A突变;或者与SEQ ID NO:3相比,该核酸具有c.C6265T突变。根据本发明的实施例,发明人确定了DNAH5和DNAH11基因突变体,这些新突变体与原发性纤毛运动障碍征的发病密切相关,从而通过检测这些新突变体在生物样品中是否存在,可以有效地检测生物样品是否易感原发性纤毛运动障碍征。
根据本发明的第二方面,本发明提出了一种分离的多肽。根据本发明的实施例,与SEQ ID NO:2相比,该分离的多肽具有p.R2677Q突变;或者与SEQ ID NO:4相比,该分离的多肽具有p.R2089*突变。通过检测生物样品中是否表达该多肽,可以有效地检测生物样品是否易感原发性纤毛运动障碍征。
根据本发明的第三方面,本发明提出了一种筛选易感原发性纤毛运动障碍征的生物样品的方法。根据本发明的实施例,该方法包括以下步骤:从生物样品提取核酸样本;确定所述核酸样本的核酸序列;所述核酸样本的核酸序列或其互补序列,与SEQ ID NO:1相比具有c.G8030A突变,或者与SEQ ID NO:3相比具有c.C6265T突变,是所述生物样品易感原发性纤毛运动障碍征的指示。通过根据本发明实施例的筛选易感原发性纤毛运动障碍征的生物样品的方法,可以有效地筛选易感原发性纤毛运动障碍征的生物样品。
根据本发明的第四方面,本发明提出了一种筛选易感原发性纤毛运动障碍征的生物样品的系统。根据本发明的实施例,该系统包括:核酸提取装置,所述核酸提取装置用于从所述生物样品提取核酸样本;核酸序列确定装置,所述核酸序列确定装置与所述核酸提取装置相连,用于对所述核酸样本进行分析,以便确定所述核酸样本的核酸序列;判断装置,所述判断装置与所述核酸序列确定装置相连,以便基于所述核酸样本的核酸序列或其互补序列,与SEQ ID NO:1相比具有c.G8030A突变,或者与SEQ ID NO:3相比具有c.C6265T突变,判断所述生物样品是否易感原发性纤毛运动障碍征。利用该系统,能够有效地实施前述筛选易感原发性纤毛运动障碍征的生物样品的方法,从而可以有效地筛选易感原发性纤毛运动障碍征的生物样品。
根据本发明的第五方面,本发明提出了一种用于筛选易感原发性纤毛运动障碍征的生物样品的试剂盒。根据本发明的实施例,该试剂盒含有:适于检测DNAH5和DNAH11基因突变体的至少一种的试剂,其中与SEQ ID NO:1相比,所述DNAH5基因突变体具有c.G8030A突变;与SEQ ID NO:3相比,所述DNAH11基因突变体具有c.C6265T突变。利用根据本发明的实施例的试剂盒,能够有效地筛选易感原发性纤毛运动障碍征的生物样品。
根据本发明的第六方面,本发明还提出了一种构建体。根据本发明的实施例,该构建体包含前面所述的分离的核酸。需要说明的是,“构建体包含前面所述的分离的核酸”表示,本发明的构建体包含与SEQ ID NO:1相比具有c.G8030A突变的DNAH5基因突变体的核酸序列,或者包含与SEQ ID NO:3相比具有c.C6265T突变的DNAH11基因突变体的核酸序列,或者同时包含上述DNAH5基因突变体和DNAH11基因突变体的核酸序列。由此,利用本发明的构建体转化受体细胞获得的重组细胞,能够有效地用于筛选治疗原发性纤毛运动障碍征的药物。
根据本发明的第七方面,本发明还提出了一种重组细胞。根据本发明的实施例,该重组细胞是通过前面所述的构建体转化受体细胞而获得的。根据本发明的一些实施例,,利用本发明的重组细胞,能够有效地筛选治疗原发性纤毛运动障碍征的药物。
本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:
图1:显示了根据本发明一个实施例的筛选易感原发性纤毛运动障碍征的生物样品的系统及其组成部分的示意图,其中,
A为根据本发明实施例的筛选易感原发性纤毛运动障碍征的生物样品的系统的示意图,
B为根据本发明实施例的核酸提取装置的示意图,
C为根据本发明实施例的核酸序列确定装置的示意图;
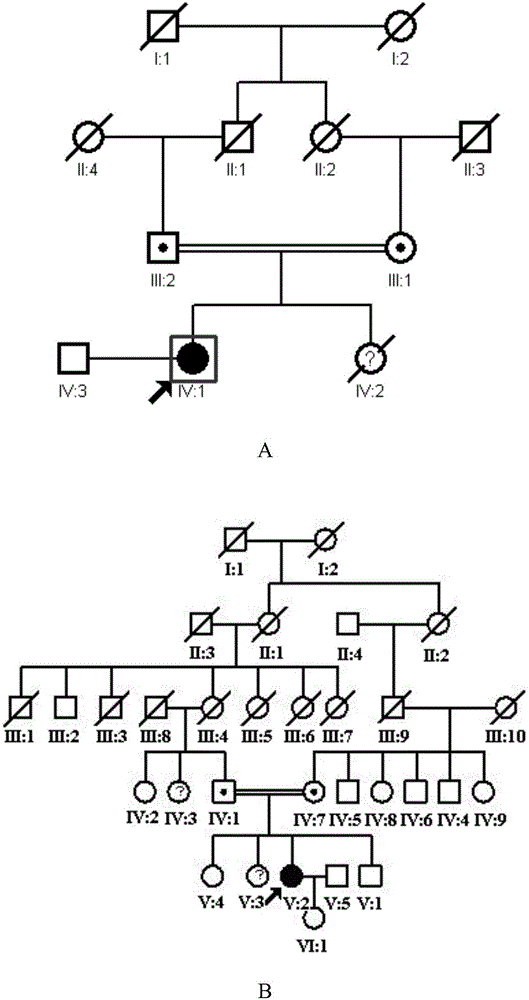
图2:显示了根据本发明一个实施例的两个PCD患者家系的家系图谱,其中,
A为根据本发明实施例的PCD患者家系1的家系图谱,
B为根据本发明实施例的PCD患者家系2的家系图谱;
图3:显示了根据本发明一个实施例,PCD患者家系1内的先证者及其父母的DNAH5基因突变位点的Sanger测序验证峰图;
图4:显示了根据本发明一个实施例,PCD患者家系2内的先证者及其父母DNAH11基因突变位点的Sanger测序验证峰图。
具体实施方式
下面详细描述本发明的实施例。下面描述的实施例是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。
DNAH5及DNAH11基因突变体
根据本发明的第一方面,本发明提出了一种分离的核酸。根据本发明的实施例,与SEQ ID NO:1相比,该核酸具有c.G8030A突变;或者与SEQ ID NO:3相比,该核酸具有c.C6265T突变。需要说明的是,本发明的分离的核酸编码DNAH5或者DNAH11突变体,也可以称为“编码DNAH5或者DNAH11突变体的核酸”,即该核酸可以理解为与编码DNAH5或者DNAH11突变体的基因相对应的核酸物质,即核酸的类型不受特别限制,可以是任何包含与DNAH5和DNAH11的编码基因相对应的脱氧核糖核苷酸和/或核糖核苷酸的聚合物,包括但不限于DNA、RNA或cDNA。根据本发明的一个具体示例,前面所述的编码DNAH5和DNAH11突变体的核酸为DNA。根据本发明的实施例,发明人确定了DNAH5和DNAH11基因的新突变体,该突变体与原发性纤毛运动障碍征的发病密切相关,从而通过检测该突变体在生物样品中是否存在,可以有效地检测生物样品是否易感原发性纤毛运动障碍征,也可以通过检测该突变体在生物体中是否存在,可以有效地预测生物体是否易感原发性纤毛运动障碍征。
对于本发明说明书和权利要求书中,提及核酸,本领域技术人员应当理解,实际包括互补双链的任意一条,或者两条。为了方便,在本说明书和权利要求书中,虽然多数情况下只给出了一条链,但实际上也公开了与之互补的另一条链。例如,提及SEQ ID NO:1,实际包括其互补序列。本领域技术人员还可以理解,利用一条链可以检测另一条链,反之亦然。
这些编码DNAH5和DNAH11突变体的核酸,是本申请的发明人通过高通量外显子组测序联合候选基因突变验证的方法,确定的原发性纤毛运动障碍征的致病基因上的新突变,并且在现有技术中并未见到DNAH5基因上的c.G8030A突变,以及DNAH11基因上的c.C6265T突变与原发性纤毛运动障碍征相关的报道。
DNAH5基因为负义链编码。野生型DNAH5基因的cDNA的核苷酸序列如SEQ ID NO:1所示(13875 nt):
其编码的的氨基酸序列如SEQ ID NO:2所示(4624 aa):
野生型DNAH11基因的cDNA的核苷酸序列如SEQ ID NO:3所示(13569 nt):
其编码的的氨基酸序列如SEQ ID NO:4所示(4523 aa):
发明人发现的DNAH5基因突变体与SEQ ID NO:1相比,具有c.G8030A突变,即相对于野生型DNAH5基因,本发明的DNAH5基因突变体的cDNA中第8030位的G突变为A,由此,其所编码的产物与野生型DNAH5(SEQ ID NO:2)相比,具有p.R2677Q突变,即其2677位氨基酸从R突变为Q。
此外,发明人发现的DNAH11基因突变体与SEQ ID NO:3相比,具有c.C6265T突变,即相对于野生型DNAH11基因,本发明的DNAH11基因突变体的cDNA中第6265位的C突变为T,由此,其所编码的产物与野生型DNAH11相比,具有p.R2089*突变,即其第2089位编码氨基酸R的密码子突变后成终止密码子,翻译终止。
本发明的发明人首次提出DNAH5基因的c.G8030A突变以及DNAH11基因的c.C6265T突变导致患者出现原发性纤毛运动障碍症状。根据本发明的第二方面,本发明提出了一种分离的多肽。根据本发明的实施例,与SEQ ID NO:2相比,该分离的多肽具有p.R2677Q突变;或者与SEQ ID NO:4相比,该分离的多肽具有p.R2089*突变。根据本发明的一些具体示例,具有p.R2677Q突变的多肽是由前述分离的编码DNAH5突变体的核酸编码的,具有p.R2089*突变突变的多肽是由前述分离的编码DNAH11突变体的核酸编码的。通过检测生物样品中是否表达该多肽,可以有效地检测生物样品是否易感原发性纤毛运动障碍征,也可以通过检测这些多肽在生物体中是否存在,有效地预测生物体是否易感原发性纤毛运动障碍征。
筛选易感原发性纤毛运动障碍征的生物样品的方法
根据本发明的第三方面,本发明提出了一种筛选易感原发性纤毛运动障碍征的生物样品的方法。根据本发明的实施例,该筛选易感原发性纤毛运动障碍征的生物样品的方法可以包括以下步骤:
首先,从生物样品提取核酸样本。根据本发明的实施例,生物样品的类型并不受特别限制,只要从该生物样品中能够提取到反映生物样品DNAH5和DNAH11是否存在突变的核酸样本即可。根据本发明的实施例,生物样品可以为选自人体血液、皮肤、皮下组织的至少一种。由此,可以方便地进行取样和检测,从而能够进一步提高筛选易感原发性纤毛运动障碍征的生物样品的效率。根据本发明的实施例,这里所使用的术语“核酸样本”应做广义理解,其可以是任何能够反映生物样品中DNAH5和DNAH11是否存在突变的样本,例如可以是从生物样品中直接提取的全基因组DNA,也可以是该全基因组中包含DNAH5和DNAH11编码序列的一部分,可以是从生物样品中提取的总RNA,也可以是从生物样品中提取的mRNA。根据本发明的一个实施例,所述核酸样本为全基因组DNA。由此,可以扩大生物样品的来源范围,并且可以同时对生物样品的多种信息进行确定,从而能够提高筛选易感原发性纤毛运动障碍征的生物样品的效率。另外,根据本发明的实施例,针对采用RNA作为核酸样本,从生物样品提取核酸样本可以进一步包括:从生物样品提取RNA样本,优选RNA样本为mRNA;以及基于所得到的RNA样本,通过反转录反应,获得cDNA样本,所得到的cDNA样本构成核酸样本。由此,可以进一步提高利用RNA作为核酸样本筛选易感原发性纤毛运动障碍征的生物样品的效率。
接下来,在得到核酸样本之后,可以对核酸样本进行分析,从而能够确定所得到核酸样本的核酸序列。根据本发明的实施例,确定所得到核酸样本的核酸序列的方法和设备并不受特别限制。根据本发明的具体实施例,可以通过测序方法,确定核酸样本的核酸序列。根据本发明的实施例,可以用于进行测序的方法和设备并不受特别限制。根据本发明的实施例,可以采用第二代测序技术,也可以采用第三代以及第四代或者更先进的测序技术。根据本发明的具体示例,可以利用选自Hiseq2000、SOLiD、454和单分子测序装置的至少一种对核酸序列进行测序。由此,结合最新的测序技术,针对单个位点可以达到较高的测序深度,检测灵敏度和准确性大大提高,因而能够利用这些测序装置的高通量、深度测序的特点,进一步提高对核酸样本进行检测分析的效率。从而,能够提高后续对测序数据进行分析时的精确性和准确度。由此,根据本发明的实施例,确定核酸样本的核酸序列可以进一步包括:首先,针对所得到的核酸样本,构建核酸测序文库;以及对所得到的核酸测序文库进行测序,以便获得由多个测序数据构成的测序结果。根据本发明的一些实施例,可以采用选自Hiseq2000、SOLiD、454和单分子测序装置的至少一种对所得到的核酸测序文库进行测序。另外,根据本发明的实施例,可以对核酸样本进行筛选,富集DNAH5和DNAH11外显子,该筛选富集可以在构建测序文库之前,构建测序文库过程中,或者构建测序文库之后进行。根据本发明的一个实施例,针对核酸样本,构建核酸测序文库进一步包括:利用选自DNAH5和DNAH11基因外显子特异性引物的至少一种,对核酸样本进行PCR扩增;以及针对所得到的扩增产物,构建核酸测序文库。由此,可以通过PCR扩增,富集DNAH5和DNAH11外显子,从而能够进一步提高筛选易感原发性纤毛运动障碍征的生物样品的效率。根据本发明的实施例,DNAH5和DNAH11基因外显子特异性引物的序列不受特别限制,根据本发明的优选实施例,DNAH5基因外显子特异性引物可以具有如SEQ ID NO:5-6所示的核苷酸序列,DNAH11基因外显子特异性引物可以具有如SEQ ID NO:7-8所示的核苷酸序列。发明人惊奇地发现,通过采用SEQ ID NO:5-6所示的引物,可以在PCR反应体系中显著有效地完成对DNAH5尤其是c.G8030A所在的外显子序列的扩增;采用SEQ ID NO:7-8所示的引物,可以显著有效地完成对DNAH11尤其是c.C6265T所在外显子序列的扩增。需要说明的是,这些SEQ ID NO:5-8所示的核苷酸序列是本发明的发明人在付出了艰苦的劳动后,意外获得的。
关于针对核酸样本,构建测序文库的方法和流程,本领域技术人员可以根据不同的测序技术进行适当选择,关于流程的细节,可以参见测序仪器的厂商例如Illumina公司所提供的规程,例如参见Illumina公司Multiplexing Sample Preparation Guide(Part#1005361;Feb 2010)或Paired-End SamplePrep Guide(Part#1005063;Feb 2010),通过参照将其并入本文。根据本发明的实施例,从生物样品提取核酸样本的方法和设备,也不受特别限制,可以采用商品化的核酸提取试剂盒进行。
需要说明的是,在这里所使用的术语“核酸序列”应作广义理解,其可以是在对核酸样本进行测序得到的测序数据进行组装后,得到的完整的核酸序列信息,也可以是直接采用通过对核酸样本进行测序所得到的测序数据(reads)作为核酸序列,只要这些核酸序列中含有对应DNAH5和DNAH11基因的编码序列即可。
最后,在确定核酸样本的核酸序列之后,将所得到的核酸样本的核酸序列相应的参考序列进行比对,当所得到的核酸序列中具有前述的三种突变的至少之一时,即指示生物样品易感原发性纤毛运动障碍征。具体地,当获得的核酸样本是采用DNAH5基因外显子特异性引物扩增获得时,将该核酸样本的核酸序列与SEQ ID NO:1的序列相比对,如果在所得到的核酸序列中具有c.G8030A突变,则指示生物样品易感原发性纤毛运动障碍征。当获得的核酸样本是采用DNAH11基因外显子特异性引物扩增获得时,将该核酸样本的核酸序列与SEQ ID NO:3的序列相比对,如果在所得到的核酸序列中具有c.C6265T突变,则指示生物样品易感原发性纤毛运动障碍征。当获得的核酸样本是采用DNAH11及DNAH5基因外显子特异性引物扩增获得时,将该核酸样本的核酸序列分别与SEQ ID NO:1和SEQ ID NO:3的序列相比对,如果在所得到的核酸序列中具有c.G8030A、c.C6265T突变,则指示生物样品易感原发性纤毛运动障碍征。由此,通过根据本发明实施例的筛选易感原发性纤毛运动障碍征的生物样品的方法,可以有效地筛选易感原发性纤毛运动障碍征的生物样品。根据本发明的实施例,对核酸序列与SEQ ID NO:1及SEQ ID NO:3进行比对的方法和设备并不受特别限制,可以采用任意常规的软件进行操作,根据本发明的具体实例,可以采用SOAPALIGNER/SOAP2进行比对。
需要说明的是,根据本发明实施例的“筛选易感原发性纤毛运动障碍征的生物样品的方法”的用途不受特别限制,例如可以用作非诊断目的的筛选方法。
筛选易感原发性纤毛运动障碍征的生物样品的系统和试剂盒
根据本发明的第四方面,本发明提出了一种能够有效实施上述筛选易感原发性纤毛运动障碍征的生物样品的方法的系统。
参考图1,根据本发明的实施例,该筛选易感原发性纤毛运动障碍征的生物样品的系统1000包括:核酸提取装置100、核酸序列确定装置200以及判断装置300。
根据本发明的实施例,核酸提取装置100用于从生物样品提取核酸样本。如前所述,根据本发明的实施例,核酸样本的类型并不受特别限制,对于采用RNA作为核酸样本,则核酸提取装置进一步包括RNA提取单元101和反转录单元102,其中,提取单元101用于从生物样品提取RNA样本,反转录单元102与RNA提取单元101相连,用于对RNA样本进行反转录反应,以便获得cDNA样本,所得到的cDNA样本构成核酸样本。
根据本发明的实施例,核酸序列确定装置200与核酸提取装置100相连,用于对核酸样本进行分析,以便确定核酸样本的核酸序列。如前所示,可以采用测序的方法确定核酸样本的核酸序列。由此,根据本发明的一个实施例,所述核酸序列确定装置200可以进一步包括:文库构建单元201以及测序单元202。文库构建单元201用于针对核酸样本,构建核酸测序文库;测序单元202与文库构建单元201相连,用于对核酸测序文库进行测序,以便获得由多个测序数据构成的测序结果。如前所述,可以通过PCR扩增,富集DNAH5和DNAH11外显子,进一步提高筛选易感原发性纤毛运动障碍征的生物样品的效率。由此,文库构建单元201可以进一步包括PCR扩增模块(图中未示出),在该PCR扩增模块中设置有选自DNAH5和DNAH11基因外显子特异性引物的至少一种,以便利用DNAH5和DNAH11基因外显子特异性引物的至少一种,对所述核酸样本进行PCR扩增,根据本发明的具体实施例,DNAH5基因外显子特异性引物具有如SEQ ID NO:5-6所示的核苷酸序列,DNAH11基因外显子特异性引物具有如SEQ ID NO:7-8所示的核苷酸序列。根据本发明的实施例,测序单元202可以包括选自HISEQ2000、SOLiD、454和单分子测序装置的至少一种。由此,结合最新的测序技术,针对单个位点可以达到较高的测序深度,检测灵敏度和准确性大大提高,因而能够利用这些测序装置的高通量、深度测序的特点,进一步提高对核酸样本进行检测分析的效率。从而,提高后续对测序数据进行分析时的精确性和准确度。
根据本发明的实施例,判断装置300与核酸序列确定装置200相连,适于将核酸样本的核酸序列进行比对,以便基于核酸样本的核酸序列与SEQ ID NO:1及SEQ ID NO:3的区别判断生物样品是否易感原发性纤毛运动障碍征。具体地,基于所述核酸样本的核酸序列或其互补序列,与SEQ ID NO:1相比具有c.G8030A突变,或者与SEQ ID NO:3相比具有c.C6265T突变,判断生物样品是否易感原发性纤毛运动障碍征。如前所述,根据本发明的一个实施例,核酸样本的核酸序列或其互补序列,与SEQ ID NO:1相比具有选自c.G8030A突变,或者与SEQ ID NO:3相比具有c.C6265T突变,是生物样品易感原发性纤毛运动障碍征的指示。如前所述,根据本发明的实施例,对核酸序列与SEQ ID NO:1以及SEQ ID NO:3进行比对的设备并不受特别限制,可以采用任意常规的软件进行操作,例如根据本发明的具体实例,可以采用SOAPALIGNER/SOAP2进行比对。
由此,利用该系统,能够有效地实施前述筛选易感原发性纤毛运动障碍征的生物样品的方法,从而可以有效地筛选易感原发性纤毛运动障碍征的生物样品。
根据本发明的第五方面,本发明提出了一种用于筛选易感原发性纤毛运动障碍征的生物样品的试剂盒。根据本发明的实施例,该用于筛选易感原发性纤毛运动障碍征的生物样品的试剂盒包括:适于检测DNAH5和DNAH11基因突变体的至少一种的试剂,其中与SEQ ID NO:1相比,该DNAH5基因突变体具有c.G8030A突变;与SEQ ID NO:3相比,该DNAH11基因突变体具有c.C6265T突变。利用根据本发明的实施例的试剂盒,能够有效地筛选易感原发性纤毛运动障碍征的生物样品。在本文中,所使用的术语“适于检测DNAH5和DNAH11基因突变体的至少一种的试剂”应做广义理解,即可以是检测DNAH5和DNAH11编码基因的至少一种的试剂,也可以是检测DNAH5和DNAH11突变体的至少一种的试剂,例如可以采用识别特异性位点的抗体。根据本发明的一个实施例,该试剂为核酸探针。由此,可以高效地筛选易感原发性纤毛运动障碍征的生物样品。
构建体及重组细胞
根据本发明的第六方面,本发明还提出了一种构建体。根据本发明的实施例,该构建体包含前面所述的分离的核酸。需要说明的是,“构建体包含前面所述的分离的核酸”表示,本发明的构建体包含与SEQ ID NO:1相比具有c.G8030A突变的DNAH5基因突变体的核酸序列,或者包含与SEQ ID NO:3相比具有c.C6265T突变的DNAH11基因突变体的核酸序列,或者同时包含上述DNAH5基因突变体和DNAH11基因突变体的核酸序列。由此,利用本发明的构建体转化受体细胞获得的重组细胞,能够有效地用于筛选治疗原发性纤毛运动障碍征的药物。其中,所述受体细胞的种类不受特别限制,例如可以为大肠杆菌细胞、哺乳动物细胞,优选该受体细胞来源于哺乳动物。
在本发明中所使用的术语“构建体”是指这样的一种遗传载体,其包含特定核酸序列,并且能够将目的核酸序列转入宿主细胞中,以获得重组细胞。根据本发明的实施例,构建体的形式不受特别限制。根据本发明的实施例,其可以为质粒、噬菌体、人工染色体、粘粒(Cosmid)、病毒的至少一种,优选质粒。质粒作为遗传载体,具有操作简单,可以携带较大片段的性质,便于操作和处理。质粒的形式也不受特别限制,既可以是环形质粒,也可以是线性质粒,即可以是单链的,也可以是双链的。本领域技术人员可以根据需要进行选择。在本发明中所使用的术语“核酸”可以是任何包含脱氧核糖核苷酸或者核糖核苷酸的聚合物,包括但不限于经过修饰的或者未经修饰的DNA、RNA,其长度不受任何特别限制。对于用于构建重组细胞的构建体,优选所述核酸为DNA,因为DNA相对于RNA而言,其更稳定,并且易于操作。
根据本发明的第七方面,本发明还提出了一种重组细胞。根据本发明的实施例,该重组细胞是通过前面所述的构建体转化受体细胞而获得的。从而,本发明的重组细胞能够有效表达构建体所携带的DNAH5基因突变体和DNAH11基因突变体的至少一种。根据本发明的一些实施例,利用本发明的重组细胞,能够有效地筛选治疗原发性纤毛运动障碍征的药物。根据本发明的实施例,受体细胞的种类不受特别限制,例如可以为大肠杆菌细胞、哺乳动物细胞,优选所述受体细胞来源于非人哺乳动物。
需要说明的是,在本文前面筛选易感原发性纤毛运动障碍征的生物样品的方法部分中所描述的特征和优点,同样适用于筛选易感原发性纤毛运动障碍征的生物样品的系统或者试剂盒,在此不再赘述。
此外,还需要说明的是,根据本发明实施例的筛选易感原发性纤毛运动障碍征的生物样品的方法、系统以及试剂盒,是本申请的发明人经过艰苦的创造性劳动和优化工作才完成的。
下面参考具体实施例,对本发明进行说明,需要说明的是,这些实施例仅仅是说明性的,而不能理解为对本发明的限制。若未特别指明,实施例中所采用的技术手段为本领域技术人员所熟知的常规手段,可以参照《分子克隆实验指南》第三版或者相关产品进行,所采用的试剂和产品也均为可商业获得的。未详细描述的各种过程和方法是本领域中公知的常规方法,所用试剂的来源、商品名以及有必要列出其组成成分者,均在首次出现时标明,其后所用相同试剂如无特殊说明,均以首次标明的内容相同。
实施例1全外显子组测序确定致病基因及突变位点
1、样本收集:
发明人收集到2个PCD患者家系,在本文中有时也称为“PCD患者家系1”和“PCD患者家系2”。其中,图2分别显示了上述2个PCD患者家系PCD患者家系2的家系图谱。其中,图2A为PCD患者家系1PCD患者家系1的家系图谱,图2B为PCD患者家系2PCD患者家系2的家系图谱。如图2所示,表示正常女性;表示无法确定是否患病的女性;表示正常男性;表示女性患者;表示已故正常男性;表示已故正常女性;表示男性患者;表示女性患者;表示已故无法确定是否患病的女性;箭头所指为先证者。如图2所示,PCD患者家系1,先证者为青年女性,29岁;表现为自幼反复的上呼吸道验证、鼻窦炎、支气管扩张、右位心脏及不孕。先证者有一同胞妹妹,因车祸去世,其生前也有自幼上呼吸道感染,并支气管扩张。先证者父母为近亲结婚,均为正常人。结合先证者病史、检查及家族史,先证者被临床诊断为PCD。
PCD患者家系2,先证者为中年女性,36岁,河北人;表现为自幼反复的上呼吸道验证、鼻窦炎、支气管扩张、右位心脏。先证者父母为近亲结婚,均为正常人;先证者育有一女,身体健康。结合先证者者病史、检查及父母近亲结婚的情况,先证者被临床诊断为PCD。
两个先证者的病理诊断均为:原发性纤毛运动障碍征。
发明人收集获得上述PCD患者家系1中先证者及其父母(家系内正常人)的DNA样本,PCD患者家系2中先证者及其父母(家系内正常人)的DNA样本。
2、全外显子组测序确定致病基因及突变位点
发明人利用NimbleGen SeqCap EZ Human Exome Library v2.0全外显子捕获平台,结合Illumina Hiseq 2000高通量测序技术,对上述2个PCD患者家系中先证者及其父母(家系内正常人)均进行了全外显子组捕获测序,具体步骤如下:
2.1样品制备
分别取上述2个PCD患者家系中先证者及其父母(家系内正常人)的外周血,利用常规盐析法抽提基因组DNA,并利用分光光度计测量DNA的浓度及纯度,所得的每个标本基因组DNA的OD260/OD280均位于1.7-2.0之间,浓度不少于200ng/μl,总量不少于30μg,备用。
2.2文库构建及测序
利用超声波仪(CovarisS2,Massachusetts,USA)将各基因组DNA样本随机打断成250-300 bp左右的片段,随后按照制造商提供的操作说明书,在片段两端分别连接上接头制备文库(可参见:http://www.illumina.com/提供的Illumina/Solexa标准建库说明书,通过参照将其全文并入本文)。文库经纯化后经过Ligation-mediated PCR(LM-PCR)的线性扩增与捕获试剂SureSelect Biotiny lated RNA Library(BAITS)进行杂交富集,再经过LM-PCR的线性扩增,文库检测合格后即可上机测序,以便获得原始测序数据。其中,参照Illumina标准的成簇和测序的protocol进行测序,测序平台为Illumina Hiseq 2000,读取长度为90bp,样本的平均测序深度为50×。
2.3变异检测、注释及数据库比较
利用Illumina basecalling Software 1.7对上述获得的原始测序数据进行处理,经过过滤去污染后,使用SOAPaligner/SOAP2(可参见:Li R,Li Y,Kristiansen K,et al,SOAP:short oligonucleotide alignment program.Bioinformatics 2008,24(5):713-714;Li R,Yu C,Li Y,ea al,SOAP2:an improved ultrafast tool for short read alignment.Bioinformatics 2009,25(15):1966-1967,通过参照将其全文并入本文)比对到参考基因组UCSC NCBI37/hg19,以便获得比对到基因组上的唯一比对序列。然后利用SOAPsnp(可参见:Li R,Li Y,Fang X,Yang H,et al,SNP detection for massively parallel whole-genome resequencing.Genome Res 2009,19(6):1124-1132,通过参照将其全文并入本文)确定靶区域的基因型。
在得到测序结果之后,对非同义突变、剪接受体/供体位点突变、编码区插入和缺失突变这三类最有可能与病理相关的突变进行研究。结果,发明人通过测序分析发现,针对PCD患者家系1中,在先证者的DNA样本中发现100289个单核苷酸多态性(SNPs)和7059个插入/缺失(Indels),在先证者父亲的DNA样本中发现99191个SNPs和6960个Indels,在先证者母亲的DNA样本中发现97904个SNPs和6981个Indels;针对PCD患者家系2,在先证者的DNA样本中发现100414个单核苷酸多态性(SNPs)和7088个插入/缺失(Indels),在先证者父亲的DNA样本中发现103106个SNPs和7011个Indels,在先证者母亲的DNA样本中发现94530个SNPs和7017个Indels。随后通过dbSNP数据库(http://hgdownload.cse.ucsc.edu/goldenPath/hg19/database/snp132.txt.gz),HapMap数据库(ftp://ftp.ncbi.nlm.nih.gov/hapmap),千人基因组数据库(ftp://ftp.1000genomes.ebi.ac.uk/vol1/ftp),炎黄数据库(http://yh.genomics.org.cn/)等公共数据库的过滤,去掉所有已知的且在数据库中频率高的变异(变异MAF值高,通常为不致病的普通多态性)。同时过滤掉内含子或基因间区的突变以及其他区域的同义突变,即过滤掉不影响蛋白结构和功能的突变。接着,发明人结合两个PCD家系的实际情况及PCD特点,利用隐性遗传策略筛选获得的突变进行进一步分析。然后,将分析后的结果与目前已经报道的与PCD相关的基因列表取交集。结果,发明人从PCD患者家系1中得到DNAH5基因的c.G8030A突变(p.R2677Q),从PCD患者家系2中得到DNAH11基因的c.C6265T突变(p.R2089*)。
进一步分析可知,PCD患者家系1中先证者具有c.G8030A的纯合突变,其正常父母在该位点为杂合突变,该突变为已知基因的新突变且符合常隐模型,同时考虑测序质量高且SIFT预测突变有危害因素,发明人初步认为此突变为该家系的致病突变;PCD患者家系2中先证者c.C6265T的纯合突变,其正常父母在该位点为杂合突变,该突变为已知基因的新突变且符合常隐模型,同时考虑测序质量高且SIFT预测突变有危害因素,发明人初步认为此突变为该家系的致病突变。
由于外显子组测序存在一定程度的假阳性,接下来,发明人又利用Sanger测序方法,对上述确定的2个突变在2个PCD患者家系的先证者中分别进行了验证,结果显示DNAH5基因的c.G8030A突变及DNAH11基因的c.C6265T突变均为真实的突变。由此,表明DNAH5和DNAH11基因为原发性纤毛运动障碍征的致病相关基因,c.G8030A(DNAH5)和c.C6265T(DNAH11)突变是原发性纤毛运动障碍征的致病突变。
实施例2 Sanger法测序验证原发性纤毛运动障碍征的致病突变
分别对PCD患者家系1中的3人(先证者及其表现正常的父母)、PCD患者家系2中的4人(先证者及其为表现正常的父母)(见图2)的DNAH5和DNAH11基因进行检测,针对DNAH5基因的c.G8030A突变位点和DNAH11基因的c.C6265T突变位点所在序列设计引物,然后通过PCR扩增、产物纯化和测序的方法获得上述突变的有关序列,根据确定序列测定结果属于突变型还是野生型,是杂合突变还是纯合突变,以及序列与表型在家系内是否呈共分离来验证DNAH5和DNAH11与原发性纤毛运动障碍征之间的相关性。具体方法步骤如下:
1、DNA提取
分别采集上述PCD患者家系1中先证者及其表现正常的父母、PCD患者家系2中先证者及其表现正常的父母,然后利用QIAmp Blood kit(Qiagen,Hilden,Germany)抽提外周血白细胞中的基因组DNA,并利用Qubit Fluorometer和琼脂糖凝胶电泳测量所提取DNA的浓度及纯度,所得的每个标本基因组DNA的OD260/OD280均位于1.7-2.0之间,浓度不少于50ng/微升,总量不少于3μg,由此,获得各DNA样品,备用。
2、引物设计及PCR反应
首先,参考人类基因组序列数据库GRCh37.1/hg19,设计得到具有SEQ ID NO:5-6所示的核苷酸序列的DNAH5基因外显子特异性引物,以及具有SEQ ID NO:7-8所示的核苷酸序列的DNAH11基因外显子特异性引物,具体见下表。
DNAH5和DNAH11基因外显子特异性引物
接着,分别按照以下配比配制各基因组DNA样本的PCR反应体系以及进行PCR反应。
针对DNAH5基因的c.G8030A突变位点和DNAH11基因的c.C6265T突变位点所在的外显子序列,按以下配比分别配制各基因组DNA样本的各PCR反应体系:
反应体系:25μl
然后,将配制获得各PCR反应体系按照以下反应条件分别进行PCR反应(不同的突变位点采用相同的反应条件):
反应条件:
由此,获得上述PCD患者家系1中先证者及其表现正常的父母、PCD患者家系2中先证者及其表现正常的父母的PCR扩增产物。
3、测序
将步骤2中获得的获自PCD患者家系1中先证者及其表现正常的父母、PCD患者家系2中先证者及其表现正常的父母PCR扩增产物,进行DNA测序。其中,测序采用ABI3730型测序仪
基于测序结果,对上述各样本进行DNAH5和DNAH11基因编码序列比对。发明人发现,两个家系内的患者(先证者)及其家系内正常人(PCD患者家系1中先证者的父母、PCD患者家系2中先证者的父母)分别在c.G8030A(DNAH5)和c.C6265T(DNAH11)出现共分离现象,PCD患者家系1和PCD患者家系2的患者分别携带c.G8030A和c.C6265T突变。由此,证明DNAH5基因的c.G8030A突变、DNAH11基因的c.C6265T突变是原发性纤毛运动障碍征的致病突变。
其中,图3显示了PCD患者家系1内的先证者及其父母的DNAH5基因突变位点的Sanger测序验证峰图,图4显示了PCD患者家系2内的先证者及其父母的DNAH11基因突变位点的Sanger测序验证峰图。由图3和4可知,PCD患者家系1中患者的DNAH5基因具有c.G8030A突变,而该家系中的正常人不携带该突变;PCD患者家系2中患者的DNAH11基因具有c.C6265T突变,而该家系中的正常人不携带该突变。由此,进一步证明DNAH5基因的c.G8030A突变、DNAH11基因的c.C6265T突变是原发性纤毛运动障碍征的致病突变。
需要说明的是,DNAH5为已知PCD致病基因,国内外对该基因的致病性进行了大量的研究,DNAH5约占总PCD致病基因的28%,并被认为是PCD的主要致病基因。PCD的发病基础是动力纤毛的结构异常或调控动力纤毛过程出现异常。动力纤毛结构为9+2结构,中央为两个中心微小管,周围由次纤维A和次纤维B组成9对外周微小管,有动力臂、链接环和轮幅使之互相联接。动力臂有两条,分别是内侧动力臂(IDA)和外侧动力臂(ODA),在动力纤毛运动中起关键作用。目前大部分研究认为,DNAH5突变会导致外侧动力蛋白臂结构异常,但也有研究认为DNAH5突变会同时导致内外侧动力臂同时异常。DNAH11也是已知的PCD的致病基因,目前该基因的致病性已明确。DNAH11位于7号染色体短臂,具有82个外显子。目前研究显示,DNAH11并不造成动力纤毛的结构异常,其致病特点主要通过调解机制对动力纤毛的摆动产生影响。
综上,发明人进一步证明了DNAH5和DNAH11基因为原发性纤毛运动障碍征的致病相关基因,DNAH5基因的c.G8030A突变、DNAH11基因的c.C6265T突变是原发性纤毛运动障碍征的致病突变。
实施例3检测试剂盒
制备一检测试剂盒,其包含适于检测DNAH5和DNAH11基因突变体的至少一种的引物(其中与SEQ ID NO:1相比,所述DNAH5基因突变体具有c.G8030A突变;与SEQ ID NO:3相比,所述DNAH11基因突变体具有c.C6265T突变),以便用于筛选易患原发性纤毛运动障碍征的生物样品,其中这些引物包括SEQ ID NO:5-6所示的DNAH5基因外显子特异性引物(见实施例1),以及SEQ ID NO:7-8所示的DNAH11基因外显子特异性引物(见实施例1)。
利用上述试剂盒筛选易患原发性纤毛运动障碍征的生物样品的具体步骤为:按照实施例2的步骤1所述的方法提取待测者DNA,以所提取的DNA为模板与上述外显子特异性引物进行PCR反应,并按照本领域常规方法对PCR产物纯化,将纯化的产物进行测序,然后通过观察测序所得到的序列是否具有选自c.G8030A和c.C6265T的至少一种突变,从而有效地检测待测者是否易患原发性纤毛运动障碍征,进一步,能够从待测者中筛选出易患原发性纤毛运动障碍征的生物样品。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
尽管已经示出和描述了本发明的实施例,本领域的普通技术人员可以理解:在不脱离本发明的原理和宗旨的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由权利要求及其等同物限定。
- 还没有人留言评论。精彩留言会获得点赞!