兜甲蛋白减少的抑制/改善剂、谷氨酰胺转胺酶3激活剂和皮肤角质层角质化包膜的形成促进/结构增强剂的制作方法
相关申请参照
本申请基于在先的日本专利申请日本特愿2014-264578号(申请日:2014年12月26日),主张其优选权的利益,其全部公开内容通过参照而引入本申请中。
本发明涉及皮肤角质层角质化包膜(cornifiedenvelope)中的兜甲蛋白(loricrin)减少的抑制/改善剂、和皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的激活剂。另外本发明涉及皮肤角质层角质化包膜的形成促进/结构增强剂。它们对皮肤状态恶化的预防、抑制或改善是有用的。
背景技术:
表皮的角质层由表皮角质形成细胞(keratinocyte)终末分化而得的角质层细胞和包围该角质层细胞的角质层细胞间脂质构成。细胞间脂质由神经酰胺、胆固醇、脂肪酸等构成,通过脂质层与水分子层而形成片层结构。
另一方面,角质层细胞包含与保湿相关的成分角蛋白纤维、氨基酸等天然保湿因子。而且,角质层细胞通过角质化包膜(也称为角质包膜,或cornifiedenvelope,ce)这样的各种蛋白质的交联而被包裹在非常强韧的不溶性衬套结构中,对物理、化学的刺激非常稳定。构成角质化包膜的蛋白质中,特别是在颗粒层形成的兜甲蛋白承担增强该衬套结构的作用。在该结构中,作为蛋白质交联粘接酶的谷氨酰胺转胺酶3对在除了兜甲蛋白以外的蛋白质的交联反应中形成的未成熟的角质化包膜附着兜甲蛋白,形成成为角质化包膜的立足点的基础,从而完成。
皮肤的紫外线损伤(damage)引起皮肤的更新异常,特别是在最外层的角质层易受其影响。已知如果由于角质层细胞的损伤、角化不全而形成不完全的角质化包膜,则表皮角质层的屏障功能降低,角质层中保持的水分丧失。
从促进cornifiedenvelope(角质化包膜)的形成/成熟这样的观点出发,例如,日本特开2008-303185号公报公开了使用特定的吡咯烷酮衍生物。其中,研究了使未成熟的cornifiedenvelope成熟化。然而,就本发明者们所知,关于通过抑制由皮肤损伤等造成的兜甲蛋白减少,激活谷氨酰胺转胺酶3来促进角质化包膜的形成、增强其结构还基本没有进行研究。而且,就本发明者们所知,关于为了上述目的而经口摄取鞘脂、特别是鞘磷脂,到目前为止还不为人知。
日本特开2009-084244号公报中公开了通过连续经口摄取碳数10~36的饱和游离脂肪酸溶液而确认了皮肤的屏障功能的改善效果、神经酰胺量的增加效果、兜甲蛋白基因的表达增加效果。然而,这里关于经口摄取鞘磷脂既没有任何记载也没有任何启示。
日本特开2007-117793号公报公开了含有鞘磷脂作为有效成分的药品和饮食品,公开了鞘磷脂的唾液粘蛋白分泌促进作用、抗变态反应作用、抗氧化作用等各种作用。然而,这里关于鞘磷脂的抑制兜甲蛋白减少的作用、激活谷氨酰胺转胺酶3的作用既没有任何记载也没有任何启示。
hasegawa等的文献(hasegawatetal.,“dietaryglucosylceramideenhancescornifiedenvelopeformationviatransglutaminaseexpressionandinvolucrinproduction”,lipids(2011)46,pp.529-535)中报告了将魔芋来源的鞘脂葡糖苷酰鞘氨醇施与小鼠时,观察到小鼠的皮肤屏障功能改善、谷氨酰胺转胺酶1的表达上升、伞形蛋白(involucrin)的产生上升、谷氨酰胺转胺酶1和3的表达促进等作用。然而,确认了葡糖苷酰鞘氨醇与鞘磷脂结构不同,而且与施与鞘磷脂时作用的倾向完全不同。即,施与鞘磷脂时,实际确认了谷氨酰胺转胺酶1和伞形蛋白维持或降低(本发明的实施例),这是与施与葡糖苷酰鞘氨醇时完全相反的结果。
这样,就本发明者们所知,关于通过经口摄取鞘磷脂,来抑制兜甲蛋白减少,激活谷氨酰胺转胺酶3,由此促进角质化包膜形成,使其结构增强,目前还不为人知。
技术实现要素:
本发明者们现在意外地发现,通过经口摄取鞘脂、特别是鞘磷脂,能够抑制兜甲蛋白减少,激活谷氨酰胺转胺酶3。本发明者们着眼于通过抑制兜甲蛋白的减少、激活谷氨酰胺转胺酶3,从而促进角质化包膜形成,并增强未成熟状态的角质化包膜的结构。进而还发现由此能够改善皮肤恶化的状态,尤其能够抑制紫外线照射下的皮肤的屏障功能降低。本发明是基于这些见解而做出的。
于是,本发明的目的是提供皮肤角质层角质化包膜中的兜甲蛋白减少的抑制/改善剂、和皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的激活剂。另外,本发明的目的是提供皮肤角质层角质化包膜的形成促进/结构增强剂。进而,本发明的目的是提供用于安全且简易、经济地预防、抑制或改善由紫外线照射等造成的皮肤的屏障功能的降低的组合物和饮食品。
即,根据本发明,提供以下的发明。
<1>皮肤角质层角质化包膜中的兜甲蛋白减少的抑制/改善剂,以鞘磷脂作为有效成分。
<2>皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的激活剂,以鞘磷脂作为有效成分。
<3>皮肤角质层角质化包膜的形成促进/结构增强剂,以鞘磷脂作为有效成分。
<4>前述<1>的角质化包膜的形成促进/结构增强剂,优选角质化包膜的形成促进/结构增强是通过利用鞘磷脂来抑制/改善皮肤角质层角质化包膜中的兜甲蛋白减少和激活谷氨酰胺转胺酶3,从而实现的。
<5>前述<1>~<4>的任一减少的抑制/改善剂、激活剂或形成促进/结构增强剂,优选鞘磷脂是乳来源的鞘磷脂。
<6>经口摄取用或经肠道施与用组合物,包含前述<1>或<5>的兜甲蛋白减少的抑制/改善剂、前述<2>或<5>的谷氨酰胺转胺酶3的激活剂、或前述<3>~<5>的任一角质化包膜的形成促进/结构增强剂。
<7>前述<6>的组合物,优选用于预防、抑制或改善皮肤状态恶化。
<8>前述<7>的组合物,优选皮肤状态恶化是皮肤的屏障功能降低。
<9>前述<7>或<8>的组合物,优选皮肤的屏障功能降低是由紫外线照射引起的。
<10>前述<6>~<9>的任一组合物,优选包含每天能够摄取0.5~1500mg的量的鞘磷脂。
<11>饮食品,包含前述<1>或<5>的兜甲蛋白减少的抑制/改善剂、前述<2>或<5>的谷氨酰胺转胺酶3的激活剂、或前述<3>~<5>的任一角质化包膜的形成促进/结构增强剂。
<12>饮食品,包含前述<6>~<9>的任一组合物。
<13>前述<11>或<12>的饮食品,优选每一包装形态包含能够摄取0.2~45000mg的量的鞘磷脂。
<14>前述<11>~<13>的任一饮食品,优选是功能性食品、健康营养食品、补充剂、特定保健用食品、功能性标示食品或带疾病风险降低标示的食品。
<15>兜甲蛋白减少的抑制/改善方法,包括使皮肤角质层角质化包膜中的兜甲蛋白的量降低了的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂。
<16>皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的激活方法,包括使皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的活性降低了的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂。
<17>皮肤角质层角质化包膜的形成促进/结构增强方法,包括通过使要求皮肤角质层中的角质化包膜的形成促进/结构增强的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂,从而抑制或改善皮肤角质层角质化包膜中的兜甲蛋白减少,激活谷氨酰胺转胺酶3。
发明的效果
根据本发明,能够抑制/改善皮肤角质层角质化包膜中的兜甲蛋白减少,另外能够激活皮肤角质层角质化包膜中的谷氨酰胺转胺酶3。通过抑制兜甲蛋白减少、激活谷氨酰胺转胺酶3,能够促进角质化包膜形成,并增强未成熟状态的角质化包膜的结构。特别是本发明的减少抑制/改善剂、激活剂或形成促进/结构增强剂、和组合物能够有效地预防、抑制或改善紫外线照射下的皮肤的屏障功能降低。进而,本发明的产生促进剂和组合物是通过经口或经肠道途径摄取的,另外,原料以以往有作为食品使用的经验的物质为来源,因而安全且简易,经济性也优异。
附图说明
图1是显示实施例的试验流程的概念图。
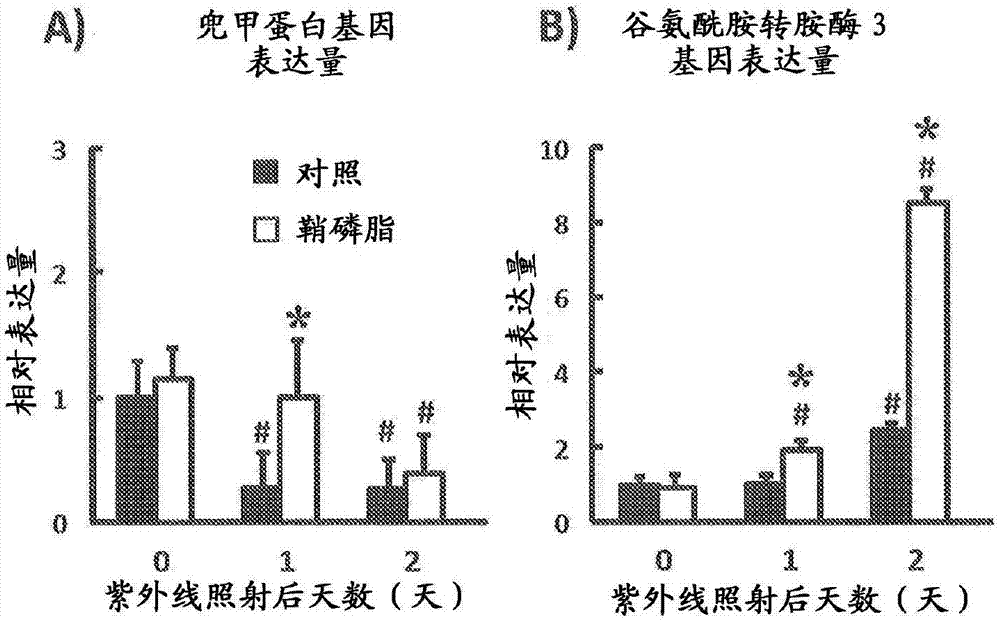
图2是显示实施例中的兜甲蛋白基因的表达量的变化和谷氨酰胺转胺酶3基因的表达量的变化的柱状图。其中,图2(a)显示兜甲蛋白基因的表达量的变化,图2(b)显示谷氨酰胺转胺酶3基因的表达量的变化。另外,图中*表示相对于对照组有显著性差异(p<0.05),#表示相对于第0天有显著性差异(p<0.05)。
图3是显示实施例中的谷氨酰胺转胺酶1基因的表达量的变化和伞形蛋白基因的表达量的变化的柱状图。其中,图3(c)显示谷氨酰胺转胺酶1基因的表达量的变化,图3(d)显示伞形蛋白基因的表达量的变化。另外,图中,*表示相对于对照组有显著性差异(p<0.05),#表示相对于第0天有显著性差异(p<0.05)。
具体实施方式
以下对于本发明的实施方式进行说明。
皮肤角质层角质化包膜中的兜甲蛋白减少的抑制/改善剂
本发明的皮肤角质层角质化包膜中的兜甲蛋白减少的抑制/改善剂如前所述以鞘磷脂作为有效成分。
其中,“作为有效成分”是指含有对于本发明的减少抑制/改善剂在生物体内的皮肤角质层角质化包膜中发挥抑制或改善兜甲蛋白减少的作用充分的使用量(即,有效量)的鞘磷脂。
另外,这里,“兜甲蛋白减少的抑制/改善”是指抑制或改善皮肤角质层角质化包膜中的兜甲蛋白减少、可以包含抑制或延迟减少的发展、使减少停止而维持,抑制减少而转为增加的任一含义。进而“兜甲蛋白减少的抑制/改善”也包含减少的预防。
“兜甲蛋白”是皮肤的角质化包膜的衬套结构的主要构成蛋白质,例如,如后述实施例所记载的那样,以兜甲蛋白基因的表达状态作为指标,能够评价皮肤角质层角质化包膜中的兜甲蛋白的减少状态。
谷氨酰胺转胺酶3的激活剂
本发明的皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的激活剂如前所述以鞘磷脂作为有效成分。
这里,“作为有效成分”是指含有对于本发明的激活剂在生物体内的皮肤角质层角质化包膜中发挥激活谷氨酰胺转胺酶3的作用充分的使用量(即,有效量)的鞘磷脂。
另外,这里,“谷氨酰胺转胺酶3的激活”以包含皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的酶活性被激活、从活性降低了的状态活性被提高、维持活性高的状态的含义使用。
“谷氨酰胺转胺酶3”是具有使角质化包膜附着兜甲蛋白、增强角质化包膜的衬套结构的功能的酶,例如,如后述的实施例所记载的那样,以谷氨酰胺转胺酶3基因的表达状态作为指标,能够评价皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的活性。
皮肤角质层角质化包膜的形成促进/结构增强剂
本发明的皮肤角质层角质化包膜的形成促进/结构增强剂如前所述以鞘磷脂作为有效成分。
这里,“作为有效成分”是指含有对于本发明的形成促进/结构增强剂显示促进皮肤角质层角质化包膜形成、和/或增强其结构的效果充分的使用量(即,有效量)的鞘磷脂。
另外,这里,“皮肤角质层角质化包膜的形成促进/结构增强”以包含促进皮肤角质层角质化包膜形成、使未成熟的角质化包膜成熟化、增强角质化包膜的结构的含义使用。
根据本发明的优选方式,在角质化包膜的形成促进/结构增强剂中,角质化包膜的形成促进/结构增强是通过利用鞘磷脂来抑制/改善皮肤角质层角质化包膜中的兜甲蛋白减少和激活谷氨酰胺转胺酶3,从而实现的。
鞘磷脂
在本说明书中,鞘磷脂是鞘脂的一种。这里,鞘脂是天然来源的鞘脂,可列举例如,牛乳、山羊乳、羊乳、马乳等乳来源的鞘脂、蛋黄来源的鞘脂、米、玉米、谷物来源的鞘脂、魔芋来源、甜菜来源等,优选为乳来源的鞘脂,更优选为牛乳来源的鞘脂。因此,能够在本发明中使用的鞘磷脂与前述的鞘脂同样地为天然来源的鞘磷脂,优选为乳来源的鞘磷脂,更优选为牛乳来源的鞘磷脂。鞘磷脂可以由天然原料通过惯用的方法制备,也可以使用市售品。
根据本发明的优选方式,鞘磷脂为乳来源的鞘磷脂。
能够在本发明中使用的乳来源的鞘磷脂优选包含选自十四烷基鞘氨醇磷酸胆碱(d18:1-c14:0)、二十三烷基鞘氨醇磷酸胆碱(d18:1-c23:0)、十六烷基鞘氨醇磷酸胆碱(d18:1-c16:0)、二十三烯基鞘氨醇磷酸胆碱(d18:1-c23:1)、十八烷基鞘氨醇磷酸胆碱(d18:1-c18:0)、二十四烷基鞘氨醇磷酸胆碱(d18:1-c24:0)、二十烷基鞘氨醇磷酸胆碱(d18:1-c20:0)、二十四烯基鞘氨醇磷酸胆碱(d18:1-c24:1)、二十二烷基鞘氨醇磷酸胆碱(d18:1-c22:0)和二十六烷基鞘氨醇磷酸胆碱(d18:1-c26:0)中的一种以上分子种类。所述乳来源的鞘磷脂更优选包含选自前述的组中的三种以上分子种类,更进一步优选包含选自前述的组中的五种以上分子种类。
本发明的减少抑制/改善剂、激活剂或形成促进/结构增强剂优选为经口摄取用(即,经口摄取剂)或经肠道施与用(即,经肠道施与剂)。
本发明的减少抑制/改善剂、激活剂或形成促进/结构增强剂优选用于状态恶化的皮肤、屏障功能降低的皮肤。
如后述的实施例所示,根据本发明,在皮肤的角质化包膜的兜甲蛋白减少那样的皮肤屏障功能降低的状态下,能够通过抑制/改善兜甲蛋白减少,来保持或改善皮肤屏障功能。同样地,如后述的实施例所示,根据本发明,在皮肤的角质化包膜的谷氨酰胺转胺酶3的活性降低那样的皮肤屏障功能降低的状态下,能够通过激活谷氨酰胺转胺酶3,来保持或改善皮肤屏障功能。进而,通过皮肤角质层角质化包膜中的兜甲蛋白减少的抑制/改善和谷氨酰胺转胺酶3的激活,从而角质化包膜的形成被促进/结构被增强,由此能够改善状态恶化的皮肤、屏障功能降低的皮肤。
因此,本发明的减少抑制/改善剂、激活剂或形成促进/结构增强剂更优选用于状态恶化的皮肤、屏障功能降低的皮肤。
用途
本发明中的有效成分鞘磷脂能够抑制/改善皮肤角质层角质化包膜中的兜甲蛋白减少,另外,能够激活皮肤角质层角质化包膜中的谷氨酰胺转胺酶3(后述的实施例)。由此,能够促进角质化包膜形成,另外,能够增强未成熟的状态的角质化包膜的结构。进而,本发明中的有效成分鞘磷脂具有皮肤状态恶化的预防、抑制或改善效果。
这里,所谓皮肤状态恶化包含例如,皮肤的屏障功能降低、皮肤干燥、皮肤粗糙、角质层的水分量降低、特应性皮炎等。皮肤的屏障功能降低也包含屏障功能的维持。另外,皮肤的屏障功能降低优选为皮肤在紫外线照射下的屏障功能降低。
另外,这里,恶化的状态的“预防、抑制或改善”以包含这样的状态的调节、发展延迟、缓和、发病预防、复发预防等的含义使用。
根据本发明的另外方式,可以谋求能够通过抑制/改善兜甲蛋白减少或激活谷氨酰胺转胺酶3来治疗、预防或改善的状态的治疗、预防或改善。
根据本发明的优选的另外一种方式,提供皮肤的状态恶化的预防、抑制或改善方法,包括使皮肤角质层角质化包膜中的兜甲蛋白的量降低了的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂。
另外,根据本发明的优选的另外一种方式,提供皮肤状态恶化的预防、抑制或改善方法,包括使皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的活性降低了的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂。
根据本发明的优选的再另外一种方式,提供皮肤状态恶化的预防、抑制或改善方法,包括通过使要求皮肤角质层中的角质化包膜的形成促进/结构增强的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂,从而进行皮肤角质层角质化包膜中的兜甲蛋白减少的抑制或改善,激活谷氨酰胺转胺酶3。
根据本发明的另外方式,提供用于抑制或改善皮肤角质层角质化包膜中的兜甲蛋白减少的鞘磷脂。
根据本发明的另外方式,提供用于激活皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的鞘磷脂。
根据本发明的另外方式,提供用于促进皮肤角质层角质化包膜的形成和/或增强其结构的鞘磷脂。
根据本发明的优选的另外一种方式,提供鞘磷脂用于抑制/改善皮肤角质层角质化包膜中的兜甲蛋白减少的应用。另外根据本发明的更优选的另外一种方式,提供鞘磷脂在用于抑制/改善皮肤角质层角质化包膜中的兜甲蛋白减少的经口摄取用或经肠道施与用组合物的制造中的应用。这里,所述应用可以是非治疗的应用。
根据本发明的优选的另外一种方式,提供鞘磷脂用于激活皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的应用。另外本发明的更优选的另外一种方式,提供鞘磷脂在用于激活皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的经口摄取用或经肠道施与用组合物的制造中的应用。这里,所述应用可以是非治疗的应用。
根据本发明的优选的另外一种方式,提供鞘磷脂用于促进皮肤角质层角质化包膜的形成和/或增强其结构的应用。另外根据本发明的更优选的另外一种方式,提供鞘磷脂在用于促进皮肤角质层角质化包膜的形成和/或增强其结构的经口摄取用或经肠道施与用组合物药品的制造中的应用。这里,所述应用可以是非治疗的应用。
组合物和饮食品
如前所述,根据本发明,提供包含本发明的减少抑制/改善剂、激活剂或形成促进/结构增强剂的经口摄取用或经肠道施与用组合物。另外,根据本发明,提供包含本发明的减少抑制/改善剂、激活剂或形成促进/结构增强剂的饮食品。
这样的组合物和饮食品可以通过例如,本发明的包含将本发明的减少抑制/改善剂、激活剂或形成促进/结构增强剂添加到组合物和饮食品的材料成分中的制造方法,从而制造。
本发明的经口摄取用或经肠道施与用组合物优选为用于皮肤状态恶化的预防、抑制或改善。即,根据本发明,提供皮肤状态恶化的预防、抑制或改善用组合物。
本发明的皮肤状态恶化的预防、抑制或改善用组合物,作为一种优选的方式,是药品组合物。
在本发明中,药物组合物是合并使用可容许用于制剂化的添加剂、按照常规方法以经口制剂或非经口制剂形式而制备的。从简易性的观点考虑,优选为经口制剂。在经口制剂的情况下能够采取片剂、散剂、细粒剂、颗粒剂、胶囊剂、丸剂、缓释剂等固体制剂、溶液、悬浮液、乳浊液等液状制剂的形态。作为可容许用于制剂化的添加剂,例如可以举出赋形剂、稳定剂、防腐剂、润湿剂、乳化剂、润滑剂、甜味剂、着色剂、香料、缓冲剂、抗氧化剂、ph调节剂等。
本发明的饮食品中可以根据需要加入任意成分。作为这样的可任意添加的成分,没有特别限制,可以配合通常能够配合在饮食品中的成分、甜味剂、酸味剂、蔬菜和/或水果和/或坚果的汁和/或其提取物、维生素、矿物质、氨基酸等营养素、乳酸菌、双歧杆菌、丙酸菌等有用微生物和/或其培养物、低聚糖等具有功能性的糖类、蜂王浆、胶原、神经酰胺、氨基葡萄糖、虾青素、多酚等现有的功能性材料、香料、ph调节剂、赋形剂、酸味剂、着色剂、乳化剂、保存剂等。
在本发明中,饮食品是指除药物组合物以外的物质,只要是溶液、悬浮液、乳浊液、粉末、固体成形物等可经口摄取的形态即可,没有特别限定。具体而言,例如可以举出乳饮料、酸奶类、乳酸菌饮料、发酵乳、冰淇淋类、奶油类、乳酪类等乳制品;清凉饮料、果汁饮料、蔬菜饮料、豆乳饮料、咖啡饮料、茶饮料、果冻饮料、可可、冰沙等粉末饮料和/或运动粉末饮料、营养强化的粉末饮料、美容用的粉末食品、粉末汤、蒸点心的材料、浓缩饮料、酒精饮料等饮料类;面包、意大利面、面条、蛋糕预拌粉、油炸面粉、面包粉等小麦粉制品;巧克力、口香糖、糖、饼干、软糖、零食、日本点心、果冻、布丁等餐后甜点等点心糖果类;加工调味料、风味调味料、预混烹饪料等调味料;咖喱、意大利面酱料、浓汤、炖菜、日本风味食品的软罐头食品;加工油脂、黄油、人造黄油、涂抹酱料、蛋黄酱等油脂类;冻干食品等快餐食品类;农产罐头、果酱/柑橘酱类、酱菜、煮豆、谷物品、菜粥等农产加工品;水产加工品;畜产加工品;比萨饼、鱼贝鸡米饭、奶汁烤干酪烙菜、家常菜、面拖等冷冻食品;流质食物、以及动物的饲料、小片、口腔内使用的化妆品等。
根据本发明的一个优选方式,饮食品是乳饮料(可以包含加工乳)、发酵乳、清凉饮料、果冻饮料、小片、美容用粉末食品、粉末饮料、流质食物、液状的配方奶粉,根据更优选的方式,饮食品是乳饮料、发酵乳、清凉饮料、果冻饮料、小片、美容用的粉末食品,根据进一步优选的方式,饮食品是乳饮料(可以包含加工乳)、发酵乳。
另外,饮食品也包含功能性食品、健康营养食品、补充剂、健康食品、特定保健用食品、功能性标示食品、营养功能食品、患者用食品、婴幼儿配方奶粉、孕产妇或哺乳期妇女用奶粉或带有疾病风险降低标示的饮食品这样分类的食品。根据本发明的一个优选方式,饮食品是功能性食品、健康营养食品、补充剂、特定保健用食品、功能性标示食品或带有疾病风险降低标示的食品。
此外,这里,疾病风险降低标示是有降低疾病风险的可能性的饮食品的标示,可以是基于fao/who联合食品标准委员会(食品法典委员会)制定的标准或参考该标准而规定的标示或被认可的标示。
因此,本发明的饮食品可以作为例如适于期待改善或缓和皮肤状态恶化的消费者的食品、适于改善皮肤状态恶化的食品、即所谓特定保健用食品或功能性标示食品的形式提供。
根据本发明的另外方式,能够提供标示了预防、抑制或改善皮肤状态恶化的功能的饮食品。
有效成分在饮食品及组合物中的含量可以根据组合物的种类、方式、预防/改善的目的等而变化,因此,难以一概规定,在本发明的组合物中,可以调整到成人(体重:60kg)能够以每天0.5~1500mg、优选1~1000mg、更优选5~500mg摄取鞘磷脂的有效量。
鞘磷脂的含量可以通过惯用的方法测定,例如采用液相色谱法使用aquasilsp100(4.6×250mm,センシュー科学社)作为柱来测定。
此时,作为流动相,例如可使用使0.5mm磷酸-柠檬酸缓冲液(ph3.0)与甲醇以5比95的比例混合而得的溶液。可以将测定时间设定为20分钟,流动相的流速设定为0.6ml/分钟,柱温设定为40℃,以吸光度205nm进行检测。作为标准物质,可以使用例如鞘磷脂(乳来源,長良サイエンス社制造),可以通过面积比来定量。
在本发明的另外方式中,有效成分在饮食品及组合物中的含量也可以以每一包装形态规定,例如饮食品的情况下,鞘磷脂的含量可以以5~1500mg、优选6~1000mg、更优选7~500mg包含,另外,组合物的情况下,鞘磷脂的含量可以以0.5~1500mg、优选1~1000mg、更优选5~500mg包含。另外,每一包装形态的量(含量)不限于一次的摄取量,也可以包括多次份或多天份(例如30天份)的摄取量,例如饮食品的情况下,鞘磷脂的含量可以以5~45000mg、优选为6~30000mg、更优选为7~15000mg包含,另外,组合物的情况下,鞘磷脂的含量可以以0.5~45000mg、优选为1~30000mg、更优选为5~15000mg包含。
现有的常见乳饮料、发酵乳中,每1g脂质包含磷脂20mg,而本发明的乳饮料、发酵乳中,每1g脂质可以包含磷脂25~3000mg,优选30~2500mg,更优选40~2000mg,进一步优选50~1500mg。另外,现有的常见乳饮料、发酵乳中,每1g脂质包含鞘磷脂6mg,而本发明的乳饮料、发酵乳中,每1g脂质可以包含鞘磷脂7~1500mg,优选8~1250mg,更优选9~1000mg,进一步优选10~750mg。
即,在本发明的一个优选方式中,可以使用有意地提高了鞘磷脂含量的乳饮料或发酵乳。
在本发明的乳饮料、发酵乳中,可以以通常量包含脂质(例如,以3重量%包含脂质),可以包含鞘磷脂0.2~60mg/g,优选为0.25~50mg/g、更优选为0.3~40mg/g、进一步优选为0.35~30mg/g。
另一方面,本发明的乳饮料、发酵乳中,在少量包含脂质(例如以1重量%包含脂质的低脂肪的)的情况下,可以包含鞘磷脂0.05~60mg/g,优选为0.1~50mg/g,更优选为0.15~40mg/g,进一步优选为0.2~30mg/g。
而且,本发明的乳饮料、发酵乳、清凉饮料、果冻饮料、小片、美容用的粉末食品中,在几乎不含脂质(无脂肪)的情况下,可以包含鞘磷脂0.02~60mg/g,优选为0.04~50mg/g,更优选为0.06~40mg/g,进一步优选为0.08~30mg/g。
因此,根据本发明的一个更优选方式,提供包含补加的鞘磷脂的乳饮料和/或发酵乳,进而提供包含这样的乳饮料和/或发酵乳的组合物或饮食品。作为这样的组合物或饮食品,可列举例如酸奶。
例如,在酸奶的情况下,可以提供包含补加的鞘磷脂的酸奶,这是指不仅包含酸奶本来可包含的鞘磷脂,还对酸奶另外添加鞘磷脂而有意识地提高了鞘磷脂的浓度的酸奶。此时,这里所说的“补加的鞘磷脂”不是酸奶本来可包含的鞘磷脂,而是指在制作有意识地提高了鞘磷脂的浓度的酸奶时添加的、另外添加的鞘磷脂。
于是,根据本发明的另外优选方式,提供包含本发明的兜甲蛋白减少的抑制/改善剂、本发明的谷氨酰胺转胺酶3的激活剂、或本发明的角质化包膜的形成促进/结构增强剂的酸奶。
另外根据本发明的另外一个优选方式,提供具有兜甲蛋白减少的抑制/改善作用的酸奶,包含补加的鞘磷脂。
根据本发明的另外一个优选方式,提供具有谷氨酰胺转胺酶3的激活作用的酸奶,包含补加的鞘磷脂。
根据本发明的另外一个优选方式,提供具有角质化包膜的形成促进/结构增强作用的酸奶,包含补加的鞘磷脂。
根据本发明的另外方式,提供兜甲蛋白减少的抑制/改善方法,包括使皮肤角质层角质化包膜中的兜甲蛋白的量降低了的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂。
这里,兜甲蛋白的量是指皮肤角质层角质化包膜中的兜甲蛋白的存在量,例如,可以以兜甲蛋白基因的表达量来评价。
根据本发明的另外方式,提供皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的激活方法,包括使皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的活性降低了的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂。
这里,谷氨酰胺转胺酶3的活性,例如,可以以谷氨酰胺转胺酶3基因的表达量来评价。
根据本发明的另外方式,提供皮肤角质层角质化包膜的形成促进/结构增强方法,包括通过使要求皮肤角质层中的角质化包膜的形成促进/结构增强的对象经口摄取鞘磷脂,或对所述对象经肠道施与鞘磷脂,从而抑制或改善皮肤角质层角质化包膜中的兜甲蛋白减少,激活谷氨酰胺转胺酶3。
此外,这里,优选前述方法是除了医疗用途以外的方法。另外,前述对象优选为人或除人以外的哺乳类。
而且,前述方法优选可以是2天以上连续经口摄取或经肠道施与鞘磷脂的用于皮肤角质层角质化包膜中的兜甲蛋白的量降低了的对象的兜甲蛋白减少的抑制/改善方法、用于皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的活性降低了的对象的皮肤角质层角质化包膜中的谷氨酰胺转胺酶3的激活方法、或皮肤角质层角质化包膜的形成促进/结构增强方法。
实施例
以下,通过下述实施例详细说明本发明,但本发明不限定于这些实施例。
试验:鞘磷脂对紫外线照射下的皮肤的屏障功能恶化的影响
对无毛小鼠照射紫外线(gl20se、三共电气株式会社制),使皮肤的屏障功能恶化,评价鞘磷脂的连续经口摄取的影响。
<实验方法>
(1)通过紫外线照射使皮肤的屏障功能恶化
将无毛小鼠(hos:hr-1、雌、8周龄),然后在1周之后以20mj/cm2的条件照射紫外线(uv-b)。
试验中,由于各测定和皮肤的采取需要个体,因而共计使用48只小鼠,以每组各8只小鼠进行分组。
(2)组构成和试验步骤
使用前述(1)中制成的紫外线照射模型动物的试验系统,评价鞘磷脂(纯度98%、長良サイエンス社制)的经口摄取(经口施与)对皮肤的基因表达的影响。
供于试验的各组条件如下所述。
从分组日起在9天间进行经口施与。
(i)对照第0天组
(ii)对照第1天组
(iii)对照第2天组
(iv)鞘磷脂摄取第0天组
(v)鞘磷脂摄取第1天组
(vi)鞘磷脂摄取第2天组
在对照第0、1、2天组中,摄取通常饲料,以10ml/kg-bw/天经口施与溶剂(乙醇的5%水溶液)。另外,在鞘磷脂摄取第0、1、2天组中,以10ml/kg-bw/天经口施与鞘磷脂(纯度:98%、長良サイエンス社):146mg/10ml-溶剂(乙醇5%水溶液)。
试验具体按照图1的流程,在照射前(第0天)、照射第1天和照射第2天对于规定的组定量兜甲蛋白基因和谷氨酰胺转胺酶3基因的表达量。此时,也定量谷氨酰胺转胺酶1基因和伞形蛋白基因的表达量。
(兜甲蛋白、谷氨酰胺转胺酶3、谷氨酰胺转胺酶1和伞形蛋白的各基因的表达量的定量法)
从由各个体采取的皮肤样品使用rneasyfibiroustissueminikit(qiagen社)提取总rna,由从皮肤提取的1.5μg当量的总rna使用rivertaidfirststrandcdnasynthesiskit(thermoscientific社)进行互补dna(cdna)合成和逆转录反应。
合成的cdna通过rt-pcr法,引物使用taqmangeneexpressionassay(appliedbiosystems社),通过7500实时pcrsystem(appliedbiosystems社制)测定各样品的靶标基因兜甲蛋白(loricrin)(assayid:mm01962650_s1)、谷氨酰胺转胺酶3(transglutaminase3)(assayid:mm00436999_m1)、谷氨酰胺转胺酶1(transglutaminase1)(assayid:mm00498375_m1)、和伞形蛋白(involcrin)(mm00515219_s1)的mrna表达量。
同时,测定甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphatedehydrogenase(gapdh))(assayid:mm99999915_g1)的mrna表达量作为内标。
定量化通过δδct法来进行,作为相对表达量,计算出各组的皮肤样品的靶标基因表达量相对于对照第0天组的靶标基因表达量的各组的靶标基因表达量的比率。
具体地,使用如下所述的算式计算相对表达量。
δct=(各个体样品的靶标基因的ct值)―(各个体样品的gapdh基因的ct值)
δδct=(各个体样品的靶标基因的δct值)―(对照第0天组的δct平均值)
基因表达量=2-δδct
相对表达量=(各个体样品的靶标基因的2-δδct)/(对照第0天组的2-δδct平均值)
(3)试验结果
通过兜甲蛋白基因和谷氨酰胺转胺酶3基因的表达量,来评价与角质化包膜的形成促进、结构增强相关的基因的表达的变化。
其中,如果与对照第0、1、2天组相比,在鞘磷脂摄取第0、1、2天组中兜甲蛋白基因的表达量为高值,则说明兜甲蛋白的表达降低被抑制。另外,如果与对照第0、1、2天组相比,在鞘磷脂摄取第0、1、2天组中谷氨酰胺转胺酶3基因的表达量为高值,则说明谷氨酰胺转胺酶3基因的表达上升被促进。
另一方面,关于谷氨酰胺转胺酶1基因的表达量,如果与对照第0、1、2天组相比,在鞘磷脂摄取第0、1、2天组中谷氨酰胺转胺酶1基因的表达量为低值,则说明谷氨酰胺转胺酶1基因的表达上升被抑制。另外,如果与对照第0、1、2天组相比,在鞘磷脂摄取第0、1、2天组中伞形蛋白基因的表达量为低值,则说明伞形蛋白基因的表达上升被抑制。
结果如图2和3所示。
由图2(a)可知,与对照第1天组(紫外线照射1天后)相比,在鞘磷脂摄取第1天组中,兜甲蛋白基因的表达量为高值。
由图2(b)可知,与对照第1天组(紫外线照射1天后)和对照第2天组(紫外线照射2天后)相比,在鞘磷脂组摄取第1天组和鞘磷脂组摄取第2天组中,谷氨酰胺转胺酶3基因的表达量为高值。
由图3(a)可知,与对照第1/2/3天组(对照组)(紫外线照射第1/2/3天后)相比,在鞘磷脂摄取第1/2/3天组中,谷氨酰胺转胺酶1基因的表达量分别为低值。
由图3(b)可知,与对照第1/2/3天组(sm组)(紫外线照射第1/2/3天后)相比,在鞘磷脂摄取第1/2/3天组中,伞形蛋白基因的表达量分别为低值。
这些结果启示了,通过经口摄取鞘磷脂,由紫外线照射引起的兜甲蛋白基因的表达降低被抑制,并且谷氨酰胺转胺酶3基因的表达上升被促进,实现了角质化包膜的形成促进、结构增强。
另外,通过经口摄取鞘磷脂,谷氨酰胺转胺酶1基因、伞形蛋白基因的表达上升没有被促进,由此启示了鞘磷脂的经口摄取特异性地贡献于与角质化包膜的形成促进、结构增强相关的特异基因(这里为兜甲蛋白基因、谷氨酰胺转胺酶3基因)的表达促进。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种制备自噬小体型瘤苗的培养基添加剂及其制备方法与制造工艺
- N-萘烷基取代的含氮杂环衍生物、制备方法及其抗肿瘤用途与制造工艺
- 作为BET蛋白抑制剂的1H‑吡咯并[2,3‑c]吡啶‑7(6H)‑酮和吡唑并[3,4‑c]吡啶‑7(6H)‑酮的制造方法与工艺
- 一种人肿瘤抑制蛋白变体及其应用的制造方法与工艺
- 一种人肿瘤抑制蛋白变体及其应用的制造方法与工艺
- G蛋白信号调节因子6及其抑制剂在治疗脂肪肝和Ⅱ型糖尿病中的功能和应用的制造方法与工艺
- 蛋白酶体抑制剂在制备降低动物脂含量或脂储积能力产品中的应用的制造方法与工艺
- GINS2基因或蛋白的抑制剂在制备抗肿瘤药物中的应用的制造方法与工艺
- ZNF383蛋白在制备抑制p53蛋白活性的产品中的应用的制造方法与工艺
- 蛋白酶体抑制剂MLN9708的合成方法与制造工艺